
下列说法正确的是()
A. NaHSO4无论在水溶液或熔融状态下都可以电离出Na+、H+和SO42﹣
B. NaCl溶液能导电是因为溶液中有自由移动的Na+和Cl﹣
C. H2SO4在电流作用下在水中电离出H+和SO42﹣
D. 液态HCl,固态NaCl均不导电,所以HCl、NaCl都不是电解质
考点: 电解质在水溶液中的电离.
分析: A.硫酸氢钠在熔融状态下电离出钠离子和硫酸根离子;
B.含有自由移动离子或电子的物质能导电;
C.硫酸在水分子的作用下电离出自由移动的阴阳离子;
D.HCl、NaCl都是强电解质,不含自由移动离子的强电解质不导电.
解答: 解:A.硫酸氢钠在熔融状态下电离出钠离子和硫酸根离子,在水溶液中电离出Na+、H+和SO42﹣,故A错误;
B.含有自由移动离子或电子的物质能导电,氯化钠的水溶液中,NaCl在水分子的作用下电离出自由移动的Na+和Cl﹣,所以氯化钠溶液能导电,故B正确;
C.硫酸在水分子的作用下电离出自由移动的阴阳离子,不需要电流,故C错误;
D.不含自由移动离子的强电解质不导电,HCl、NaCl都是强电解质,但因为液态HCl、固态NaCl不含自由移动的离子,所以不导电,故D错误;
故选B.
点评: 本题考查电解质的电离及物质导电性,为高频考点,知道物质导电原理即可解答,易错选项是AC,注意硫酸氢钠在水溶液中和熔融状态下电离方式的区别,注意电解质不一定导电,导电的不一定是电解质,为易错点.


 口算能手系列答案
口算能手系列答案科目:高中化学 来源: 题型:
下表列出了a﹣f六种元素在周期表前三周期的位置.
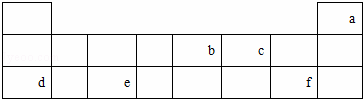
请回答下列问题:
(1)c元素的名称是氧,d元素位于IA族.
(2)用元素符号表示,六种元素中,性质最稳定的元素原子结构示意图 , 元素的原子半径最大.
(3)非金属性b c.(填“大于”“小于”)
(4)用化学式表示,六种元素中,最高价氧化物属于两性氧化物的是 ,最高价氧化物对应水化物酸性最强的是 4
(5)写出d元素单质与水反应的离子方程式
(6)写出e元素单质与NaOH反应的离子方程式
(7)用电子式表示化合物d2c的形成过程 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中,正确的是()
A. 含金属元素的离子一定都是阳离子
B. 在氧化还原反应中,非金属单质一定是氧化剂
C. 某元素从化合态变为游离态时,该元素一定被还原
D. 金属阳离子被还原不一定得到金属单质
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是()
①标准状况下,6.02×1023个分子所占的体积约是22.4L
②0.5mol H2所占体积为11.2L
③标准状况下,1mol H2O的体积为22.4L
④常温常压下,28g CO与N2的混合气体所含的原子数为2NA
⑤各种气体的气体摩尔体积都约为22.4L•mol﹣1
⑥标准状况下,体积相同的气体的分子数相同.
A. ①③⑤ B. ④⑥ C. ③④⑥ D. ①④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
氧化还原反应中,水的作用可以是氧化剂、还原剂、既是氧化剂又是还原剂、既非氧化剂又非还原剂等.下列反应与Br2+SO2+2H2O=H2SO2+2HBr相比较,水的作用相同的是()
A. 电解水:2H20=2H2↑+O2↑ B. 4Fe(OH)2+O2+2H2O=4Fe(OH)3
C. 2F2+H2O=4HF+O2 D. 3NO2+H2O=2HNO3+NO
查看答案和解析>>
科目:高中化学 来源: 题型:
在容积相同的两密闭容器A和B中,保持温度为150℃,同时向A容器中加入a mol HI,向B容器中加入b mol HI (a>b),当反应2HI (g)⇌H2(g)+I2(g) 达到平衡后,下列说法正确的是()
A. 应开始达到平衡,所需时间tA>tB
B. 平衡时 C(I2)A=C(I2)B
C. 平衡时I2蒸气在混合气体中的体积分数:A>B
D. A与B中HI的平衡分解率相等.
查看答案和解析>>
科目:高中化学 来源: 题型:
三聚氰胺,分子式C3H6N6.有毒的三鹿牌奶粉就是因为其牛奶和奶粉中添加三聚氰胺,以提升食品检测中的蛋白质含量指标.下列关于三聚氰胺的说法中你认为正确的是( )
|
| A. | 三聚氰胺由多种分子组成,所以其属于混合物 |
|
| B. | 三聚氰胺的中碳、氢、氮三种元素的质量比为12:1:14 |
|
| C. | 每摩尔三聚氰胺分子中含有原子个数为15NA |
|
| D. | 三聚氰胺的摩尔质量为126 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com