
| A. | 是否是大量分子或离子的集合体 | B. | 是否均一、透明、稳定 | ||
| C. | 是否能透过滤纸或半透膜 | D. | 分散质微粒直径大小 |
科目:高中化学 来源: 题型:选择题
| A. | 都可以 | B. | 只有①不能发生 | C. | 只有②不能发生 | D. | 有②⑥不能发生 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 1molFeBr2与1molCl2反应时转移的电子数为3NA | |
| B. | 20g H218O与D216O的混合物中所含中子、电子数目均为10NA | |
| C. | 273K,101kPa下,1molCH3OCH3的体积约为22.4L | |
| D. | pH=1的H2SO4溶液中,含H+的数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
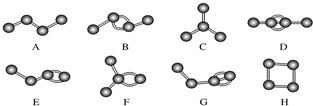
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 丙烷分子中三个碳原子共平面 | B. | 丁烷的一氯代物共有4种 | ||
| C. | 正丁烷的4个碳原子在一直线上 | D. | CnH2n+2的烃中含有3n+1个共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2gH2在标态下所占的体积为22.4L | |
| B. | 2.3gNa作还原剂时可失去0.1NA个电子 | |
| C. | 2molNaOH与NA个NA个H2SO4分子恰好中和 | |
| D. | 1molZn与足量的稀硫酸反应时共获得2gH2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com