
【题目】欲用含有少量氯化钙的氯化钠固体,配制100 mL a mol·L-1的氯化钠溶液,设计了下面的操作方案。根据方案操作步骤回答下列问题:

(1)称量粗盐样品m g,在托盘天平左盘上放________,右盘上放_______。
(2)蒸发操作时应将液体放在________中加热,等加热至________时即停止加热。
(3)在样品的溶液中加入过量的Na2CO3溶液,作用是_________________________________,
反应的化学方程式是______________________________________________________。
(4)在滤液中加入盐酸的作用是____________________________________,
反应的化学方程式是____________________________________________。
(5)配制100 mL a mol·L-1的NaCl溶液时,应从W g固体中称取NaCl的质量为________。
【答案】粗盐(放在称量纸上)砝码(放在称量纸上)蒸发皿出现大量晶体使钙离子完全形成沉淀而除去CaCl2+Na2CO3===CaCO3↓+2NaCl除去过量的Na2CO3Na2CO3+2HCl===2NaCl+H2O+CO2↑5.85a g
【解析】
(1)称量时左物右码;(2)蒸发在蒸发皿中进行,当加热到剩有少量液体时停止加热用余热蒸干;(3)Na2CO3是除杂试剂,加入过量的目的是把杂质除得更干净;(4)盐酸也是除杂试剂,用于除去所加的过量碳酸钠;(5)用W g NaCl配制100 mL a mol·L-1的NaCl溶液应称取NaCl的质量为100 mL×10-3 L·mL-1×a mol·L-1×58.5 g·mol-1=5.85a g.
(1)称量时左物右码,因此粗盐放在托盘天平的左盘,砝码放在托盘天平的右盘;(2)蒸发操作时应将液体放在蒸发皿中加热,等加热至出现大量晶体时即停止加热;(3)在样品的溶液中加入过量的Na2CO3溶液,作用是除掉钙离子,反应的化学方程式是CaCl2+Na2CO3═CaCO3↓+2NaCl;(4)在滤液中加入盐酸的作用是除掉过量的除杂试剂Na2CO3,反应的化学方程式是Na2CO3+2HCl═2NaCl+H2O+CO2↑;(5)配制100mL a mol·L-1的NaCl溶液时,n(NaCl)=0.1×a mol,m(NaCl)=0.1×a mol×58.5g·mol-1=5.85a g。.


科目:高中化学 来源: 题型:
【题目】下列有关化学用语的表示正确的是( )
A. 甲烷的球棍模型:![]() B. 氯离子的结构示意图:
B. 氯离子的结构示意图:![]()
C. 氮气的结构式:∶N≡N∶ D. 氯化氢的电子式:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是

A. X→Y反应类型为酯化反应
B. X、Y、Z均能使溴的四氯化碳溶液褪色
C. Y和Z互为同分异构体
D. 等物质的量的X、Z分别与足量Na反应,消耗Na的物质的量之比为2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于同分异构体的叙述正确的是
A. 相对分子质量相同而结构不同的化合物互称为同分异构体
B. 化学式相同而结构不同的化合物互称为同分异构体
C. 同分异构体之间由于分子组成相同,所以它们的性质相同
D. 只有少数的有机物之间存在同分异构现象
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.CH3COOH和CH3COOCH3互为同系物B.氧气和臭氧互为同位素
C.C5H12有四种同分异构体D.金刚石和石墨互为同素异形体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学学习小组在帮助老师整理实验室的化学试剂时,发现一盛无色盐溶液的试剂瓶,标签破损如右图,该小组根据已掌握的知识,对药品作出猜想,并设计实验验证。

(1)该实验药品为中学化学常用试剂,推测它的阳离子化合价为______________________。
(2)同学们做出以下三种推测。
猜想1:Na2SO4
实验设计: 进行……,.证明是Na2SO4溶液;
猜想2: K2SO4
实验设计:____________________________,证明是K2SO4溶液;
猜想3; (NH4)2SO4
实验设计:____________________________,证明是(NH4)2SO4溶液。
(3)通过实验发现“猜想3”成立,已知(NH4)2SO4受热易分解,该小组拟用下图所示装置探究其分解产物。(夹持和加热装置略)

实验I:装置B 盛0.5000mol/L盐酸50.00mL,通入N2排尽空气后,将装置A 加热至260℃一段时间,停止加热,停止通入N2,品红溶液不褪色,取下装置B,用0.1000mol/LNaOH溶液滴定剩余盐酸,消耗NaOH 溶液50.00mL。经检验滴定后的溶液中无SO42-。

①请从右图选择盛放0.1000mol/LNaOH 溶液的滴定管____________(填“甲”或“乙”)。
②装置B 内溶液吸收气体的物质的量是_____________________mol。
实验Ⅱ:通入N2排尽空气后,将装置A 加热到400℃,至固体无残留,停止加热,停止通入N2,观察到装置A、D之间的导气管内有少量白色固体。经检验,该白色固体和装置D内溶液中有SO32-,无SO42-。
①装置E 的作用是____________________________。
②A、D之间的导气管内的少量白色固体是____________________________。
③有同学提出在AD之间需要增加一个防倒吸的安全瓶,老师说不需要,原因是____________________________。
④进一步研究发现,气体产物中无氮氧化物,则(NH4)2SO4在400℃分解的化学方程式是_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温时,向20 mL 0.1 mol/L的醋酸溶液中不断滴入0.1 mol/L的NaOH溶液,溶液的pH变化曲线如图所示。在滴定过程中,关于溶液中离子浓度大小关系的描述正确的是
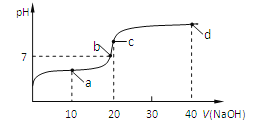
A.a点时:c(CH3COOH) c(CH3COO-) c(H+) c(Na+) c(OH-)
B.b点时:c(Na+)=c(CH3COO-)
C.c点时:c(H+)=c(CH3COOH)+c(OH-)
D.d点时:c(Na+) c(OH-) c(CH3COO-) c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com