
| A、营养补品吃得越多越好 |
| B、矿泉水中不含任何化学物质 |
| C、虽然药物能治病,但大部分药物都有不良反应 |
| D、食品添加剂的作用仅仅是为了好看 |


科目:高中化学 来源: 题型:
| A、44.8 g固体物质为Na2CO3 |
| B、44.8 g固体物质为NaOH和Na2O2混合物 |
| C、44.8 g固体物质为0.2 mol NaOH和0.4 mol Na2CO3混合物 |
| D、44.8 g固体物质为0.2 mol NaOH、0.2 mol Na2CO3、0.2 mol Na2O2混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用托盘天平称取3.23gNaCl固体 |
| B、用50mL量筒量取30.12mL水 |
| C、用酒精萃取碘水中的碘 |
| D、用淘洗的方法从沙里淘金 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 X、Y、Z、W有如图所示的转化关系,且△H=△H1+△H2,则X、Y可能是
X、Y、Z、W有如图所示的转化关系,且△H=△H1+△H2,则X、Y可能是| A、①②③④ | B、①③④⑤ |
| C、③④⑤ | D、①③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
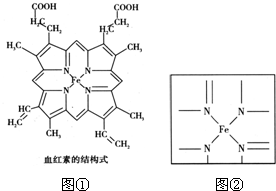

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子半径:R>T>Y>Z |
| B、电负性:W<R<T |
| C、最高价氧化物对应的水化物碱性:X<Z |
| D、XR2、WR2两化合物中R的化合价相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
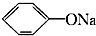 ④CH3COONH4 ⑤NH4HCO3
④CH3COONH4 ⑤NH4HCO3 >HCO3-.常温下,物质的量浓度相同的①、②、③溶液pH由大到小顺序为(填序号)
>HCO3-.常温下,物质的量浓度相同的①、②、③溶液pH由大到小顺序为(填序号)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com