
| A. | 温室效应--减少化石燃料使用,开发清洁能源 | |
| B. | 雾霾--适当限号,减少汽车尾气排放及扬尘 | |
| C. | 白色污染--杜绝生产塑料袋,从根源上治理 | |
| D. | 水体污染--节约用水,减少污水排放 |
分析 A、二氧化碳是造成温室效应的主要气体;
B、雾霾是悬浮在空气中烟、灰尘等物质;
C、根据白色污染是由于塑料制品的任意丢弃引起的考虑;
D、节约用水和合理施用农药、化肥,可以减少水体污染;
解答 解:A、二氧化碳是造成温室效应的主要气体,所以可以通过减少化石燃料使用,开发清洁能源,从而减少二氧化碳的排放,故A正确;
B、雾霾是悬浮在空气中烟、灰尘等物质,所以可以适当限号,减少汽车尾气排放及扬尘,故B正确;
C、白色污染是由于塑料制品的任意丢弃引起的,所以用布袋或纸袋代替塑料袋购物有利于减少白色污染,而不是杜绝生产塑料袋,故C错误;
D、节约用水和合理施用农药、化肥,可以减少水体污染,故D正确.
故选C.
点评 本题考查了常见的生活环境的污染和治理,运用化学知识解释生活现象,学以致用,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | H2=2H++2e- | B. | H2+2OH--2e-═2H2O | ||
| C. | O2+2H2O+4e-═4OH- | D. | 4H++O2═2H2O-4e- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 无色的溶液中:Fe3+、K+、ClO-、Cl- | |
| B. | pH=12的溶液中:NH4+、Na+、SO42-、Cl- | |
| C. | 含有大量Mg2+的溶液中:NH4+、Na+、SO42-、Cl- | |
| D. | c(H+)=0.1mol•L-1的溶液中:K+、I-、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钠不能用于治疗胃酸过多 | |
| B. | 二氧化硫可广泛应用于食品的漂白 | |
| C. | 水玻璃浸泡过的木材既能防腐又能耐火 | |
| D. | 氢氟酸(HF)可用于刻蚀玻璃 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
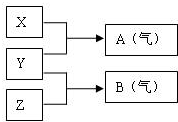 X、Y、Z为三种不同短周期非金属元素的单质.在一定条件下发生如下反应:请针对以下两种不同的情况回答:
X、Y、Z为三种不同短周期非金属元素的单质.在一定条件下发生如下反应:请针对以下两种不同的情况回答:查看答案和解析>>
科目:高中化学 来源: 题型:实验题
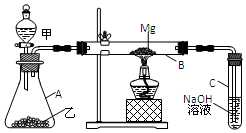 已知SiO2、SO2和CO2都是酸性氧化物,化学性质具有一定的相似性;Mg和Na的化学性质也具有一定的相似性.用如图所示装置进行Mg和SO2反应的实验.
已知SiO2、SO2和CO2都是酸性氧化物,化学性质具有一定的相似性;Mg和Na的化学性质也具有一定的相似性.用如图所示装置进行Mg和SO2反应的实验.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2气体中含有的少量杂质SO2可通过饱和Na2CO3溶液除去 | |
| B. | NaOH溶液中含有少量的Ba(OH)2可加入适量的Na2SO4过滤除去 | |
| C. | K2CO3固体中含有少量的NaHCO3杂质可用加热的方式提纯 | |
| D. | Cu粉中含有的少量杂质Fe可加入FeCl3溶液除去 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com