
甲醚作为一种基本化工原料,由于其良好的易压缩、冷凝、汽化特性,使得甲醚在制药、燃料、农药等化学工业中有许多独特的用途。
(1)已知:2CH3OH(g)CH3OCH3(g)+H2O(g) ΔH=-25 kJ·mol-1,某温度下的平衡常数为400。此温度下,在1 L的密闭容器中加入CH3OH,反应到某时刻测得各组分的物质的量浓度如下:
| 物质 | CH3OH | CH3OCH3 | H2O |
| c(mol·L-1) | 0.8 | 1.24 | ? |
①平衡时,c(CH3OCH3)等于________ mol·L-1,反应混合物的总能量减少________ kJ。
②若在平衡后的容器中再加入与起始时等量的CH3OH,请在下图中画出CH3OH的转化率和浓度的曲线示意图。

(2)在直接以甲醚为燃料的电池中,电解质溶液为酸性,负极的反应为________________、正极的反应为________________。
科目:高中化学 来源: 题型:
X、Y均为短周期元素,且X位于IA族,Y位于VIA族。下列说法中,正确的是
A.X、Y形成的离子化合物中只含有离子键 B.X、Y形成的化合物X2Y溶于水后溶液均呈碱性
C.同周期中X的原子半径大于Y的原子半径
D.1 mol 由X、Y组成的化合物所含有的电子总数均为18×6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
下列表述正确的是 ( )
A.0.1mol·L-1Na2CO3溶液中:=++
B.0.1mol·L-1CH3COONa溶液中:=+
C. CH3COONa、NaOH和Na2CO3三种溶液的pH相同,则浓度大小顺序:
c (NaOH) <c (Na2CO3) <c(CH3COONa)
D.向0.1mol·L-1CH3COOH溶液中滴加NaOH溶液至中性,溶液中离子浓度的关系:>>=
查看答案和解析>>
科目:高中化学 来源: 题型:
电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0 ~6.0之间,通过电解生成Fe(OH)3 沉淀。Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用。阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用。某科研小组用电浮选凝聚法处理污水,设计如图所示装置示意图。
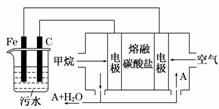
(1)实验时若污水中离子浓度较小,导电能力较差,产生气泡速率缓慢,无法使悬浮物形成浮渣。此时,应向污水中加入适量的________。
A.BaSO4 B.CH3CH2OH
C.Na2SO4 D.NaOH
(2)电解池阳极发生了两个电极反应,其中一个反应生成一种无色气体,则阳极的电极反应式分别是:
Ⅰ.______________;Ⅱ.______________。
(3)电极反应Ⅰ和Ⅱ的生成物反应得到Fe(OH)3沉淀的离子方程式是________________________________________________________________________。
(4)该燃料电池是以熔融碳酸盐为电解质,CH4为燃料,空气为氧化剂,稀土金属材料作电极。为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时必须有部分A物质参加循环(见上图)。A物质的化学式是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
甲醇脱氢可制取甲醛CH3OH(g)HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如图所示(已知反应在1 L的密闭容器中进行)。下列有关说法正确的是( )
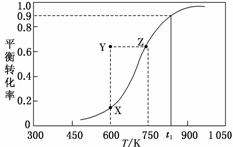
A.脱氢反应的ΔH<0
B.600 K时,Y点甲醇的v逆<v正
C.从Y点到Z点可通过增大压强
D.在t1 K时,该反应的平衡常数为8.1
查看答案和解析>>
科目:高中化学 来源: 题型:
已知FeCl3溶液与KSCN溶液混合后发生反应FeCl3+3KSCNFe(SCN)3+3KCl,达到平衡后,改变条件,则下列说法正确的是( )
A.向溶液中加入少许KCl固体,溶液颜色变浅
B.升高温度,平衡一定发生移动
C.加入少许KCl固体或者加入少许FeCl3固体平衡常数均发生变化,且变化方向相反
D.平衡常数表达式为K=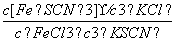
查看答案和解析>>
科目:高中化学 来源: 题型:
标准状况下有①6.72L甲烷②3.01×1023个氯化氢分子③13.6g硫化氢④0.2mol NH3.下列对这四种气体的关系从小到大表示不正确的是()
| A. | 体积:④<①<②<③ | B. | 密度:①<④<③<② | |
| C. | 质量:④<①<③<② | D. | 氢原子数:②<④<③<① |
查看答案和解析>>
科目:高中化学 来源: 题型:
表示溶液中浓度的方法通常有两种:溶液中溶质的质量分数(%)和物质的量浓度(C),因此在配制溶液时,根据不同的需要,有不同的配制方法,如:(请完成填空)
(1)用10%(密度为1.01g/cm3)的氢氧化钠溶液配制成27.5g2%的氢氧化钠溶液.
①计算:需5.5g10%(密度为1.01g/cm3)的氢氧化钠溶液,其体积为5.4mL,需加22mL水(ρ水=1g/cm3)进行稀释.
②量取:用10ml量筒取10%氢氧化钠,量取时视线要跟量筒凹液面的最低处保持水平,然后倒入烧杯里,用25ml量筒量取蒸馏水也注入烧杯里.
③溶解:用玻璃棒将上述溶液搅拌均匀,即得27.5g2%的氢氧化钠溶液.
(2)用98%(密度为1.84g/cm3)的浓硫酸稀释成3mol/L的稀硫酸100mL,回答下列问题:
①需要取浓硫酸16.3mL;
②配制操作可分解成如下几步,以下正确的操作顺序是ADECBHGF.
A、向容量瓶中注入少量蒸馏水,检查是否漏水
B、用少量蒸馏水洗涤烧杯及玻璃棒,将溶液注入容量瓶,并重复操作两次
C、用已冷却的稀硫酸注入已检查不漏水的容量瓶中
D、根据计算,用量筒量取一定体积的浓硫酸
E、将浓硫酸沿烧杯壁慢慢注入盛有蒸馏水的小烧杯中,并不断用玻璃棒搅拌
F、盖上容量瓶塞子,振荡,摇匀
G、用胶头滴管滴加蒸馏水,使溶液凹面恰好与刻度相切
H、继续往容量瓶中小心地加蒸馏水,使液面接近刻度线
(3)实验室需配制1mol•L﹣1的NaOH溶液和1mol•L﹣1的H2SO4溶液各100mL.
①要配制NaOH溶液,在用托盘天平称取NaOH固体时,天平读数为C.(填代号)
A.4.0g B.4.00g C.>4.0g
②在配制NaOH溶液和H2SO4溶液的各步操作中,有明显不同的是AB.
A.称量或量取 B.溶解 C.移液、洗涤 D.定容.
查看答案和解析>>
科目:高中化学 来源: 题型:
有A、B、C、D四块金属片,进行如下实验,①A、B用导线相连后,同时插入稀H2SO4中,A极为负极 ②C、D用导线相连后,同时浸入稀H2SO4中,电子由C→导线→D ③A、C相连后,同时浸入稀H2SO4,C极产生大量气泡 ④B、D相连后,同时浸入稀H2SO4中,D极发生氧化反应,则四种金属的活动性顺序为:
A.A>B>C>D B.C>A>B>D C.A>C>D>B D.B>D>C>A
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com