
【题目】回答下列问题
![]() 工业利用冶铜炉渣
工业利用冶铜炉渣![]() 含Fe2O3、FeO、SiO2、Al2O3等
含Fe2O3、FeO、SiO2、Al2O3等![]() 制Fe2O3的生产流程示意图如下:
制Fe2O3的生产流程示意图如下:
炉渣![]() 滤液
滤液![]() 沉淀
沉淀![]() 氧化铁
氧化铁
经“足量的NaOH溶液”处理后,铝元素的存在形态为 ______ ![]() 填序号
填序号![]() .
.
a.Al b.Al(OH)3 c.Al3+ d.AlO2-
![]() 要证明某溶液不含Fe3+但可能含有Fe2+,最佳的实验操作顺序是 ______
要证明某溶液不含Fe3+但可能含有Fe2+,最佳的实验操作顺序是 ______ ![]() 填序号
填序号![]() .
.
①加入少量氯水②加入足量KMnO4溶液③加入少量NH4SCN溶液
a. ①③ b.③② c. ③① d. ①②③
(3)25℃时,23gC2H5OH在血液中被氧气完全氧化放出668kJ热量,该反应的热化学方程式为 ______ .
(4)X、Y、Z、Q、R是原子序数依次增大的短周期主族元素,X、Q同主族,Z+与Y2-具有相同的电子层结构,Q 的单质是一种重要的半导体材料,R的单质在常温下呈气态.
①X、Y、Z三种元素的原子半径从大到小的顺序是 ______ ![]() 用元素符号表示
用元素符号表示![]() ,写出含有X、Y、Z三种元素且水溶液显碱性的物质化学式 ______ .
,写出含有X、Y、Z三种元素且水溶液显碱性的物质化学式 ______ .
![]() 下列选项一定能说明R的非金属性比X强的是 ______
下列选项一定能说明R的非金属性比X强的是 ______ ![]() 填序号
填序号![]() .
.
a.原子的半径:r(R)>r(X)
b.原子的最外层电子数:n(R)>n(X)
c.热稳定性:R的气态氢化物>X的气态氢化物
d.酸性:R的最高价氧化物对应的水化物>X的最高价氧化物对应的水化物
③R在周期表的位置是 ______ R和Q形成的化合物在潮湿的空气中冒白色烟雾,该反应的化学方程式为 ______ .
【答案】d c C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l)![]() H=-1336kJ/mol Na>C>O Na2CO3或CH3COONa cd 第三周期ⅦA族 SiCl4+3H2O=H2SiO3+4HCl↑
H=-1336kJ/mol Na>C>O Na2CO3或CH3COONa cd 第三周期ⅦA族 SiCl4+3H2O=H2SiO3+4HCl↑
【解析】
(1)炉渣被盐酸处理后,滤液中Al以Al3+形式存在,向滤液中加入足量的氢氧化钠,反应生成AlO2-;
(2)少量NH4SCN溶液不变红色,说明不含Fe3+,再滴加氯水,溶液变为红色,说明含有Fe2+;
(3)计算1mol乙醇完全燃烧放出的热量,注明物质的聚集状态、反应热,据此书写热化学方程式;
![]() 、Y、Z、Q、R是原子序数依次增大的短周期主族元素,Q的单质是一种重要的半导体材料,则Q为Si;X、Q同主族,则X为C元素;Z+与Y2-具有相同的电子层结构,Z处于短周期、Y处于第二周期,则Z为Na、Y为O,R的单质在常温下呈气态,原子序数大于Si,则R为Cl。
、Y、Z、Q、R是原子序数依次增大的短周期主族元素,Q的单质是一种重要的半导体材料,则Q为Si;X、Q同主族,则X为C元素;Z+与Y2-具有相同的电子层结构,Z处于短周期、Y处于第二周期,则Z为Na、Y为O,R的单质在常温下呈气态,原子序数大于Si,则R为Cl。
(1)炉渣被盐酸处理后,滤液中Al以Al3+形式存在,向滤液中加入足量的氢氧化钠,反应生成AlO2-;
(2)少量NH4SCN溶液不变红色,说明不含Fe3+,再滴加氯水,溶液变为红色,说明含有Fe2+;
(3)1mol乙醇完全燃烧放出的热量=668kJ![]() =1336kJ,故热化学方程式为:C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l)
=1336kJ,故热化学方程式为:C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l)![]() H=-1336kJ/mol;
H=-1336kJ/mol;
(4)X、Y、Z、Q、R是原子序数依次增大的短周期主族元素,Q的单质是一种重要的半导体材料,则Q为Si;X、Q同主族,则X为C元素;Z+与Y2-具有相同的电子层结构,Z处于短周期、Y处于第二周期,则Z为Na、Y为O,R的单质在常温下呈气态,原子序数大于Si,则R为Cl,则:
①同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径Na>C>O,含Na、C、O三种元素且水溶液显碱性的物质为Na2CO3或CH3COONa等;
②a.![]() 、Cl不同周期,原子半径小不能说明非金属性更强,Cl元素非金属性较强,a错误;
、Cl不同周期,原子半径小不能说明非金属性更强,Cl元素非金属性较强,a错误;
b.C、Cl不同周期,原子的最外层电子数不能说明非金属性强弱,b错误;
![]() 热稳定性:R的气态氢化物>X的气态氢化物,说明非金属性R更强,c正确;
热稳定性:R的气态氢化物>X的气态氢化物,说明非金属性R更强,c正确;
![]() 元素最高价含氧酸的酸性越强,元素的非金属性越强,d正确,
元素最高价含氧酸的酸性越强,元素的非金属性越强,d正确,
答案为cd;
③R为Cl元素,处于周期表中第三周期ⅦA族,Cl和Si形成的化合物为SiCl4,在潮湿的空气中冒白色烟雾,水解生成硅酸与HCl,该反应的化学方程式为:SiCl4+3H2O=H2SiO3+4HCl↑。


科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示。下列说法正确的是
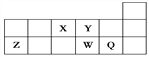
A. 原子半径的大小顺序为:rX>rY>rZ>rW>rQ
B. 元素W的最高价氧化物对应的水化物酸性比Q的强
C. 元素X与元素Z的最高正化合价之和的数值等于8
D. 离子Y2-和Z3+的核外电子数和电子层数都不相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)基态碳原子的核外电子排布式为______。
(2)基态铬原子外围电子轨道表示式为___。
(3)卤族元素F、Cl的电负性由小到大的顺序是______。
(4)比较晶格能:MgO___MgS(用“>”、“<”)
(5)CO分子内σ键与π键个数之比为________。
(6)比较第一电离能:Mg___Al(用“>”、“<”)
(7)乙炔是________(填“非极性”或“极性”)分子。
(8)丙烯(CH3CH=CH2)分子中碳原子的杂化方式为________和________。
(9)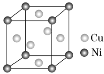 某镍白铜合金的立方晶胞结构如图所示。晶胞中铜原子与镍原子的数量比为________。
某镍白铜合金的立方晶胞结构如图所示。晶胞中铜原子与镍原子的数量比为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式中,正确的是
A.碳酸氢铵溶液中加入足量的浓氢氧化钠溶液并加热:NH![]() +OH-
+OH-![]() NH3↑+H2O
NH3↑+H2O
B.铜与稀硝酸的反应:Cu+4H++2NO![]() =Cu2++2NO2↑+2H2O
=Cu2++2NO2↑+2H2O
C.向Ba(OH)2溶液中滴加稀硫酸:Ba2++OH-+H++SO![]() =BaSO4↓+H2O
=BaSO4↓+H2O
D.过量二氧化硫与氢氧化钠溶液反应:SO2+OH-=HSO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在2 L密闭容器中充入4 mol A气体和3 mol B气体,发生下列反应:2A(g)+B(g)![]() C(g)+xD(g),5 s达到平衡。达到平衡时,生成了1 mol C,测定D的浓度为1 mol·L-1。
C(g)+xD(g),5 s达到平衡。达到平衡时,生成了1 mol C,测定D的浓度为1 mol·L-1。
(1)求x=_____。
(2)求这段时间A的平均反应速率为_____。
(3)平衡时A的转化率为_____。
(4)下列叙述能说明上述反应达到平衡状态的是_____
A. 单位时间内每消耗2 mol A,同时生成1 mol C
B. 单位时间内每生成1 molB,同时生成1 molC
C. D的体积分数不再变化
D. 混合气体的压强不再变化
E. B、C 的浓度之比为1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有5种元素X、Y、Z、Q、T。X原子最外层M层上有2个未成对电子且无空轨道;Y原子的价电子构型为3d64s2;Z原子的L电子层的p能级上有一个空轨道;Q原子的L电子层的p能级上只有一对成对电子;T原子的M电子层上p轨道半充满。下列叙述不正确的是( )
A.元素Y和Q可形成化合物Y2O3
B.T的一种单质的空间构型为正四面体形,键角为![]()
C.X和Q结合生成的化合物为共价化合物
D.ZO2是极性键构成的非极性分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂离子电池应用很广。某种锂离子二次电池的电极材料主要是钴酸锂(LiCoO2)和石墨。钴是一种稀有的贵重金属,废旧锂离子电池电极材料的回收再生意义重大。
(1)锂离子电池(又称锂离子浓差电池)的充电过程:Li+从含LiCoO2的电极中脱出,正三价Co被氧化,此时该极处于贫锂态(Li1-xCoO2)。
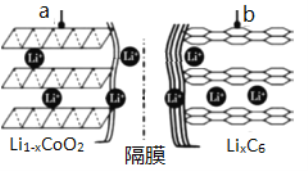
①充电时,a极的电极反应式为____________________________________。
②放电时,电流从______(填“a”或“b”)极流出。
(2)钴酸锂回收再生流程如下:
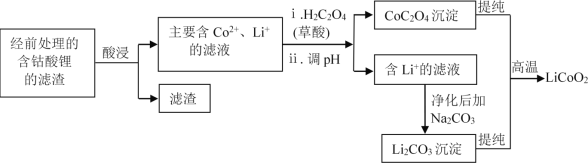
①H2SO4酸浸时,通常添加30%的H2O2以提高浸出效率,其中H2O2的作用是_______________。
②用盐酸代替H2SO4和H2O2,浸出效率也很高,但工业上不使用盐酸,主要原因之一是:会产生有毒、有污染的气体。写出相应反应的化学方程式______________________________。
③高温下,在O2存在时纯净的CoC2O4与Li2CO3再生为LiCoO2的化学方程式为_______________。
(3)已知下列热化学方程式:
Fe2O3(s)+3CO(g)===2Fe(s)+3CO2(g) ΔH1=-25 kJ·mol-1
3Fe2O3(s)+CO(g)===2Fe3O4(s)+CO2(g) ΔH2=-47 kJ·mol-1
Fe3O4(s)+CO(g)===3FeO(s)+CO2(g) ΔH3=+19 kJ·mol-1
写出FeO(s)被CO还原成Fe和CO2的热化学方程式_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】RbH是一种离子化合物,它跟水反应的方程式为:![]() ,它也能跟液氨、乙醇等发生类似的反应,并都产生氢气,下列有关RbH的叙述错误的是
,它也能跟液氨、乙醇等发生类似的反应,并都产生氢气,下列有关RbH的叙述错误的是![]()
A.灼烧RbH时,火焰有特殊颜色
B.RbH中![]() 半径比
半径比![]() 半径小
半径小
C.跟液氨反应时,有![]() 生成
生成
D.在Na、K、Rb三种单质中,Rb的熔点最低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某厂利用一种天然产物进行发酵,发现发酵液中含有U、V、W、X等多种化合物。已知:①U和W均可与银氨溶液反应,析出金属银,而且U是一种单糖。②V是单官能团化合物,其碳原子数和X相同。V在浓硫酸作用下经加热得到Y,Y可以使溴水褪色。③V经缓和氧化可生成W。④V和X在少量浓硫酸作用下经加热可以得到Z。⑤X的组成为C 40%、H 6.7%、O 53.3%,X含有一个羧基,已知X的相对分子质量为90。X也可与乙酸起酯化反应。根据上述条件,回答下列问题:
(1)写出符合U的一种可能的单糖结构简式:___________。
(2)X的分子式是_____,其所有可能的结构简式是_________。
(3)V、W、Y、Z的可能的结构简式分别是:V_____,W_____,Y_______,Z______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com