
【题目】某兴趣小组同学欲研究SO2的相关性质。
(1)比较下表中的两组物质关系,第2组中物质X的化学式是 。
第1组 | 第2组 |
C、CO、CO2、H2CO3、Na2CO3、、NaHCO3、 | S 、SO2、SO3、X、Na2SO4、NaHSO4 |
(2)利用下图装置来检验SO2的性质
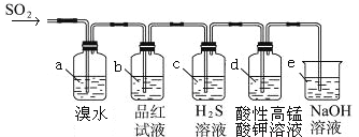
①装置a中的现象是: ; (填“能”或“不能”)说明 SO2 有漂白性
②若装置e中有40 mL 2.5 molL-1 NaOH溶液,反应后增重4.8 g,则装置IV中发生反应的总化学方程式是 。
(3)该小组的甲、乙两位同学利用下图装置继续探究SO2及氯气漂白性:
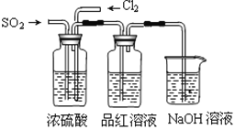
通气一段时间后,甲同学实验过程中品红溶液几乎不褪色,而乙同学的实验现象是品红溶液随时间的推移变得越来越浅。试根据该实验装置和两名同学的实验结果回答问题。
①试分析甲同学实验过程中,用离子方程式表示品红溶液不褪色的原因是: 。
②你认为乙同学是怎样做到让品红溶液变得越来越浅的?
。
【答案】(1)H2SO4;(2)①溴水褪色,不能;
②3SO2+4NaOH==Na2SO3+2NaHSO3+H2O;
(3)①SO2+Cl2+2H2O=SO42-+2Cl—+4H+;
②控制SO2和Cl2进气的物质的量,使之不相等。
【解析】
试题分析:(1)根据第1组,从左向右第四种物质为最高价氧化物的含氧酸,因此X为H2SO4;(2)①SO2具有还原性,Br2具有强氧化性,两者发生SO2+Br2+2H2O=2HBr+H2SO4,现象是溴水褪色,不能说明SO2具有漂白性;②假设全部生成Na2SO3,质量增重40×10-3×2.5×64/2g=3.2g<4.8g,假设全部生成NaHSO3,质量增重40×10-3×2.5×64g=6.4g>4.8g,假设生成Na2SO3物质的量为xmol,NaHSO3物质的量ymol,根据钠元素守恒,推出2x+y=40×10-3×2.5mol,(x+y)×64=4.8,两式联立解得,x=0.025,y=0.05,因此反应方程式为3SO2+4NaOH=Na2SO3+2NaHSO3+H2O;(3)①利用氯气的氧化性,把SO2氧化,发生的离子反应是SO2+Cl2+2H2O=SO42-+2Cl-+4H+;②控制SO2和Cl2进气的物质的量,使之不相等。


 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:高中化学 来源: 题型:
【题目】实验是进行化学研究的重要环节,下列有关化学实验的说法正确的是( )
A. 向滴有KSCN的FeCl3溶液中加入NaOH溶液以研究反应物浓度对化学平衡的影响
B. 用酒精萃取碘水中的碘,水从分液漏斗下口放出,碘的酒精溶液从分液漏斗上口倒出
C. 将高锰酸钾溶液装入碱式滴定管中进行滴定实验,以测定某FeSO4样品的纯度
D. 为制备硅酸胶体,以酚酞为指示剂,将浓盐酸滴入饱和Na2SiO3溶液中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一定量的NaOH溶液中逐滴加入AlCl3溶液,生成沉淀Al(OH)3的量随AlCl3加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是( )
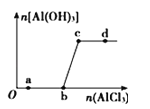
A.a点对应的溶液中:Na+、Fe3+、SO42﹣、HCO3﹣
B.b点对应的溶液中:Na+、S2﹣、SO42﹣、Cl﹣
C.c点对应的溶液中:Ag+、Ca2+、NO3﹣、Na+
D.d点对应的溶液中:K+、NH4+、I﹣、HCO3﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图甲是CO2电催化还原为碳氢化合物(CxHy)的工作原理示意图,用某钾盐水溶液做电解液;图乙 是用H2还原CO2制备甲醇的工作原理示意图,用硫酸为电解质溶液。下列说法中不正确的是( )
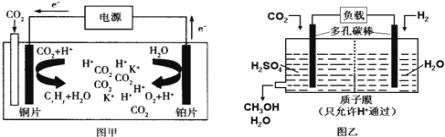
A.甲中铜片作阴极,K+向铜片电极移动
B.甲中若CxHy为C2H4,则生成1mol C2H4的同时生成3mol O2
C.乙中H2SO4的作用是增强溶液的导电性
D.乙中正极发生的电极反应为CO2+5e-+6H+═CH3OH+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列对于溶液问题的叙述正确的是( )
A.pH=4的氯化铵溶液,用蒸馏水稀释10倍后,溶液的pH小于5
B.pH=3的盐酸与pH=3的CH3COOH溶液相比,c(Cl﹣)>C(CH3COO﹣)
C.pH=2的一元酸HA溶液与pH=12的NaOH溶液以体积比1:1混合后,c(Na+)一定小于c(A﹣)
D.pH相同的NaOH、NaClO两种溶液中水的电离程度相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列仪器:①集气瓶;②量筒;③烧杯;④表面皿;⑤蒸发皿;⑥容量瓶;⑦圆底烧瓶。其中能用酒精灯加热的是( )
A. ①③④ B. ②③⑤ C. ③⑤⑦ D. ③⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于原电池的叙述中正确的是( )
A.原电池是将化学能直接转变为电能的装置
B.原电池负极发生的电极反应是还原反应
C.原电池在工作时其正极不断产生电子并经外电路流向负极
D.原电池的电极只能由两种不同的金属构成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把NaOH和Na2CO3混和物配制成100mL溶液,其中c(Na+)=0.5mol/L。在该溶液中加入过量盐酸反应完全后,将溶液蒸干后所得固体质量约为
A、2.93 g B、5.85 g C、6.56g D、无法确定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com