
温时,M(OH)2(s)⇌M2+(aq)+2OH﹣(aq)Ksp=a,c(M2+)=b mol•L﹣1时,溶液的pH等于( )
|
| A. |
| B. |
| C. | 14+ | D. | 14+ |
考点:
难溶电解质的溶解平衡及沉淀转化的本质;pH的简单计算.
专题:
电离平衡与溶液的pH专题.
分析:
依据Ksp=c(M2+)c2(OH﹣)表达式和题干Ksp=a,C(M2+)=b mol•L﹣1,计算溶液中氢氧根离子浓度,结合溶液中离子积计算氢离子浓度和溶液pH;
解答:
解:室温时,M(OH)2(s)⇌M2+(aq)+2OH﹣(aq),已知Ksp=a,c(M2+)=b mol•L﹣1,则c(OH﹣)= =
= mol•L﹣1,
mol•L﹣1,
所以c(H+)= =
=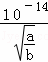 mol•L﹣1,则pH=﹣lgc(H+)=14+
mol•L﹣1,则pH=﹣lgc(H+)=14+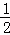 lg(
lg(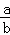 );
);
故选C.
点评:
本题考查了溶度积常数的有关计算和PH的计算,题目难度不大,注意对Ksp含义的理解.


 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案科目:高中化学 来源: 题型:
下列实验“操作和现象”与“结论”对应关系正确的是( )
| 操作和现象 | 结论 | |
| A | 向装有Fe(NO3)2溶液的试管中加入稀H2SO4,在管口观察到红棕色气体 | HNO3分解成了NO2 |
| B | 向淀粉溶液中加入稀H2SO4,加热几分钟,冷却后再加入新制Cu(OH)2浊液,加热,没有红色沉淀生成 | 淀粉没有水解成葡萄糖 |
| C | 向无水乙醇中加入浓H2SO4,加热至170℃,产生的气体通入酸性KMnO4溶液,紫红色褪去 | 使溶液褪色的气体是乙烯 |
| D | 向饱和Na2CO3溶液中通入足量CO2,溶液变浑浊 | 析出了NaHCO3 |
|
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:
中学阶级介绍的电解原理的应用主要有三种:一是氯碱工业、二是电解精炼铜、三是电解冶金。下列关于这三个工业生产的描述中正确的是
A.电解精炼铜时,负极反应式:Cu2++2e-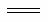 Cu
Cu
B.氯碱工业和电解精炼铜中,阳极都是氯离子放电放出氯气
C.在氯碱工业中,电解池中的阴极产生的是H2, NaOH在阳极附近产生
D.电解精炼铜时,应用粗铜作阳极、精铜作阴极,可溶性铜盐作电解质溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
有机物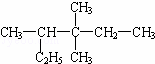 的正确命名是( )
的正确命名是( )
|
| A. | 3,3﹣二甲基﹣4﹣乙基戊烷 | B. | 3,3,4﹣三甲基己烷 |
|
| C. | 3,4,4﹣三甲基己烷 | D. | 2,3,3﹣三甲基己烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:
120℃时,1体积某烃和4体积O2混和,完全燃烧后恢复到原来的温度和压强,体积不变,该烃分子式中所含的碳原子数不可能是( )
|
| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品中;NH4HSO4在分析试剂、医药、电子工业中用途广泛.请回答下列问题:
(1)NH4Al(SO4)2可作净水剂,其理由是
(用必要的化学用语和相关文字说明).
(2)相同条件下,0.1mol•L﹣1 NH4Al(SO4)2中c(NH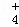 ) (填“等于”“大于”或“小于”)0.1mol•L﹣1 NH4HSO4中c(NH
) (填“等于”“大于”或“小于”)0.1mol•L﹣1 NH4HSO4中c(NH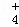 ).
).
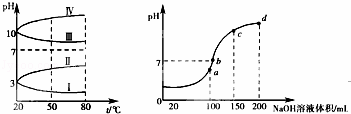
(3)如图1所示是0.1mol•L﹣1电解质溶液的pH随温度变化的图象.
①其中符合0.1mol•L﹣1 NH4Al(SO4)2的pH随温度变化的曲线是 (填写序号),导致pH随温度变化的原因是 ;
②20℃时,0.1mol•L﹣1 NH4Al(SO4)2中2c(SO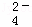 )﹣c(NH
)﹣c(NH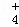 )﹣3c(Al3+)= (填数值).
)﹣3c(Al3+)= (填数值).
(4)室温时,向100mL 0.1mol•L﹣1 NH4HSO4溶液中滴加0.1mol•L﹣1 NaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图2所示:试分析图中a、b、c、d四个点,水的电离程度最大是 点;在b点,溶液中各离子浓度由大到小的排列顺序是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法或表示方法正确的是( )
|
| A. | 等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 |
|
| B. | 由C(石墨)→C(金刚石);△H=+1.9 kJ/mol可知,金刚石比石墨稳定 |
|
| C. | 在稀溶液中:H+(aq)+OH﹣(aq)═H2O(l);△H=﹣57.3 kJ/mol,若将含0.5mol H2SO4的浓硫酸与含1mol NaOH的稀溶液混合,放出的热量大于57.3 kJ |
|
| D. | 在101kPa、25℃时,2g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)═2H2O(l);△H=﹣285.8 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
请按要求填空
(1)下列实验操作或对实验事实的描述不正确的是 (填序号)
①用热的浓HCl洗涤附着有MnO2的试管;
②浓硫酸不小心沾在皮肤上,先用抹布擦干净,再用大量的水冲洗;
③测定硫酸铜晶体中结晶水含量的实验中,至少需经过4次称量;④蒸馏石油时,冷凝管中的冷水应上进下出;
⑤向蛋白质溶液中加入浓的无机盐(如Na2SO4、CuSO4)溶液,可使蛋白质盐析而分离提纯;
⑥配制一定浓度的溶液时,若定容时不小心加水超过容量瓶的刻度线,应立即用滴管吸去多余的部分.
(2)实验室利用如图装置进行中和热的测定.
回答下列问题:
①该图中有两处未画出,它们是 、 ;
②在操作正确的前提下提高中和热测定的准确性的关键是 ;
③如果用0.5 mol/L的盐酸和氢氧化钠固体进行实验,则实验中所测出的“中和热”将 (填“偏大”、“偏小”、“不变”);原因是 .
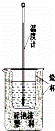
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述Ⅰ和Ⅱ均正确并且有因果关系的是( )
选项 叙述Ⅰ 叙述Ⅱ
A NH4Cl为强酸弱碱盐 用加热法除去NaCl中的NH4Cl
B Fe3+具有氧化性 用KSCN溶液可以鉴别Fe3+
C 溶解度:CaCO3<Ca(HCO3)2 溶解度:Na2CO3<NaHCO3
D SiO2可与HF反应 氢氟酸不能保存在玻璃瓶中
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com