
 ;不溶性的固体与溶液的分离为过滤,故答案为:
;不溶性的固体与溶液的分离为过滤,故答案为: ; 过滤;
; 过滤;

科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaHCO3═Na++H++CO32- |
| B、NaHSO4═Na++H++SO42- |
| C、H2SO4═2H++SO4- |
| D、KClO3═K++Cl-+3O2- |
查看答案和解析>>
科目:高中化学 来源: 题型:
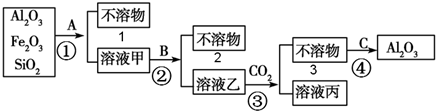
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、AlCl3溶液中加入过量的氨水 |
| B、MgCl2溶液中加入过量的氨水 |
| C、Al2(SO4)3溶液中加入过量的KOH溶液 |
| D、MgSO4溶液中加入过量的KOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、刚充入时反应速率v(正)增大,v(逆)增大 |
| B、达到新的平衡时,反应混合物中A、B的体积分数减小 |
| C、充入A、B、Q后,体系压强先增大,后逐渐减小 |
| D、若B为有色物质,达到新平衡后混合气颜色比原平衡浅 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、I-、ClO-、H+、Na+ |
| B、K+、HCO3-、OH-、NH4+ |
| C、Fe3+、Cu2+、SO42-、Cl- |
| D、Ca2+、Na+、SO42-、SO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 溶解 |
| ① |
| BaCl2 |
| ② |
| NaOH |
| ③ |
| Na2CO3 |
| ④ |
| 过滤 |
| ⑤ |
| 适量盐酸 |
| ⑥ |
| 蒸发、结晶、烘干 |
| ⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:
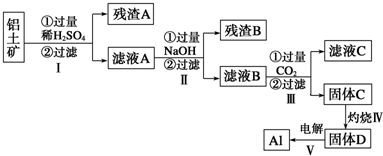
- 2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com