
【题目】水中溶氧量(DO)是衡量水体自净能力的一个指标,通常用每升水中溶解氧分子的质量表示,单位mg·L-1。我国《地表水环境质量标准》规定,生活饮用水源的DO不能低于5 mg·L-1。水中溶解氧的测定步骤如下:
(1)向一定量水样中加入适量MnSO4和碱性KI溶液,生成MnO(OH)2沉淀,密封静置;
(2)加入适量稀H2SO4,搅拌,等MnO(OH)2与I-完全反应生成Mn2+和I2后;
(3)用Na2S2O3标准溶液滴定至终点。
测定过程中物质的转化关系如下:
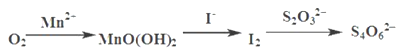
已知:MnO(OH)2+2I-+4H+ =Mn2++I2+3H2O 2S2O32- +I2= S4O62-+2I-
①加入稀硫酸后搅拌的作用是__________;Na2S2O3标准溶液应装在______________滴定管中(填酸式或碱式)。
②滴定过程中以_____________为指示剂;达到滴定终点的标志为____________________。
③写出O2将Mn2+氧化成MnO(OH)2的离子方程式____________________;
④若加入的稀H2SO4溶液反应后,若溶液pH过低,滴定时会产生明显的误差。写出产生误差的一个原因(用离子方程式表示)__________________。
⑤下列操作使测得水样中溶氧量(DO)比实际值偏高的是__________________。
A.第(1)步操作静置时没有密封 B.装Na2S2O3标准溶液的滴定管没有润洗
C.滴定前锥形瓶洗净后没有干燥 D.滴定前读数正确,滴定后俯视读数
⑥取加过一定量CaO2·8H2O的池塘水样l00.00mL,按上述方法测定水中溶解氧量,消耗0.01000
mol·L-1 Na2S2O3标准溶液13.50 mL。计算该水样中的溶解氧为____________mg·L-1。
【答案】 使溶液混合均匀,加快反应速率 碱式 淀粉溶液 当滴入最后一滴标准液时,溶液蓝色褪去且半分钟内不变色 2Mn2++O2+4OH-=2MnO(OH)2↓ S2O32-+2H+= S↓+ SO2↑+H2O或 SO2+I2+2H2O=4H++SO42-+2I- 或4 I-+4 H++O2=2I2+2H2O AB 10.80
【解析】试题分析:本题考查酸碱中和滴定的拓展实验——氧化还原滴定,考查滴定管和指示剂的选择、滴定终点的判断,误差分析和计算。
①加入稀硫酸后搅拌的作用是:使溶液混合均匀,加快反应速率。Na2S2O3溶液呈碱性,且Na2S2O3具有强还原性,所以Na2S2O3溶液应盛装在碱式滴定管中。
②该实验以标准Na2S2O3溶液滴定I2,所以选用淀粉溶液作指示剂。滴定终点的标志是:滴入最后一滴标准Na2S2O3溶液,溶液由蓝色褪为无色且在半分钟内不恢复。
③依据O2将Mn2+氧化成MnO(OH)2写出:O2+Mn2+→MnO(OH)2↓,根据得失电子守恒配平:O2+2Mn2+→2MnO(OH)2↓,结合原子守恒、电荷守恒和溶液呈碱性,写出离子方程式为:2Mn2++O2+4OH-=2MnO(OH)2↓。
④若溶液pH过低,Na2S2O3会与H+反应,消耗Na2S2O3增多,引起误差,反应的离子方程式为:S2O32-+2H+= S↓+ SO2↑+H2O,生成的SO2会与I2反应:SO2+I2+2H2O=4H++SO42-+2I-;溶液中KI在酸性条件下会被空气中O2氧化成I2,消耗Na2S2O3增多,引起误差,KI被O2氧化的离子方程式为:4 I-+4 H++O2=2I2+2H2O。
⑤根据方程式:2Mn2++O2+4OH-=2MnO(OH)2↓、MnO(OH)2+2I-+4H+ =Mn2++I2+3H2O、2S2O32- +I2= S4O62-+2I-,得出关系式O2~4Na2S2O3,则n(O2)=![]() n(Na2S2O3)=
n(Na2S2O3)=![]() c(Na2S2O3)V[Na2S2O3(aq)]。A项,第(1)步操作静置时没有密封,空气中的O2进入参与反应,使所耗Na2S2O3标准溶液体积偏大,测得水样中溶氧量比实际值偏高;B项,装Na2S2O3标准溶液的滴定管没有润洗,Na2S2O3被稀释,使所耗Na2S2O3标准溶液体积偏大,测得水样中溶氧量比实际值偏高;C项,滴定前锥形瓶洗净后没有干燥,对测定结果无影响;D项,滴定前读数正确,滴定后俯视读数,所耗Na2S2O3标准溶液体积偏小,测得水样中溶氧量比实际值偏低;答案选AB。
c(Na2S2O3)V[Na2S2O3(aq)]。A项,第(1)步操作静置时没有密封,空气中的O2进入参与反应,使所耗Na2S2O3标准溶液体积偏大,测得水样中溶氧量比实际值偏高;B项,装Na2S2O3标准溶液的滴定管没有润洗,Na2S2O3被稀释,使所耗Na2S2O3标准溶液体积偏大,测得水样中溶氧量比实际值偏高;C项,滴定前锥形瓶洗净后没有干燥,对测定结果无影响;D项,滴定前读数正确,滴定后俯视读数,所耗Na2S2O3标准溶液体积偏小,测得水样中溶氧量比实际值偏低;答案选AB。
⑥根据关系式O2~4Na2S2O3,得出n(O2)=![]() n(Na2S2O3)=
n(Na2S2O3)=![]() c(Na2S2O3)V[Na2S2O3(aq)]=
c(Na2S2O3)V[Na2S2O3(aq)]= ![]() 0.01000mol/L
0.01000mol/L![]() 0.0135L=3.375
0.0135L=3.375![]() 10-5mol,m(O2)=3.375
10-5mol,m(O2)=3.375![]() 10-5mol
10-5mol![]() 32g/mol=1.08
32g/mol=1.08![]() 10-3g=1.08mg,该水样中的溶解氧为
10-3g=1.08mg,该水样中的溶解氧为![]() =10.80mg/L。
=10.80mg/L。


科目:高中化学 来源: 题型:
【题目】采用如下装置(夹持和加热仪器已略去)电解饱和食盐水,并检验氯气的氧化性,同时用电解产生的H2还原CuO粉末来测定Cu的相对原子质量。

(1)写出电解饱和食盐水的离子方程式_________________________________。
(2)为完成上述实验,正确的连接顺序为A连_______;B连_______ (填写导管口字母)。
(3)若检验氯气的氧化性,则乙装置的a瓶中溶液可以是下列试剂中的___________。
a.酸性高锰酸钾溶液 b.淀粉碘化钾溶液 c.亚硫酸钠溶液 d.氯化亚铁溶液
(4)丙装置的c瓶中盛放的试剂为___________,作用是______________________。
(5)为测定Cu的相对原子质量,设计了如下甲、乙两个实验方案:
精确测量硬质玻璃管的质量为a g,放入CuO后,精确测量硬质玻璃管和CuO的总质量为b g(假设CuO充分反应),实验完毕后:
甲方案:通过精确测量硬质玻璃管和Cu粉的总质量为c g,进而确定Cu的相对原子质量。
乙方案:通过精确测定U型管b反应前后的质量变化,得到生成水的质量d g,进而确定Cu的相对原子质量。
①请你分析并回答:___________方案所测结果更准确。若按合理方案测定的数据计算,Cu的相对原子质量为________________。
②不合理的方案会造成测定结果___________(填“偏低、偏高或无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学研究性学习小组设计实验探究铜的常见化学性质,过程设计如下:提出猜想
问题1:在周期表中,铜与铝的位置很接近,铜不如铝活泼,氢氧化铝具有两性,氢氧化铜也有两性吗?
问题2:铁和铜都有变价,一般情况下,正二价铁的稳定性小于正三价的铁,正一价铜的稳定性也小于正二价的铜吗?
问题3:氧化铜有氧化性,能被H2、CO还原,它也能被氮的某种气态氢化物还原吗?
实验探究
(1)I.解决问题1
a.需用到的药品除1molL﹣1CuSO4溶液、稀硫酸外还需________(填试剂的化学式)溶液.
b.用胆矾晶体配制1molL﹣1CuSO4溶液250mL,选用的仪器除烧杯、托盘天平、药匙、
玻璃棒、胶头滴管外,还有________(填仪器名称).
c.为达到实验目的,请你补全实验内容和步骤:
①用CuSO4溶液制备Cu(OH)2;
②________.
(2)Ⅱ.解决问题2
取一定量I中制备获得的氢氧化铜固体于坩埚中灼烧,当温度达到80~100℃得到黑色固体粉末;继续加热至1000℃以上,黑色粉末全部变成红色粉末氧化亚铜;取适量红色氧化亚铜粉末于洁净试管中,加入过量的稀硫酸(或盐酸),得到蓝色溶液,同时观察到试管底部还有红色固体存在.根据以上实验现象回答问题.
a.写出氧化亚铜与稀硫酸(或盐酸)反应的离子方程式:________.
b.从实验Ⅱ可得出的结论是在高温下正一价铜比正二价铜________(填稳定或不稳定),溶液中正一价铜比正二价铜________(填稳定或不稳定).
(3)Ⅲ.解决问题3设计如下装置(夹持装置未画出):

当氮的某种气态氢化物(X)缓缓通过灼热的氧化铜时,观察到氧化铜由黑色变成了红色,无水硫酸铜变成蓝色,生成物中还有一种无污染的单质气体Y;将X通人灼热的CuO燃烧管完全反应后,消耗0.01mol X,测得B装置增重0.36g,并收集到0.28g气体Y.
a.仪器A的名称是________.
b.X的化学式为________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有1.16g白色沉淀,在所得的悬浊液中逐滴加入1mol/LHCl溶液,加入HCl溶液的体积V与生成沉淀的质量m的关系如下图所示.试回答: 
(1)A点的沉淀物的化学式为 , B点的沉淀物的化学式为 .
(2)原混合物中MgCl2的质量是g,AlCl3的质量是g,NaOH的质量是g.
(3)Q点HCl溶液加入量是mL.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家研制的一种使沙漠变绿洲的新技术,即在沙漠中喷洒一定量的聚丙烯酸酯与水的混合物,使其与沙粒结合,形成既能阻止地下的盐分上升,又能拦截、蓄积雨水的作用。下列对聚丙烯酸酯的叙述中正确的是( )

①聚丙烯酸酯的单体的结构简式为CH2=CHCOOR
②聚丙烯酸酯没有固定的熔沸点
③聚丙烯酸酯能发生加成反应
④合成聚丙烯酸酯的反应属于缩聚反应
A. ③④ B. ①② C. ①②③ D. ①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.在化学反应过程中,发生物质变化的同时不一定发生能量变化
B.生成物全部化学键形成时所释放的能量大于破坏反应物全部化学键所吸收的能量时,反应为吸热反应
C.反应产物的总焓大于反应物的总焓时,反应吸热,△H>0
D.△H的大小与热化学方程式的计量系数无关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所学知识完成题目:
(1)12.4gNa2X中含Na+0.4mol,则Na2X的摩尔质量是 , X的相对原子质量是 .
(2)某硫酸钠溶液中含有3.01×1022个Na+ , 则该溶液中SO42﹣的物质的量是 .
(3)人造空气(氧气和氦气的混合气)可用于减轻某些疾病或供深水潜水员使用.在标准状况下,11.2L“人造空气”的质量是4.8g,其中氧气和氦气的分子数之比是 , 氧气的质量是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在溶液中能大量共存的是( )
A.Cu2+、Mg2+、SO42﹣、NO3﹣
B.H+、Mg2+、SO42﹣、ClO﹣
C.Ag+、Na+、NO3﹣、Cl﹣
D.NH4+、Ba2+、NO3﹣、OH﹣
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com