
在同温同压下,下列各组热化学方程式中Q2>Q1的是
A.2H2(g)+O2(g)====2H2O(g) ΔH=-Q1 2H2(g)+O2(g)====2H2O(l) ΔH=-Q2
B.S(g)+O2(g)====SO2(g) ΔH=-Q1 S(s)+ O2(g)====SO2(g) ΔH=-Q2
C.C(s)+O2(g)====CO2(g) ΔH=-Q1 C(s)+1/2O2(g)====CO(g) ΔH=-Q2
D.H2(g)+Cl2(g)====2HCl(g) ΔH=-Q1
1/2 H2(g)+1/2Cl2(g)====HCl(g) ΔH=-Q2
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案科目:高中化学 来源:2016届甘肃省张掖市高三上学期第一次质量检测化学试卷(解析版) 题型:填空题
硫和氮氧化物是形成酸雨、雾霾等环境污染的罪魁祸首,采用合适的措施消除其污染是保护环境的重要举措。
(1)研究发现利用NH3可消除硝酸尾气中的NO污染。NH3与NO的物质的量之比分别为1﹕3、3﹕1、4﹕1时,NO脱除率随温度变化的曲线如图所示:
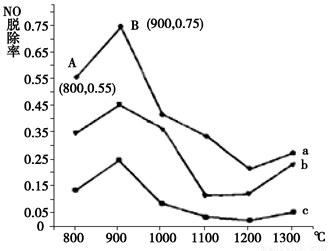
①用化学反应方程式表示NH3消除NO的反应原理 (不用注明反应条件)。
②曲线b 对应NH3与NO的物质的量之比是 。
③曲线a中,NO的起始浓度为6×10-4mg/m3,从A点到B点经过0.8 s,该时间段内NO的脱除速率为____ mg/(m3·s)。
(2)NO、NO2混合气体能被NaOH溶液吸收生成NaNO2和NaNO3,若吸收的溶液中N 的浓度为ag·L- 1,要使1m3该溶液中的完全转化为,至少需通入标准状况下的O2 L。(用含a的代数式表示,计算结果保留整数)
(3)SO2被少许NaOH溶液吸收生成能使pH试纸变红的NaHSO3溶液,工业上可电解NaHSO3得到重要化工产品Na2S2O4。
①NaHSO3溶液中离子浓度大小为 。
②写出生成S2的电极反应式 。
查看答案和解析>>
科目:高中化学 来源:2016届天津一中高三零月考化学试卷(解析版) 题型:推断题
下图所示各物质是由1~20号元素中部分元素组成的单质或其化合物,图中部分反应条件未列出。已知C、H是无色有刺激性气味的气体,D是一种黄绿色的气体单质,物质J可用于泳池消毒。反应②和④是化工生产中的重要反应,反应⑤是实验室制备气体C的重要方法。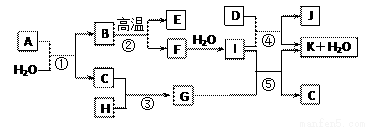
请回答下列问题:
(1)物质E的电子式________;I中所含化学键类型__________;气体D所含元素在周期表中的位置_____。
(2)G的水溶液呈____性,用离子方程式表示其原因___________________
(3)写出E与过量I溶液反应的离子方程式________________。
(4)实验室制备气体C的化学方程式__________________。
(5)已知含7.4gI的稀溶液与200mL1mol/L的H溶液反应放出11.56kJ的热量,写出该反应的热化学方程式___________________
(6)物质A由三种元素组成,1 mol A与水反应可生成1 mol B和2 mol C,A化学式为____________
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州省高二上第一半月考化学试卷(解析版) 题型:选择题
已知下列数据:
2Fe(s)+O2(g)===2FeO(s) ΔH=-544 kJ·mol-1
4Al(s)+3O2(g)===2Al2O3(s) ΔH=-3 350 kJ·mol-1
则2Al(s)+3FeO(s)===Al2O3(s)+3Fe(s)的ΔH是
A.-859 kJ·mol-1 B.+859 kJ·mol-1
C.-1 403 kJ·mol-1 D.-2 491 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西太原五中高二上第一周考理科化学试卷(解析版) 题型:选择题
反应4NH3(g)+5O2(g) 4NO(g)+6H2O(g),在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率V(x)可表示为
A.V(NH3)=0.010mol/(L·S) B.V(O2)=0.0010mol/(L·S)
C.V(NO)=0.0010mol/(L·S) D.V(H2O)=0.045mol/(L·S)
查看答案和解析>>
科目:高中化学 来源:2016届湖南省衡阳市高三上学期第一次月考化学试卷(解析版) 题型:选择题
关于铅蓄电池的说法正确的是
A.在放电时,正极发生的反应是Pb(s)+SO42-(aq)-2e-===PbSO4(s)
B.在放电时,该电池的负极材料是铅板
C.在充电时,电池中硫酸的浓度不断变小
D.在充电时,阳极发生的反应是PbSO4(s)+2e-===Pb(s)+SO42-(aq)
查看答案和解析>>
科目:高中化学 来源:2016届湖南省衡阳市高三上学期第一次月考化学试卷(解析版) 题型:选择题
下列叙述正确的是
A.将5.85 g NaCl晶体溶入100 mL水中,制得0.1 mol/L NaCl溶液
B.将1体积c mol/L硫酸溶液用水稀释为5体积,得到0.2c mol/L硫酸溶液
C.将25 g无水CuSO4溶于水制成100 mL溶液,其浓度为1 mol/L
D.将w g a% NaCl溶液蒸发掉w/2 g水,得到4a%NaCl溶液
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高一入学摸底化学试卷(解析版) 题型:填空题
已知:A、B为常见的非金属单质且均为气体;甲、乙为短周期金属单质,乙在I的浓溶液中发生钝化;C、H、J的溶液均呈碱性。各物质间的转化关系如下(部分生成物未给出,且未注明反应条件):

图10-3
(1)写出反应②的化学方程式_______________。
(2)反应④中每消耗1 mol G,转移电子的物质的量为________。
(3)反应⑥的离子方程式是______________。
(4)写出工业冶炼金属乙的化学方程式________________。
(5)实验室中保存I的浓溶液的方法是______________。
(6)SiCl4与过量A在加热条件下反应可制得高纯硅,整个制备纯硅的过程中必须严格控制无水无氧。SiCl4在潮湿的空气中因水解而产生白色烟雾,其生成物是_______________;H2还原SiCl4过程中若混入O2,可能引起的后果是________________。
(7)有一种常见金属丙,常温时只能溶于稀的I溶液,写出过量的此金属溶于稀I溶液的离子方程式___________,向此溶液中加入H溶液,现象为__________。
查看答案和解析>>
科目:高中化学 来源:2016届云南省高三第一次月考试卷化学试卷(解析版) 题型:选择题
下列叙述正确的是
A.用NaOH溶液、蒸馏水和红色石蕊试纸检验溶液中是否含有NH4+
B.用干燥的pH试纸可测得新制氯水的pH=2
C.有机物A(C4H6O2)能发生加聚反应,可推知A的结构一定是CH2=CH—COOCH3
D.食盐中的碘可以直接用淀粉检验其是否存在
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com