
| A. | 中子数为18的硫原子:$\frac{18}{16}$S | B. | CS2分子的电子式: | ||
| C. | 硫离子(S2-)的结构示意图: | D. | 苯磺酸的结构简式: |
分析 A.质量数=质子数+中子数,元素符号的左上角表示质量数、左下角表示质子数;
B.CS2为共价化合物,分子中中含有两个C=S键;
C.硫离子的核电荷数为16,最外层含有8个电子;
D.苯磺酸中S与苯环碳原子相连.
解答 解:A.中子数为18的硫原子的质量数为34,该S原子可以表示为1634S,故A错误;
B.硫原子与碳原子之间形成2对共用电子对,电子式为 ,故B正确;
,故B正确;
C.硫离子的核内质子数为16,核外有3个电子层,第一层上有2个电子,第二层上有8个电子,第三层上有8个电子,其离子结构示意图为 ,故C错误;
,故C错误;
D.苯磺酸中S与苯环C原子相连,苯磺酸正确的结构简式为 ,故D错误;
,故D错误;
故选B.
点评 本题考查了常见化学用语的表示方法,题目难度中等,涉及电子式、结构简式、离子结构示意图、元素符号等知识,明确常见化学用语的书写原则为解答关键,试题培养了学生的规范答题能力.


科目:高中化学 来源: 题型:填空题
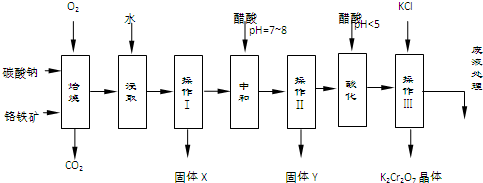
| 物质 | 溶解度/(g/100g水) | ||
| 0°C | 40°C | 80°C | |
| KCl | 28 | 40.1 | 51.3 |
| NaCl | 35.7 | 36.4 | 38 |
| K2Cr2O7 | 4.7 | 26.3 | 73 |
| Na2Cr2O7 | 163 | 215 | 376 |
 ),该反应可用来检验Cr2O72-的存在.写出反应的离子方程4H2O2+Cr2O72-+2H+═2CrO5+5H2O.该反应不属于(填“属于”或“不属于”)氧化还原反应.
),该反应可用来检验Cr2O72-的存在.写出反应的离子方程4H2O2+Cr2O72-+2H+═2CrO5+5H2O.该反应不属于(填“属于”或“不属于”)氧化还原反应.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
①分离饱和食盐水与沙子的混合物 | ②分离水和汽油的混合物 | ③分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合物,CCl4和甲苯互溶 | ④提取出碘水中的碘单质 |
| D | B | C | A |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甘油加水作护肤剂 | |
| B. | 蜂、蚁蛰咬处涂抹稀氨水可解痛 | |
| C. | 烹鱼时加入少量的料酒和食醋可减少腥味,增加香味 | |
| D. | 医用酒精可用于皮肤的消毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用铂丝蘸取溶液在酒精灯外焰上灼烧,火焰呈黄色,说明原溶液只含有Na+ | |
| B. | 加入盐酸产生无色气体,该气体能使澄清的石灰水变浑浊,原溶液一定存在CO32- | |
| C. | 加入NaOH溶液共热,产生能使湿润的红色石蕊试纸变蓝的气体,原溶液中存在NH4+ | |
| D. | 加入BaCl2溶液时,产生白色沉淀,加稀硝酸沉淀不溶解,原溶液中一定存在SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 微粒半径:X<X- | |
| B. | 简单氢化物的稳定性:Z比W的强 | |
| C. | W的氧化物的水化物的酸性一定比Z的强 | |
| D. | 最外层电子数由大到小的顺序为:Z、W、Y |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
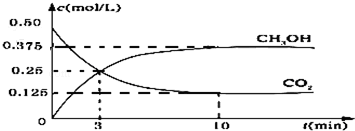
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室常用排饱和食盐水的方法收集氯气 | |
| B. | 工业合成氨控制温度在较高温度(500℃)进行 | |
| C. | 在浓氨水中加入烧碱可用于实验室快速生氨 | |
| D. | 工业上将二氧化硫转化为三氧化硫常通入过量空气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com