
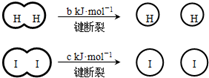
 (a、b、c均大于零)
(a、b、c均大于零)| A. | H2、I2和HI分子中的化学键都是非极性共价键 | |
| B. | 断开2mol HI分子中的化学键所需能量约为(c+b+a)kJ | |
| C. | 相同条件下,1mol H2(g)和1mol I2(g)总能量小于2molHI(g)的总能量 | |
| D. | 向密闭容器中加入2mol H2(g)和2mol I2(g),充分反应后放出的热量小于2a kJ |
分析 A.HI中存在H-I极性键;
B.依据焓变=反应物断裂化学键需要的能量-生成物形成化学键放出的能量分析判断;
C.放热反应的反应物的总能量大于生成物的总能量;
D.反应是可逆反应不能进行彻底.
解答 解:A.H2、I2分子中的化学键都是非极性共价键,HI中存在H-I极性键,故A错误;
B.△H=反应物断裂化学键需要的能量-生成物形成化学键放出的能量=bKJ/mol+cKJ/mol-2H-I=-aKJ/mol,得到断开2mol H-I键所需能量约为(a+b+c)KJ,故B正确;
C.反应是放热反应,反应物的总能量大于生成物的总能量,即相同条件下,1mol H2(g)和1mol I2(g)总能量大于2molHI(g)的总能量,故C错误;
D.反应是可逆反应不能进行彻底,依据焓变意义分析,向密闭容器中加入2mol H2和2mol I2,充分反应后放出的热量小于2a kJ,故D正确;
故选BD.
点评 本题考查了共价键、化学反应的焓变、化学键与焓变关系的计算分析应用,掌握原理和基础是解题关键,题目难度中等,侧重于考查学生的分析能力和计算能力.


 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:选择题
| A. | 玻璃钢是由玻璃纤维和合成树脂组成的材料 | |
| B. | 碳纤维增强复合材料具有韧性好,强度高而质轻的特点 | |
| C. | 硅酸盐材料是新型无机非金属材料 | |
| D. | 有机合成材料易老化,不耐高温 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
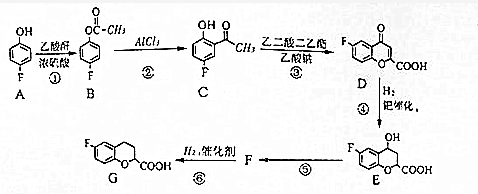
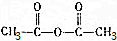 ,请回答下列问题:
,请回答下列问题: .
.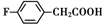 、
、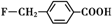 .
.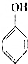 和乙酸酐为原料制备
和乙酸酐为原料制备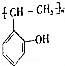 的合成路线流程图(无机试剂任选)
的合成路线流程图(无机试剂任选)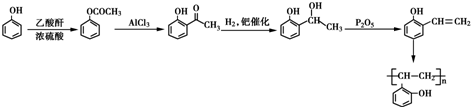 .合成路线流程图示例如下:H2C=CH2$\stackrel{HBr}{→}$CH2CH2Br$→_{△}^{NaOH溶液}$CH2CH2OH.
.合成路线流程图示例如下:H2C=CH2$\stackrel{HBr}{→}$CH2CH2Br$→_{△}^{NaOH溶液}$CH2CH2OH.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某特定反应的平衡常数只与温度有关 | |
| B. | 催化剂不能改变平衡常数的大小 | |
| C. | 平衡常数发生改变,化学平衡必发生改变 | |
| D. | 化学平衡移动时,平衡常数必改变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸铝溶液中加入过量氨水:Al3++4OH-═AlO2-+2H2O | |
| B. | 浓盐酸与铁屑反应:2Fe+6H+═2Fe3++3H2↑ | |
| C. | 钠与CuSO4溶液反应:2Na+Cu2+═Cu↓+2Na+ | |
| D. | 在8.12天津大爆炸中消防员喷洒双氧水以防止氰化钠污染环境:CN-+H2O2+H2O═HCO3-+NH3↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
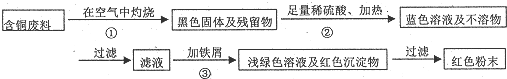
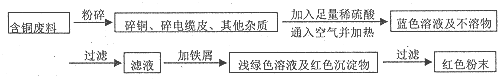
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若NO2与O2的体积比是4:3,则此溶液除了硝酸不含其他杂质 | |
| B. | 将一定量的Cu投入溶液中,只产生1.12L(标况)的红棕色气体,则反应的铜有1.6g | |
| C. | 将溶液在强光下光照,产生气泡,溶液变浅黄,产生气泡,则气泡是NO2 | |
| D. | 向浅黄的硝酸中通入氧气,可以使其pH值降低,溶液质量不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
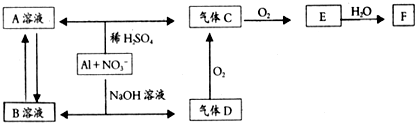

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com