
分析 A.容量瓶为精密仪器,不能盛放过热液体;
B.定容后,经摇匀后发现液面低于刻度线,部分溶液沾到瓶塞上,是正常操作;
C.量取5.2mL稀硫酸,应该使用10mL量筒;
D.托盘天平精确值为0.1g;
E.为防止试管中的液体沸腾时喷出伤人,试管中的液体体积最好不要超过试管容积的$\frac{1}{3}$;
F.浓硫酸和氢氧化钠都具有强腐蚀性,不能立即用氢氧化钠溶液冲洗;
G.蒸馏时,温度计测量的是蒸汽的温度;
解答 解:A容量瓶为精密仪器,不能盛放过热液体,所以溶液稀释、冷却后才能转移到容量瓶中,故A正确;
B.定容后,经摇匀后发现液面低于刻度线,部分溶液沾到瓶塞上,是正常操作,再加入蒸馏水使其液面与刻度线相平,导致溶液体积偏大,溶液浓度偏低,故B错误;
C.使用200ml量筒量取5.2ml稀硫酸,会产生较大的误差,应该使用10mL量筒量取5.2mL稀硫酸,故C错误;
D.托盘天平精确值为0.1g,故D错误;
E.为防止试管中的液体沸腾时喷出伤人,试管中的液体体积最好不要超过试管容积的$\frac{1}{3}$,故E正确;
F.浓硫酸和氢氧化钠都具有强腐蚀性,所以在实验中如果不慎将浓硫酸沾到皮肤上,应立即先用抹布拭去,然后用大量水冲洗,然后涂上3%~5%的碳酸氢钠溶液,故F错误;
G.蒸馏时,温度计测量的是蒸汽的温度,水银球应放在蒸馏烧瓶支管口处,故G错误;
故选:A E.
点评 本题为实验综合题,考查了常见仪器的使用方法和注意事项,化学安全事故及处理方法等知识,侧重于学生的分析能力和实验能力的考查,掌握基础是解题关键,注意相关知识的积累.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 用食醋清洗热水瓶中的水垢;用米汤检验碘盐中含有碘酸钾 | |
| B. | 小苏打可中和胃酸,热纯碱溶液可除油污;小苏打和纯碱可以用石灰水鉴别 | |
| C. | 用丁达尔效应区别鸡蛋白溶液和食盐水 | |
| D. | “84消毒液”和洁厕剂能同时使用,除污垢效果更好 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 升高温度平衡向正反应方向移动 | |
| B. | 该反应在任何温度下均能自发进行 | |
| C. | 向容器中充入少量He,平衡向正反应方向移动 | |
| D. | 该反应的△S<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如图是可逆反应X2+3Y2?2Z2 在反应过程中的反应速率(V)与时间(t)的关系曲线,下列叙述不正确的是( )
如图是可逆反应X2+3Y2?2Z2 在反应过程中的反应速率(V)与时间(t)的关系曲线,下列叙述不正确的是( )| A. | t2时,反应到达限度 | B. | t2-t3,反应仍在进行 | ||
| C. | t1时,只有正方向反应 | D. | t2-t3,各物质的浓度不再发生变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
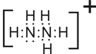
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2NO2═O2+2NO;△H=+116.2kJ/mol(反应热) | |
| B. | S(s)+O2(g)═SO2(g);△H=+269.8kJ/mol(反应热) | |
| C. | Ba(OH)2(aq)+2HCl(aq)═BaCl2(aq)+2H2O(l));△H=-57.3kJ/mol(中和热) | |
| D. | C2H5OH(l)+3O2(g)═2CO2(g)+3H2O(g);△H=-1367.0kJ/mol(燃烧热) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.8 mol | B. | 2.6 mol | C. | 1.4 mol | D. | 0.8 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol K2SO4溶于水,所得溶液中K+的数目为NA | |
| B. | 常温常压下,32g氧气所含分子的数目为NA | |
| C. | 标准状况下,22.4LH2O含有氢原子的数目为2 NA | |
| D. | 11.2L H2含有氢原子的数目为NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com