
【题目】在四个不同的容器中,在不同的条件下进行合成氨反应,根据下列在相同时间内测得的结果判断,生成氨的反应速率最快的是
A.v (N2)=0.2molL﹣1min﹣1B.v (N2)=5molL﹣1s﹣1
C.v (NH3)=0.1molL﹣1min﹣1D.v (H2)=0.3molL﹣1min﹣1
 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:高中化学 来源: 题型:
【题目】下列关于盐类水解的说法错误的是( )
A.浓度均为0.1 mol·L-1的①(NH4)2CO3、②(NH4)2SO4、③(NH4)2Fe(SO4)2溶液中,c(NH4+)的大小顺序为①>②>③
B.pH相等的①NaHCO3、②Na2CO3、③NaOH溶液的物质的量浓度大小:①>②>③
C.在NH4Cl溶液中加入稀HNO3,能抑制NH4+水解
D.将硫酸亚铁溶液加热蒸干得不到原溶质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳和碳的化合物在生产、生活中的应用非常广泛,在提倡健康生活已成潮流的今天,“低碳生活”不再只是一种理想,更是一种值得期待的新的生活方式。
(1)甲烷燃烧放出大量的热,可作为能源用于人类的生产和生活。
已知:①2CH4(g)+3O2(g)=2CO(g)+4H2O(l) △H=—1214 kJ/mol
②2CO(g)+O2(g)=2CO2(g) △H= —566kJ/mol
则表示甲烷燃烧热的热化学方程式_______________________。
(2)生产甲醇的原料CO和H2来源于:CH4(g)+H2O(g)![]() CO(g)+3H2(g)
CO(g)+3H2(g)
①一定条件下CH4的平衡转化率与温度、压强的关系如图,则Pl_______P2;A、B、C三点处对应平衡常数(KA、KB、KC)的大小顺序为___________(填“<”、“>”“=”)。
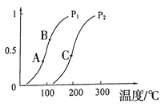
②100℃时,将1mol CH4和2mol H2O通入容积为10L的反应室,反应达平衡的标志是:_______。
a.容器的压强恒定
b.单位时间内消耗0.1mol CH4同时生成0.3mol H2
c.容器内气体密度恒定
d.3v(CH4)=v(H2)
e. 容器内气体平均相对分子质量恒定
(3)已知2H2(g)+CO(g)![]() CH3OH(g)△H=-akJmol-1(a>0),在一个容积固定的容器中加入2mol H2和1mol CO,在500℃时充分反应,达平衡后CH3OH的浓度为W molL-1。反应平衡后,若向原来容器中再加入2mol H2和1mol CO,500℃充分反应再次达平衡后,则CH3OH浓度___________2WmolL-1(填“>”、“<”或“=”)。
CH3OH(g)△H=-akJmol-1(a>0),在一个容积固定的容器中加入2mol H2和1mol CO,在500℃时充分反应,达平衡后CH3OH的浓度为W molL-1。反应平衡后,若向原来容器中再加入2mol H2和1mol CO,500℃充分反应再次达平衡后,则CH3OH浓度___________2WmolL-1(填“>”、“<”或“=”)。
(4)某实验小组利用CO(g)、O2(g)、KOH(aq)设计成如图所示的电池装置,

①负极的电极反应式为___________。
②用该原电池做电源,用惰性电极电解200mL饱和食盐水(足量),消耗标准状况下的CO 224mL,则溶液的pH=___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱式氧化镍(NiOOH)可用作镍氢电池的正极材料,可用废镍催化剂(主要含Ni、Al,少量Cr、FeS 等)来制备,其工艺流程如下:
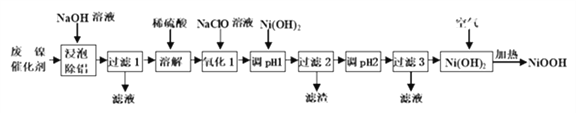
回答下列问题:
(1)“浸泡除铝”时,发生反应的离子反应方程式为_________________________;
(2)“溶解”时放出的气体为_______________ (填化学式);
(3)已知该条件下金属离子开始沉淀和完全沉淀的pH如下表:
开始沉淀的pH | 完全沉淀的pH | |
Ni2+ | 6.2 | 8.6 |
Fe2+ | 7.6 | 9.1 |
Fe3+ | 2.3 | 3.3 |
Cr3+ | 4.5 | 5.6 |
“调pH 1”时,溶液pH范围为______________________;
(4)在空气中加热Ni(OH)2可得NiOOH,请写出此反应的化学方程式_____________;
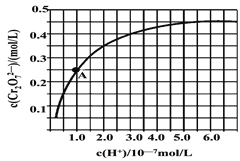
(5)金属铬在溶液中有多种存在形式, CrO42—和Cr2O72—在溶液中可相互转化。室温下,初始浓度为1.0mol/L的Na2CrO4溶液中c(Cr2O72—)随c(H+)的变化如图所示,用离子方程式表示Na2CrO4溶液中的转化反应________________,根据A点数据计算出该转化反应的平衡常数为______________,温度升高,溶液中CrO42—的平衡转化率减小,则该反应的△H____0(填“>”、“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化锌为白色粉末,可用于湿疹、癣等皮肤病的治疗。工业ZnO中含有Fe(Ⅱ)、Mn(Ⅱ)、Ni(Ⅱ),纯化工业ZnO的流程如下:
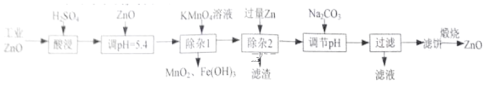
提示:在本实验条件下,Ni(Ⅱ)不能被氧化。
(1)“酸浸”时需不断通入髙温水蒸气,其目的是 ________________。
(2)“除杂I”中生成Fe(OH)3反应的离子方程式为______________________________。
(3)“除杂2”中所得滤渣主要成分是____________。
(4)滤饼要用水洗,检验是否洗涤干净的方法是_________________。
(5)已知:Zn(OH)2 的 Ksp=l×10-17。室温下为使Zn2+完全沉淀(其浓度<1×10-5mol·L-1),需调节溶液pH范围为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二茂铁![]() 的结构简式为
的结构简式为![]() ,与芳香族化合物性质相似,广泛应用于航天、化工等领域,可以环戊二烯与铁为原料制得。下列说法错误的是( )
,与芳香族化合物性质相似,广泛应用于航天、化工等领域,可以环戊二烯与铁为原料制得。下列说法错误的是( )
A.环戊二烯的化学式为![]() B.二茂铁的一氯取代物有2种
B.二茂铁的一氯取代物有2种
C.二茂铁能发生加成反应、氧化反应D.二茂铁中的铁为![]() 价
价
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向![]() 未知浓度的
未知浓度的![]() 、
、![]() 混合溶液逐滴滴加
混合溶液逐滴滴加![]() 溶液,混合溶液的电导率(导电能力)如图所示,下列叙述错误的是( )
溶液,混合溶液的电导率(导电能力)如图所示,下列叙述错误的是( )
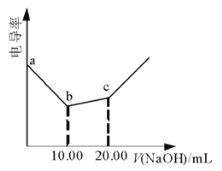
A.![]() 两点水的电离程度:
两点水的电离程度:![]()
B.原溶液中![]()
C.![]() 是
是![]() 恰好被
恰好被![]() 溶液中和的过程
溶液中和的过程
D.![]() 点:
点:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化合物的结构如图所示,分子中所有原子都达到了 8电子稳定结构,X、Y、Z、W是原子序数依次增大的短周期主族元素,原子半径:r(X)>r(Y)>r(Z),W的单质可用来制取漂白剂和自来水消毒。下列说法正确的是
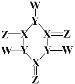
A.YZ2属于酸性氧化物
B.X的氧化物的水化物酸性弱于W的氧化物的水化物酸性
C.X、Y、Z与氢元素均可形成含非极性键的二元化合物
D.Z分别与W、X、Y形成的二元化合物均不止一种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含硅元素的化合物广泛存在于自然界中,与其他矿物共同构成岩石.晶体硅(熔点 1410℃)用途广泛,制取与提纯方法有多种.
(1)炼钢开始和结束阶段都可能发生反应:Si+2FeO![]() 2Fe+SiO2,其目的是________________.
2Fe+SiO2,其目的是________________.
A.得到副产品硅酸盐水泥 B.制取SiO2,提升钢的硬度
C.除去生铁中过多的Si杂质 D.除过量FeO,防止钢变脆
(2)一种由粗硅制纯硅过程如下:Si(粗)![]() SiCl4
SiCl4![]() SiCl4(纯)
SiCl4(纯)![]() Si(纯),在上述由SiCl4制纯硅的反应中,测得每生成 1.12kg纯硅需吸收a kJ热量,写出该反应的热化学方程式:________________.
Si(纯),在上述由SiCl4制纯硅的反应中,测得每生成 1.12kg纯硅需吸收a kJ热量,写出该反应的热化学方程式:________________.
对于钠的卤化物(NaX)和硅的卤化物(SiX4)下列叙述正确的是________________
A.NaX易水解
B.SiX4是共价化合物
C.NaX的熔点一般高于SiX4
D.SiF4晶体是由共价键形成的空间网状结构
(3)粗硅经系列反应可生成硅烷(SiH4),硅烷分解也可以生成高纯硅.硅烷的热稳定性弱于甲烷,所以Si元素的非金属性弱于C元素,用原子结构解释其原因:________________.
(4)此外,还可以将粗硅转化成三氯氢硅(SiHCl3),通过反应:SiHCl3(g)+H2(g)Si(s)+3HCl(g)制得高纯硅.不同温度下,SiHCl3的平衡转化率随反应物的投料比(反应初始时,各反应物的物质的量之比)的变化关系如图所示.下列说法正确的是________________(填字母序号).

a.该反应的平衡常数随温度升高而增大
b.横坐标表示的投料比应该是![]()
c.实际生产中为提高SiHCl3的利用率,可适当降低压强
(5)硅元素最高价氧化物对应的水化物是H2SiO3.室温下,0.1mol/L的硅酸钠溶液和0.1mol/L的碳酸钠溶液,碱性更强的是___________,其原因是________________.已知:H2SiO3:Ka1=2.0×10﹣10、Ka2=1.0×10﹣12,H2CO3:Ka1=4.3×10﹣7 Ka2=5.6×10 ﹣11.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com