
¹¤ŅµÉĻÖʱøBaCl2µÄ¹¤ŅÕĮ÷³ĢĶ¼ČēĻĀ£ŗ
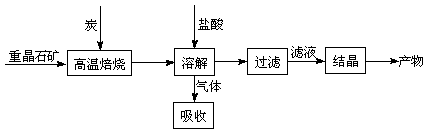
Ä³ŃŠ¾æŠ”×éŌŚŹµŃéŹŅÓĆÖŲ¾§ŹÆ£ØÖ÷ŅŖ³É·ÖBaSO4£©¶Ō¹¤Ņµ¹ż³Ģ½ųŠŠÄ£ÄāŹµŃ锣²é±ķµĆ
BaS O4(s) + 4C(s)
O4(s) + 4C(s) 4CO(g) + BaS(s) ”÷H1 = 571.2 kJ”¤mol-1 ¢Ł
4CO(g) + BaS(s) ”÷H1 = 571.2 kJ”¤mol-1 ¢Ł
BaSO4(s) + 2C(s) 2CO2(g) + BaS(s) ”÷H2= 226.2 kJ”¤mol-1 ¢Ś
2CO2(g) + BaS(s) ”÷H2= 226.2 kJ”¤mol-1 ¢Ś
¢ÅĘųĢåÓĆ¹żĮæNaOHČÜŅŗĪüŹÕ,µĆµ½Įņ»ÆÄĘ”£Na2SĖ®½āµÄĄė×Ó·½³ĢŹ½ĪŖ ”£
¢ĘĻņBaCl2ČÜŅŗÖŠ¼ÓČėAgNO3ŗĶKBr£¬µ±Į½ÖÖ³Įµķ¹²“ꏱ£¬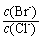 = ”£
= ӣ
[Ksp(AgBr)=5.4”Į10-13£¬Ksp(AgCl)=2.0”Į10-10]
¢Ē·“Ó¦C(s) + CO2(g) 2CO(g)µÄ”÷H2= kJ”¤mol-1”£
2CO(g)µÄ”÷H2= kJ”¤mol-1”£
 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾»Æѧ”Ŗ”ŖŃ”ŠŽ2:»ÆѧÓė¼¼Źõ”æ(15·Ö)
ĄūÓĆÉś²śĮ×ļ§£Ū(NH4)3PO4£ŻÅŷŵķĻŌüĮ×»ŅŹÆ£Ū(Ca3(PO4)2)£ŻÖĘČ”ĮņĖį²¢ĮŖ²śĖ®ÄąµÄ¹¤ŅÕĮ÷³ĢČēĻĀ:
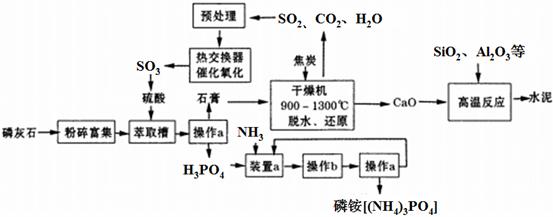
(D²Ł×÷aµÄĆū³Ę”””””””” ,ŹµŃéŹŅÖŠ½ųŠŠ“Ė²Ł×÷Ź±ÓƵ½µÄ²£Į§ŅĒĘ÷ÓŠ””””””
(2)ŌŚŹµŃéŹŅÖŠ²Ł×÷b°üĄØ____”¢ĄäČ“½į¾§”£
(3)øÉŌļ»śÖŠ·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ”””””””””””””£
(4)Ė®Äą³£ÓĆ×ö½ØÖž²ÄĮĻ,ŹĒĄūÓĆĮĖĖ®ÄąµÄ””””””ŠŌÖŹ”£
(5)SO2µÄ“ß»ÆŃõ»Æ·“Ó¦ĪŖ2SO2(g)Ź®O2(g)  2SO3(g)”£ŹµŃé²āµĆŃ¹Ēæ¼°ĪĀ¶Č¶ŌSO2×Ŗ»ÆĀŹµÄÓ°ĻģČēĻĀ±ķ(ŌĮĻĘųø÷³É·ÖµÄĢå»ż·ÖŹżĪŖSO2:7%”¢02:11%”¢N2:82%)”£
2SO3(g)”£ŹµŃé²āµĆŃ¹Ēæ¼°ĪĀ¶Č¶ŌSO2×Ŗ»ÆĀŹµÄÓ°ĻģČēĻĀ±ķ(ŌĮĻĘųø÷³É·ÖµÄĢå»ż·ÖŹżĪŖSO2:7%”¢02:11%”¢N2:82%)”£
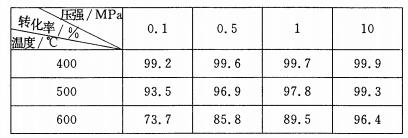
¢ŁŹµ¼ŹÉś²śÖŠ,SO2µÄ“ß»ÆŃõ»Æ·“Ó¦ŹĒŌŚ³£Ń¹”¢400”ę ”Ŗ500”ę Ģõ¼žĻĀ½ųŠŠ”£²ÉÓĆ³£Ń¹µÄÖ÷ŅŖŌŅņŹĒ”””””””” ;øĆ·“Ó¦»ÆŃ§Ę½ŗā³£Źż“󊔹ŲĻµŹĒ:K(400”ę ) ””””””K(500”ę)(Ģī”°£¾”±”¢”°£¼”±»ņ”°=”± )”£
¢Ś“ß»ÆŃõ»ÆŹ±Ź¹ÓĆČČ½»»»Ę÷µÄŌŅņŹĒ ”””””””””””£
(6)ÖĘĮņĖįĖł²śÉśµÄĪ²Ęų³żĮĖŗ¬ÓŠN2”¢O2Ķā,»¹ŗ¬ÓŠSO2”¢Ī¢ĮæµÄSO3ŗĶĖįĪķ”£ĻĀĮŠÄÜÓĆÓŚ²ā¶ØĮņĖįĪ²ĘųÖŠSO2ŗ¬ĮæµÄŹŌ¼Į×éŹĒ”””””””””£(ĢīŠ“ĻąÓ¦×ÖÄø)
a”¢NaOHČÜŅŗ”¢·ÓĢŖŹŌŅŗ b”¢Na2CO3ČÜŅŗ”¢·ÓĢŖŹŌŅŗ
c”¢µāĖ®”¢µķ·ŪČÜŅŗ d”¢KMnO4ČÜŅŗ”¢Ļ”ĮņĖį
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĀĮÓė¹żĮæµÄĻ”ŃĪĖį·“Ó¦£¬ĪŖĮĖ¼õ»ŗ·“Ó¦ĖŁĀŹ£¬µ«ŹĒÓÖ²»Ó°ĻģÉś³ÉµÄĒāĘų×ÜĮ棬ĻĀĮŠ²ÉČ”“ėŹ©²»ÄÜ“ļµ½ŹµŃéÄæµÄµÄŹĒ£Ø £©
A£®¼ÓČėŅ»¶ØĢå»żµÄNaClČÜŅŗ B£®¼ÓČėŅ»¶ØĢå»żµÄKNO3±„ŗĶČÜŅŗ
C£®¼ÓČėÉŁĮæµÄNa2CO3¹ĢĢå D£®¼ÓČėÉŁĮæµÄNaOH¹ĢĢå
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
MOHŗĶROHĮ½ÖÖŅ»ŌŖ¼īµÄČÜŅŗ·Ö±š¼ÓĖ®Ļ”ŹĶŹ±£¬pH±ä»ÆČēĻĀĶ¼ĖłŹ¾”£ĻĀĮŠŠšŹöÖŠ²»ÕżČ·µÄŹĒ£ŗ £Ø £©
A£®ROHŹĒŅ»ÖÖĒæ¼ī
B£®ŌŚxµć£¬MOH²¢Ć»ÓŠĶźČ«µēĄė
C£®ŌŚxµć£¬c(M+)=c(R+)
D£®Ļ”ŹĶĒ°£¬c(ROH)=10c(MOH)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠČÜŅŗÖŠÓŠ¹ŲĪļÖŹµÄĮæÅØ¶Č¹ŲĻµÕżČ·µÄŹĒ £Ø £©
A. pH = 2 µÄHAČÜŅŗÓėpH=12µÄMOHČÜŅŗČĪŅā±Č»ģŗĻ
c(H£«) £« c(M+)=c(A£) £« c(OH£)
B. pHĻąµČµÄCH3COONa”¢NaOHŗĶNaCO3ČżÖÖČÜŅŗ£ŗ
c(NaOH) < c(CH3COONa) < c(NaCO3)
C. ĪļÖŹµÄĮæÅضČĻąµČµÄCH3COOHŗĶCH3COONaČÜŅŗµČĢå»ż»ģŗĻ
c(CH3COO-) £« 2c(OH£) = 2c(H+) £« c(CH3COOH)
D. 0.1mol”¤L£1µÄNaHAČÜŅŗ£¬ĘäpH = 4£ŗc(HA-)£¾c(H+)£¾c(H2A)£¾c(A2£)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
½«0.01molĻĀĮŠĪļÖŹ·Ö±š¼ÓČė100mLÕōĮóĖ®ÖŠ£¬»Öø“ÖĮŹŅĪĀ£¬ĖłµĆČÜŅŗÖŠŅõĄė×ÓÅØ¶ČµÄ“óŠ”Ė³ŠņŹĒ£ØČÜŅŗĢå»ż±ä»ÆŗöĀŌ²»¼Ę£©
¢ŁNa2O2¢ŚNa2O¢ŪNa2CO3¢ÜNaCl£Ø£©
| A£® | ¢Ł£¾¢Ś£¾¢Ū£¾¢Ü | B£® | ¢Ł£¾¢Ś£¾¢Ü£¾¢Ū | C£® | ¢Ł=¢Ś£¾¢Ū£¾¢Ü | D£® | ¢Ł=¢Ś£¾¢Ū=¢Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
Na2CO3¹ĢĢåÖŠæÉÄÜŗ¬ÓŠŌÓÖŹK2CO3”¢NaHCO3”¢NaClÖŠŅ»ÖÖ»ņ¼øÖÖ£¬Č”10.6gѳʷ£¬¼ÓČė×ćĮæµÄĻ”ŃĪĖį²śÉśĘųĢå4.8g£¬ĻĀĮŠ·ÖĪöÕżČ·µÄŹĒ£Ø£©
| A£® | Ņ»¶Øŗ¬ÓŠNaHCO3 | B£® | Ņ»¶Øŗ¬ÓŠK2CO3 | |
| C£® | Ņ»¶Ø²»ŗ¬NaCl | D£® | Ņ»¶Øŗ¬ÓŠNaCl |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĆę¹ŲÓŚ»Æѧ·“Ó¦µÄĻŽ¶ČµÄŠšŹöÖŠ£¬ÕżČ·µÄŹĒ( )
A£®»Æѧ·“Ó¦µÄĻŽ¶Č¶¼ĻąĶ¬
B£®æÉŅŌĶعżøıäĪĀ¶ČæŲÖĘ»Æѧ·“Ó¦µÄĻŽ¶Č
C£®æÉŅŌĶعżŃÓ³¤»Æѧ·“Ó¦µÄŹ±¼äøıä»Æѧ·“Ó¦µÄĻŽ¶Č
D£®µ±Ņ»øö»Æѧ·“Ó¦ŌŚŅ»¶ØĢõ¼žĻĀ“ļµ½ĻŽ¶ČŹ±£¬·“Ó¦¼“Ķ£Ö¹
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠø÷×éĄė×ÓŌŚÖø¶ØČÜŅŗÖŠ£¬ÄÜ“óĮæ¹²“ęµÄŹĒ £Ø £©
¢ŁĪŽÉ«ČÜŅŗÖŠ£ŗK+£¬Cl££¬Ca2+£¬CO33££¬SO42££¬NO3£
¢ŚpH=11µÄČÜŅŗÖŠ£ŗCO32££¬Na+£¬[Al(OH)4]££¬NO3££¬S2££¬SO32£
¢ŪĖ®µēĄėµÄH+ÅضČc(H+)=10£12mol”¤L£1µÄČÜŅŗÖŠ£ŗCl££¬CO32££¬NO3££¬NH4+£¬SO32£
¢Ü¼ÓČėMgÄܷųöH2µÄČÜŅŗÖŠ£ŗMg2+£¬NH4+£¬Cl££¬K+£¬SO42£
¢ŻŹ¹ŹÆČļ±äŗģµÄČÜŅŗÖŠ£ŗFe2+£¬MnO4££¬NO3££¬Na+£¬SO42£
¢ŽÖŠŠŌČÜŅŗÖŠ£ŗFe3+£¬Al3+£¬NO3££¬I££¬Cl££¬S2£
A£®¢Ł¢Ś¢Ż”””” B£®¢Ł¢Ū¢Ž”””” C£®¢Ś¢Ü”” ”” D£®¢Ł¢Ś¢Ü
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com