
【题目】H2S2O3是一种弱酸,实验室欲用0.01 mol·L-1的Na2S2O3溶液滴定I2溶液,发生的反应为:I2+2Na2S2O32NaI+Na2S4O6,下列说法合理的是( )
A. 该滴定可选用如图所示装置示剂;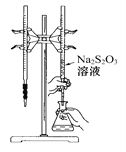
B. 该滴定可用甲基橙作指;
C. Na2S2O3是该反应的还原剂;
D. 该反应中每消耗2 mol Na2S2O3,电子转移数为4 mol;
【答案】C
【解析】分析:A、Na2S2O3溶液显碱性;
B、根据碘遇淀粉溶液变蓝色分析解答;
C、根据Na2S2O3中S元素化合价变化分析;
D、根据Na2S2O3中S元素化合价变化解答。
详解:A、Na2S2O3溶液显碱性,应该用碱式滴定管,A错误;
B、溶液中有单质碘,加入淀粉溶液呈蓝色,碘与Na2S2O3发生氧化还原反应,当反应终点时,单质碘消失,蓝色褪去,B错误;
C、Na2S2O3中S元素化合价由+2价升高到+2.5价,失去电子被氧化,作还原剂,C正确;
D、Na2S2O3中S元素化合价由+2价升高到+2.5价,因此反应中每消耗2mol Na2S2O3,转移2mol电子,D错误;答案选C。


 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案科目:高中化学 来源: 题型:
【题目】氰基丙烯酸酯在碱性条件下能快速加聚面具有胶黏性。某种氰基丙烯酸酯(G) 的合成路线如下图所示。已知有机物A的核磁共振氢谱显示为单峰。

请按要求回等下列问题:
(1)A所含官能团的名称为_________
(2)B的结构简式为__________
(3)反应②的反应类型为_________
(4)反应④的化学方程式为__________
(5)G的结构简式为_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒容密闭容器中通入X并发生反应:2X(g)![]() Y(g),温度T1、T2下X的物质的量浓度c(X)随时间t变化的曲线如图所示,下列叙述正确的是
Y(g),温度T1、T2下X的物质的量浓度c(X)随时间t变化的曲线如图所示,下列叙述正确的是
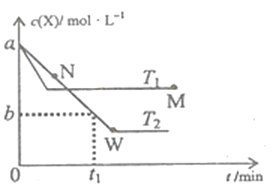
A. M点的正反应速率υ正小于N点的逆反应速率υ逆
B. T2下,在0~t1时间内,υ(Y)=![]() mol/(L·min)
mol/(L·min)
C. M点时再加入一定量X,平衡后X的转化率减小
D. 该反应进行到M点放出的热量小于进行到W点放出的热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在饱和氯水中能大量共存的是( )
A.Fe2+、Na+、Cl﹣、NO3﹣
B.Na+、Al3+、SO42﹣、Cl﹣
C.NH4+、K+、NO3﹣、S2﹣
D.Na+、K+、HCO3﹣、SiO32﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸铜可用于消毒、制杀虫剂、镀铜等。实验小组制取CuSO4·5H2O晶体并进行热分解的探究。请回答以下问题:
探究Ⅰ:制取CuSO4·5H2O晶体
小组同学设计了如下两种方案:
甲:将铜片加入足量浓硫酸中并加热
乙:将铜片加入稀硫酸,控温40~50℃,滴加双氧水
(1)方案甲发生反应的化学方程式为____________,反应结束后有大量白色固体析出。简述从中提取CuSO4·5H2O晶体的方法:倒出剩余液体,____________。
(2)方案乙发生反应:Cu+H2SO4+H2O2=CuSO4+2H2O,该实验控温40~50℃的原因是________;与方案甲相比,方案乙的主要优点有_________、___________。(写出2种)
探究Ⅱ:用以下装置(加热装置省略)探究CuSO4·5H2O晶体热分解产物

已知:CuSO4·5H2O脱水后升高温度,会继续分解成CuO和气体产物,气体产物可能含有SO3、SO2、O2中的1~3种。
(3)称5.00gCuSO4·5H2O于A中加热,当观察到A中出现_____________,可初步判断晶体已完全脱水并发生分解。加热一段时间后,A中固体质量为3.00g,则此时A中固体的成分为___________。
(4)装置B中迅速生成白色沉淀,说明分解产物中有__________,C装置的作用是____________。
(5)理论上E中应收集到VmL气体,事实上体积偏少,可能的原因是______________。(不考虑泄漏等仅器与操作原因)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是某种酶生物燃料电池的工作原理示意图。下列说法中不正确的是
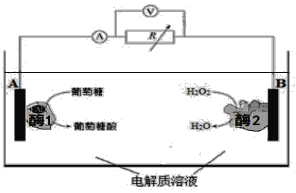
A. 葡萄糖是还原剂
B. 外电路中电子由A极移向B极
C. 溶液中H+ 由B极区移向A极区
D. B极电极反应式为:H2O2 +2H++2e-=== 2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生产、生活中产生的废水、废气是环境污染的重要源头。在环境治理方面人们可利用I2O5和Na2SO3等化工产品实现对废水和废气的治理。
(1)利用I2O5的氧化性处理废气H2S,得到S、I2两种单质,发生反应的化学方程式为________________。
(2)利用I2O5也可消除CO的污染,其反应原理为I2O5(s)+5CO(g)![]() 5CO2(g)+I2(s) ΔH。已知在不同温度(T1、T2)下,向装有足量I2O5固体的2 L恒容密闭容器中通入2 mol CO,测得CO2气体的体积分数φ(CO2)随时间t的变化曲线如图所示。
5CO2(g)+I2(s) ΔH。已知在不同温度(T1、T2)下,向装有足量I2O5固体的2 L恒容密闭容器中通入2 mol CO,测得CO2气体的体积分数φ(CO2)随时间t的变化曲线如图所示。

①温度为T2时,0~2 min 内,CO2的平均反应速率 υ(CO2)=______________。
②b点时CO的转化率为_______,化学反应的平衡常数K=_____(填表达式)。
③反应:I2O5(s)+5CO(g)![]() 5CO2(g)+I2(s)的ΔH______0(填“>”“<”或“=”)。
5CO2(g)+I2(s)的ΔH______0(填“>”“<”或“=”)。
④上述反应在T1下达到平衡时,再向容器中充入物质的量均为2 mol的CO和CO2气体,则化学平衡________(填“向左” “向右”或“不”)移动。
⑤下列现象,可以表示上述反应达到平衡状态的是____________(填字母)。
A.容器内的压强不再变化 B.混合气的平均相对分子质量不再变化
C.混合气的密度不再变化 D.单位时间内消耗CO和生成CO2的物质的量之比为1∶1
(3)Na2SO3具有还原性,其水溶液可以吸收Cl2(g),减少环境污染。
已知反应:
①Na2SO3(aq)+Cl2(g)+H2O(l) ![]() Na2SO4(aq)+2HCl(aq) ΔH1=a kJ·mol1
Na2SO4(aq)+2HCl(aq) ΔH1=a kJ·mol1
②Cl2(g)+H2O(l) ![]() HCl(aq)+HClO(aq) ΔH2=b kJ·mol1
HCl(aq)+HClO(aq) ΔH2=b kJ·mol1
试写出Na2SO3(aq)与HClO(aq)反应的热化学方程式:________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】类比是重要的学习方法,类比pH的定义可定义pOH和pKW。在某弱酸HX及其盐NaX的混合溶液中(HX和NaX的含量不确定),c(H+)和c(OH-)存在如图所示的关系,则下列说法不正确的是
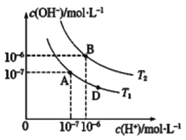
A. 图中温度T2>25℃
B. 若此混合溶液呈酸性且c(HX)=c(NaX),则HX电离能力大于NaX的水解能力
C. 位于AB线段上任意点的溶液均有pH=pOH=![]()
D. 图中D点处溶液中离子浓度:c(Na+)>c(X-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com