

| ①B2H4 |
| ②H2O2/OH |
| 56 |
| 12 |
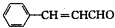 ,乙为
,乙为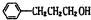 ,据此解答.
,据此解答.| 56 |
| 12 |
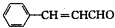 ,乙为
,乙为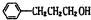 ,
,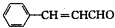 ,所含官能团有:碳碳双键、醛基,含有碳碳双键,可以发生加成反应、加聚反应,含有醛基,可以发生氧化反应,不能发生消去反应,
,所含官能团有:碳碳双键、醛基,含有碳碳双键,可以发生加成反应、加聚反应,含有醛基,可以发生氧化反应,不能发生消去反应,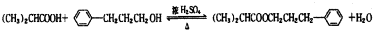 ,
,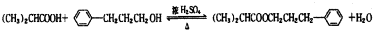 ,;
,;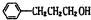 ,其同分异构体符合条件:遇FeCl3溶液显紫色,含有酚羟基;其苯环上的一溴代物只有两种,则只能有2个侧链,且处于对位,另外侧链为-CH2CH2CH3或-CH(CH3)2,故该有机物的结构简式为:
,其同分异构体符合条件:遇FeCl3溶液显紫色,含有酚羟基;其苯环上的一溴代物只有两种,则只能有2个侧链,且处于对位,另外侧链为-CH2CH2CH3或-CH(CH3)2,故该有机物的结构简式为: ,
, .
.


科目:高中化学 来源: 题型:
| A、在即将到来的新能源时代,核能、太阳能、氢能将可能成为主要能源 |
| B、开发太阳能、氢能等新型能源有利于减少二氧化碳的排放量 |
| C、煤的气化技术是减少二氧化碳排放的重要措施 |
| D、煤的“气化”和“液化”技术可提高煤的综合利用效率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 向50mL NaOH溶液中逐渐通入一定量的CO2(假设溶液体积不变),随后取此溶液10mL,将其稀释至100mL,并向此稀释后的溶液中逐滴加入0.1mol?L-1的盐酸,产生CO2气体的体积(标准状况下)与所加入的盐酸的体积关系如图,下列分析错误的是( )
向50mL NaOH溶液中逐渐通入一定量的CO2(假设溶液体积不变),随后取此溶液10mL,将其稀释至100mL,并向此稀释后的溶液中逐滴加入0.1mol?L-1的盐酸,产生CO2气体的体积(标准状况下)与所加入的盐酸的体积关系如图,下列分析错误的是( )| A、产生的CO2体积(标准状况下)为0.056L |
| B、原NaOH溶液的物质的量浓度为0.5mol?L-1 |
| C、OA段所发生反应的离子方程式:H++OH-═H2O;CO32-+H+═HCO3- |
| D、NaOH在吸收CO2后,所得溶液的溶质为NaOH和Na2CO3,其物质的量浓度之比为1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、溶液中H+向负极移动 |
| B、电子由Zn经外电路流向Cu |
| C、Zn电极反应:Zn-2e-=Zn2+ |
| D、Cu是正极 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+、AlO2-、Cl-、MnO4- 要求:无色澄清溶液 |
| B、Fe3+、NO3-、I-、HCO3- 要求:逐滴滴加盐酸立即有气体产生 |
| C、Na+、Al3+、Cl-、SO42- 逐滴滴加NaOH先有沉淀产生,后沉淀消失 |
| D、NH4+、Mg2+、SO42-、CH3COOH 要求:滴加NaOH浓溶液立刻又气体产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com