
分析 (1)酸或碱抑制水电离,pH=3的盐酸中水电离的c(H+)=c(OH-)=$\frac{{K}_{w}}{1{0}^{-pH}}$;
(2)25℃时,水的离子积Kw=10-14,某强酸溶液pH=a,则该酸溶液中氢离子浓度为10-amol/L,强碱溶液pH=b,则碱溶液中氢氧根离子浓度=10b-14 mol/L,混合后pH=7说明氢离子和氢氧根离子的物质的量相等,结合a+b=12列式计算酸溶液体积V酸和碱溶液体积V碱的关系;
(3)稀释过程中硫酸的物质的量不变,当溶液接近中性时要考虑水的电离,所以将pH=5的硫酸溶液稀释500倍后,溶液中的SO42-与H+浓度的比值约为1:10;
(4)根据溶液的pH计算溶液中氢离子浓度,根据氢氧化钠的浓度计算氢氧根离子浓度,再结合Kw=c(H+).c(OH-)计算即可;该溶液中c(H+)=10-pHmol/L=10-3mol/L,c(OH-)=$\frac{{K}_{w}}{c({H}^{+})}$,从而计算c(H+):c(OH-);
(5)纯水中c(H+)=c(OH-).
解答 解:(1)酸或碱抑制水电离,pH=3的盐酸中水电离的c(H+)=c(OH-)=$\frac{{K}_{w}}{1{0}^{-pH}}$=$\frac{1{0}^{-14}}{1{0}^{-3}}$mol/L=10-11 mol/L,故答案为:10-11;
(2)该强酸溶液pH=a,溶液中氢离子浓度为10-a mol/L,
强碱溶液pH=b,则碱溶液中氢氧根离子浓度=10b-14mol/L,
常温下混合后pH=7,说明氢离子和氢氧根离子的物质的量相等,
则:10-a mol/L×V酸=10b-14 mol/L×V碱,
整理可得:V酸=10a+b-14 V碱,而a+b=12,
则:V碱=102V酸,
故答案为:V碱=102V酸;
(3)pH为5的溶液中氢离子浓度为:c(H+)=1×10-5mol/L,硫酸根离子的浓度为:c(SO42-)=5×10-6mol/L,
溶液稀释500倍后,氢离子浓度不可能小于1×10-7mol/L,只能无限接近1×10-7mol/L,而硫酸根离子浓度为:c(SO42-)=1×10-8mol/L,
所以稀释后溶液中硫酸根离子与氢离子浓度之比为:1×10-8mol/L:1×10-7mol/L=1:10,
故答案为:1:10;
(4)0.01mol•L-1的NaOH溶液的pH为11,则氢离子浓度=10-11 mol/L,氢氧化钠是强电解质完全电离,所以溶液中氢氧根离子浓度是0.01mol/L,则Kw=c(H+).c(OH-)=0.01×10-11=10-13,
该溶液中c(H+)=10-pHmol/L=10-3mol/L,c(OH-)=$\frac{{K}_{w}}{c({H}^{+})}$=$\frac{1{0}^{-13}}{1{0}^{-3}}$mol/L=10-10mol/L,则c(H+):c(OH-)=10-3mol/L:10-7mol/L=104;
故答案为:10-13;104;
(5)纯水中c(H+)=c(OH-),则纯水中c(OH-)=5.0×10-7 mol/L,
故答案为:5.0×10-7 mol/L.
点评 本题考查pH有关计算,为高频考点,侧重考查学生分析计算能力,明确离子积常数计算方法、纯水中c(H+)和c(OH-)的关系是解本题关键,易错点是(3)题,酸或碱稀释接近中性时要考虑水的电离,且溶液接近中性不能是中性,题目难度中等.


 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | NaOH+NH4Cl═NaCl+NH3↑+H2O | B. | 2NH3+3CuO═3Cu+N2+3H2O | ||
| C. | 2Na+2NH3═2NaNH2+H2↑ | D. | NH3+CO2+H2O═NH4HCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
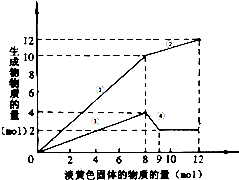 某溶液中可能含有Fe2十、Mg2+、Cu2+、NH4+、Al3+.当加入一种淡黄色固体并加热溶液时,有刺激性气味的气体放出和白色沉淀生成,加入淡黄色固体物质的量(横坐标)与析出的沉淀和产生气体的物质的量(纵坐标)的关系,如图所示.
某溶液中可能含有Fe2十、Mg2+、Cu2+、NH4+、Al3+.当加入一种淡黄色固体并加热溶液时,有刺激性气味的气体放出和白色沉淀生成,加入淡黄色固体物质的量(横坐标)与析出的沉淀和产生气体的物质的量(纵坐标)的关系,如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 沸点:乙烷>甲烷 | |
| B. | 二氯甲烷有两种不同结构的同分异构体 | |
| C. | C2H4与C4H8一定是同系物 | |
| D. | 甲苯的一氯代物有三种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金刚石>晶体硅>碳化硅 | B. | 氧化铝>氯化钾>氯化钠 | ||
| C. | CBr4>CCl4>CF4 | D. | AsH3>PH3>NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com