
| A. | 硫酸铜溶液中加入氢氧化钡溶液Cu2++SO42-+Ba2++2OH-═BaSO4↓+Cu(OH)2↓ | |
| B. | 铜片插入硝酸银溶液中:Cu+Ag+═Cu2++Ag | |
| C. | 向碳酸氢钠溶液中加入盐酸溶液:HCO3-+H+═CO2↑+H2O | |
| D. | 用氨水和氯化铝反应制备氢氧化铝沉淀:Al3++3OH-═Al(OH)3↓ |
分析 A.硫酸铜与氢氧化钡溶液反应生成硫酸钡和氢氧化铜沉淀;
B.离子方程式两边正电荷不相等;
C.碳酸氢钠与盐酸反应生成氯化钠、二氧化碳气体和水;
D.一水合氨不能拆开,应该保留分子式.
解答 解:A.硫酸铜溶液中加入氢氧化钡溶液,反应的离子方程式为:Cu2++SO42-+Ba2++2OH-═BaSO4↓+Cu(OH)2↓,故A正确;
B.铜片插入硝酸银溶液中,反应生成硝酸铜和银,正确的离子方程式为:Cu+2Ag+═Cu2++2Ag,故B错误;
C.向碳酸氢钠溶液中加入盐酸溶液,反应的离子方程式为:HCO3-+H+═CO2↑+H2O,故C正确;
D.氨水为弱碱,一水合氨必须保留分子式,正确的离子方程式为:Al3++3NH3•H2O=Al(OH)3↓+3NH4+,故D错误;
故选AC.
点评 本题考查了离子方程式的书写判断,题目难度中等,注意掌握离子方程式正误判断常用方法:检查反应能否发生,检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)等.


 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:解答题
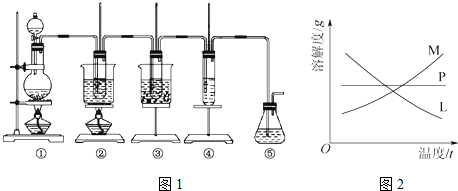
 (1)装置 I中的浓硫酸不能(能或不能)用稀硫酸代替,原因是二氧化硫易溶于水,故不能用稀硫酸.
(1)装置 I中的浓硫酸不能(能或不能)用稀硫酸代替,原因是二氧化硫易溶于水,故不能用稀硫酸.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验现象 | 原因 |
| 溶液逐渐变为红色 | 氯气与水反应生成的H+使石蕊变色 |
| 随后溶液逐渐变为无色 | 氯气与水反应生成的HClO将石蕊氧化为无色物质 |
| 然后溶液从无色逐渐变为黄绿色 | 继续通入的氯气溶于水使溶液呈黄绿色 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 在如图用石墨作电极的电解池中,放入500mL含一种溶质的某蓝色溶液(pH=4)进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成;当溶液中的原有溶质完全电解后,停止电解,取出A电极,洗涤、干燥、称量、电极增重1.6g.请回答下列问题:
在如图用石墨作电极的电解池中,放入500mL含一种溶质的某蓝色溶液(pH=4)进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成;当溶液中的原有溶质完全电解后,停止电解,取出A电极,洗涤、干燥、称量、电极增重1.6g.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 卤素原子是卤代烃的官能团.C-X之间的共用电子对偏向卤原子,形成一个极性较强的共价键,分子中C-X键易断裂 | |
| B. | 卤代烃难溶于水,易溶于大多数有机溶剂,常温下均呈液态,且密度均>1 g/cm3 | |
| C. | 强碱的水溶液中均可发生水解反应;在强碱的醇溶液中加热均可发生消去反应 | |
| D. | 卤素原子的检验步骤:①取少量卤代烃;②加入NaOH溶液;③加热煮沸;④冷却;⑤加入硝酸银溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石膏能使豆浆变成豆腐 | |
| B. | 明矾净水 | |
| C. | 花粉在水面上做布朗运动 | |
| D. | 太阳光照在弥漫灰尘的室内,可看到从窗口到地面出现一条光亮的通路 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,该烃在光照下生成的一氯代物在PMR谱中可能产生的各组信号峰的峰面积之比为3:2:2:2.
,该烃在光照下生成的一氯代物在PMR谱中可能产生的各组信号峰的峰面积之比为3:2:2:2.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com