
下列说法正确的是()
A. 我国自主研发的“龙芯1号”CPU芯片与光导纤维是同种材料
B. 需要通过化学反应才能从海水中获得食盐和淡水
C. 水晶项链和餐桌上的瓷盘都是硅酸盐制品
D. 粗硅制备单晶硅涉及氧化还原反应
考点: 硅和二氧化硅;含硅矿物及材料的应用.
专题: 碳族元素.
分析: A.光导纤维主要成分为二氧化硅,为绝缘体;
B.氯化钠溶解度随温度变化不大,利用蒸发溶剂方法得到氯化钠;
C.水晶的主要成分为二氧化硅;
D.凡是有化合价升降的反应都是氧化还原反应.
解答: 解:A.硅为良好的半导体,用作芯片,光导纤维主要成分为二氧化硅,为绝缘体,故A错误;
B.海水中获得食盐和淡水的方法是通过蒸发溶剂、蒸馏等物理过程实现,故B错误;
C.水晶的主要成分为二氧化硅,不是硅酸盐,故C错误;
D.由粗硅制取单晶硅发生Si~SiCl4~Si,它们均是氧化还原反应,故D正确;
故选:D.
点评: 本题考查了硅及其化合物的用途,明确硅、二氧化硅、硅酸盐的性质是解题关键,注意对基础知识的积累.


科目:高中化学 来源: 题型:
下列关于化学科学的叙述中,正确的是()
A. 化学学科与其他学科分支的联系不紧密
B. 化学知识只是在工业生产中起到重要作用
C. 化学研究会造成严重的环境污染,最终人类将毁灭在化学物质中
D. 化学科学是在原子、分子水平上研究物质的组成、结构、性质、变化、制备和应用的重要自然科学
查看答案和解析>>
科目:高中化学 来源: 题型:
铝是一种重要的金属,在生产、生活中具有许多重要的用途,如图是从铝土矿中制备铝的工艺流程:
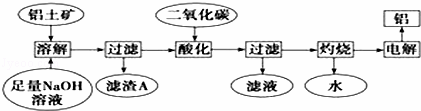
已知:(1)铝土矿的主要成分是Al2O3,此外还含有少量SiO2、Fe2O3等杂质;
(2)溶液中的Na2SiO3与Na2与 反应,能生成硅铝酸盐沉淀,化学反应方程式为:
反应,能生成硅铝酸盐沉淀,化学反应方程式为:
2Na2SiO3+2Na2═2Na2Al2Si2O8↓+2H2O+4NaOH
回答下列问题:
(1)写出向铝土矿中加入足量氢氧化钠溶液后,该步操作中主要发生反应的离子方程式: ; .
(2)滤渣A的主要成分为 ;滤渣A的用途是(只写一种) .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于氧化物的叙述不正确的是()
①非金属氧化物不一定属于酸性氧化物
②酸性氧化物都属于非金属氧化物
③金属氧化物都属于碱性氧化物
④碱性氧化物都属于金属氧化物
⑤酸性氧化物都能与水反应生成相应的含氧酸
⑥两性氧化物既能与酸也能与碱反应生成盐和水
⑦不能与酸反应的氧化物一定能与碱反应
⑧与水反应生成含氧酸的氧化物一定是酸性氧化物.
A. ①②③⑥⑧ B. ②③⑤⑦⑧ C. ②③⑤⑥⑦ D. ②③④⑥⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
现有下列物质:
①Na2CO3 ②铜 ③氯化氢 ④CO2 ⑤NaHSO4 ⑥Ba(OH)2 ⑦氢氧化铁胶体 ⑧氨水 ⑨稀硝酸 ⑩KI
(1)按物质的分类方法填写表格的空白处(填物质编号)
分类标准 电解 质 盐 非电解质 混合物
质 盐 非电解质 混合物
属于该类
的物质
(2)上述某两种物质在溶液中可发生离子反应:H++OH﹣═H2O,写出其中一个该离子反应对应的化学方程式 .
(3)物质⑩的稀溶液在空气中被氧化,加入淀粉溶液显蓝色,则反应的离子方程式为: .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列A~D四组,每组有两个反应,其中两个反应可用同一个离子方程式表示的是()
(I) (II)
A 将少量浓氨水滴入Al2(SO)4溶液 将少量Al2(SO4)3溶液滴入浓氨水
B 将少量SO2通入Ba(OH)2溶液 将过量SO2通入少量Ba(OH)2溶液
C 将0.1mol Cl2通入含0.2molFeBr2的溶液中 将0.3mol Cl2通入含0.2mol FeBr2溶液
D 将过量BaCl2溶液与少量Na2SO4溶液相混合 将少量Ba(OH)2溶液与过量MgSO4溶液相混合
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
高铁酸钠(Na2FeO4)是一种新型、高效、多功能水处理剂,是比Cl2、O3、ClO2、KMnO4氧化性更强、无二次污染的绿色水处理剂.工业制高铁酸钠的方法有如下两种:
湿法制备的主要离子反应为:2Fe(OH)3+3ClO﹣+4OH﹣=2FeO42﹣+3Cl﹣+5H2O,
干法制备的主要反应方程为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑
则下列有关说法正确的是()
A. 高铁酸钾中铁显+6价
B. 湿法中FeO42﹣是还原产物
C. 干法中每生成1mol Na2FeO4 转移4mol电子
D. K2FeO4可氧化水中的H2S、NH3,生成的Fe(OH)3胶体还能吸附悬浮杂质
查看答案和解析>>
科目:高中化学 来源: 题型:
下列现象说法正确的是()
A. 红热的铁丝在氯气中燃烧产生棕色的烟雾
B. 含有氯元素的物质都呈黄绿色
C. 氢气在氯气中燃烧时火焰呈淡蓝色,在瓶口有白雾产生
D. 钠在空气里加热,先熔成小球,剧烈燃烧,产生黄色火焰,生成淡黄色固体
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作或对实验事实的叙述中,正确的是( )
A. 用氨气做喷泉实验主要是利用氨气的水溶液呈碱性这一性质
B. 向浓硫酸中缓慢加蒸馏水,以稀释浓硫酸
C. 常温下,浓硝酸可贮存于铁制或铝制容器中
D. 向溶液中加入硝酸酸化的BaCl2溶液,产生白色沉淀,说明一定含有SO42﹣
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com