

分析 (1)A装置中温度计测定反应液的温度,B装置中温度计测定馏分的温度;
(2)C装置做乙醇与乙酸的酯化反应实验,需要连接F装置吸收乙醇,中和乙酸,降低乙酸乙酯溶解度,防止倒吸;C装置液体加热沸腾需要加入碎瓷片/沸石防止暴沸;
(3)做乙醇氧化成乙醛的实验,需要提供乙醇蒸气和氧气在催化剂作用下氧化反应生成乙醛,冷却得到液体乙醛.
解答 解:(1)①用电石制乙炔,不需要加热;
②用乙醇与浓硫酸混和制乙烯,需要测定反应液的温度为170℃;
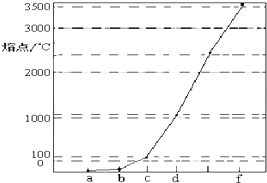
③实验室蒸馏石油,测定馏分的温度,
④制硝基苯,需要水浴加热,温度计测水的温度;
⑤制乙酸乙酯直接加热,不需要测定温度;
⑥酯的水解,可直接加热,不需要测定温度,
则可用装置A制取的是②;可用装置B制取的是③,
故答案为:②;③;
(2)若用C装置做乙醇与乙酸的酯化反应实验,则还需连接的装置是F,该装置中应加入的试剂是饱和碳酸钠溶液.从实验安全角度考虑,C装置试管中除加入反应液外,还需加入的固体物质是碎瓷片或沸石,防止暴沸,
故答案为:F;饱和碳酸钠溶液;碎瓷片或沸石;
(3)做乙醇氧化成乙醛的实验,需要提供乙醇蒸气和氧气在催化剂作用下氧化反应生成乙醛,反应的化学方程式为2CH3CH2OH+O2 $→_{△}^{Cu}$2CH3CHO+2H2O,冷却得到液体乙醛,装置连接为C、D、E,
故答案为:C、D、E.
点评 本题考查了实验制备和物质性质验证的方法,为高频考点,侧重于学生的分析能力和实验能力的考查,掌握乙醇催化氧化原理和产物性质是解题关键,题目难度中等.


 全能测控一本好卷系列答案
全能测控一本好卷系列答案 发散思维新课堂系列答案
发散思维新课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 在使石蕊试液变红的溶液中:Na+、NH4+、NO3-、AlO2- | |
| B. | 在含有较多Al3+的溶液中:Na+、K+、SO42-、HCO3- | |
| C. | 室温下,在$\frac{c({H}^{+})}{c(O{H}^{-})}$=1×10-12的溶液中:K+、I-、Cl-、HS- | |
| D. | 在无色溶液中:SO42-、Cl-、NH4+、Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在同温同压下,相同体积的任何气体含有相同数目的原子 | |
| B. | 氧化还原反应的本质是有电子转移 | |
| C. | Na2SO4溶液在电流作用下电离出Na+与SO42-而导电 | |
| D. | NaCl固体不导电,所以NaCl不是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
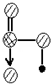 请简要说明该物质易溶于水的原因
请简要说明该物质易溶于水的原因查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ,关于该有机物下列叙述正确的是( )
,关于该有机物下列叙述正确的是( )| A. | 不能使酸性KMnO4溶液褪色 | |
| B. | 不能使溴水褪色 | |
| C. | 在加热和催化剂作用下,最多能和3mol H2反应 | |
| D. | 一定条件下,不能和NaOH醇溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
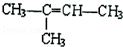 的名称是2-甲基-2-丁烯
的名称是2-甲基-2-丁烯 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
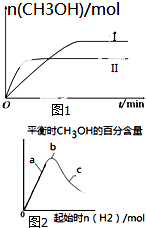 研究CO2的利用对促进低碳社会的构建具有重要的意义.
研究CO2的利用对促进低碳社会的构建具有重要的意义.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 甲~庚元素在周期表中的相对位置如图,己的最高氧化物对应水化物有强脱水性,甲和丁在同一周期,甲原子最外层与最内层具有相同电子数.下列判断正确的是( )
甲~庚元素在周期表中的相对位置如图,己的最高氧化物对应水化物有强脱水性,甲和丁在同一周期,甲原子最外层与最内层具有相同电子数.下列判断正确的是( )| A. | 丙与戊的原子序数相差27 | |
| B. | 气态氢化物的稳定性:庚<己<戊 | |
| C. | 丁的最高价氧化物可用于制造光导纤维 | |
| D. | 常温下,甲和乙的单质均能与水剧烈反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 利用风能发电、采取节能技术、使用太阳能热水器均有利于减少二氧化碳排放 | |
| B. | 生活垃圾焚烧发电也会产生有毒有害物质 | |
| C. | 丁达尔现象可用于区别溶液与胶体,云、雾、淀粉溶液均能产生丁达尔现象 | |
| D. | 硅酸钠溶液的保存和碱溶液一样,存放在橡胶塞密封的广口试剂瓶中 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com