
| A.热稳定性:HF>HCl>HBr>HI |
| B.微粒的半径:Cl->Na+>Mg2+>Al3+ |
| C.电离程度(同温度同浓度溶液中):HCl>CH3COOH>NaHCO3 |
| D.分散质粒子的直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液 |
科目:高中化学 来源:不详 题型:单选题
| A.已知Sr元素位于第五周期IIA族,故Sr(OH)2碱性比Mg(OH)2弱 |
| B.己知As元素位于第四周期VA族,故NH3比 AsH3稳定 |
| C.元素周期表分为7个主族、7个副族、1个0族、1个VIII族,共18个纵行 |
| D.副族元素中没有非金属元素 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| | | | ||||||
| | | | | | | A | B | |
| C | | | D | E | F | G] | | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Na2O2中既含离子键,又含非极性键,阴阳离子个数之比为1:1 |
| B.第IA族又名碱金属族 |
| C.1H35Cl、2H37Cl两种气体的化学性质相同,但物理性质可能不同 |
| D.由于还原性:S2->Cl-,故硫元素的非金属性强于氯元素 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
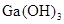 是否为两性氢氧化物,设计实验时,需要选用的试剂有GaCl3溶液、________和________。
是否为两性氢氧化物,设计实验时,需要选用的试剂有GaCl3溶液、________和________。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| X | | Z |
| | Y | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.热稳定性:H2O>HF>H2S | B.沸点:HF>HCl>HBr |
| C.密度:CH3CH2CH2Cl>CH3CH2Cl>CH3Cl | D.氧化性:Fe3+>Cu2+>H+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.通过电解熔融的Z、Q形成的化合物可制取Z单质 |
| B.原子半径的大小顺序为W>Q>Z>X>Y |
| C.元素Y的最高正化合价为+6 |
| D.XQ3分子中,中心原子是sp3杂化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com