
����Ŀ�������̼����(Na2CS3)��ũҵ������ɱ������ɱ�߳�����ڹ�ҵ�����ڴ�����ˮ�е��ؽ������ӡ�ij��ѧ��ȤС���Na2CS3��һЩ���ʽ���̽�����ش��������⣺
(1)���Թ��м������������̼������Ʒ����ˮ�ܽ⣬�����ҺpH=10���ɴ˿�֪H2CS3��______(����ǿ����������)�ᡣ�����Һ�еμ�����KMnO4��Һ����ɫ��ȥ���ɴ�˵��Na2CS3����______�ԡ�(������ԭ������������)��
(2)Ϊ�˲ⶨijNa2CS3��Һ��Ũ�ȣ�����ͼװ�ý���ʵ�顣��35.0 mL��Na2CS3��Һ��������װ��A��������ƿ�У�������d�Ļ�������������ϡ���ᣬ�رջ�����
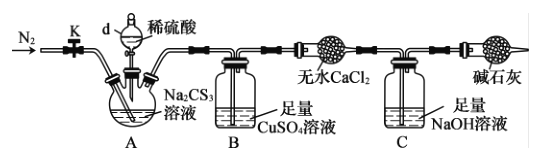
��֪��CS32- +2H+==CS2 +H2S����CS2 ��H2S���ж���CS2������ˮ���е�46��C����CO2ijЩ�������ƣ���NaOH��������Na2COS2��H2O��
������d��������__________����Ӧ��ʼʱ��Ҫ��ͨ��һ��ʱ��N2��������Ϊ______��
��B�з�����Ӧ�����ӷ���ʽ��________��
�۷�Ӧ��������K���ٻ���ͨ����N2(����60��C)һ��ʱ�䣬��Ŀ����__________��
��Ϊ�˼����Na2CS3��Һ��Ũ�ȣ��ɲⶨB�����ɳ���������������B�г�������֮ǰ����Ҫ���е�ʵ����������ǹ��ˡ�_____��________����B�����ɳ���������Ϊ8.4g�����Na2CS3��Һ�����ʵ���Ũ����___________��
������Ӧ������ͨ��N2��Ϊͨ�ȿ���(����60��C)��ͨ���ⶨC����Һ����������ֵ�����������̼������Һ��Ũ��ʱ������ֵ______(����ƫ������ƫ����������Ӱ����)��
���𰸡��� ��ԭ ��Һ©�� �ų�װ���еĿ��� Cu2++H2S=CuS��+2H+ ��װ���е�H2Sȫ������B�б�������գ���װ���е�CS2ȫ������C�б�������� ϴ�� ���� 2.5mol/L ƫ��
��������
��1����������ˮ��ԭ�������Ը�����ص�ǿ�����Է�����𣻣�2������ʵ��Ŀ�ġ�ʵ��װ�ü���������ɺ�H2S�Ļ�ԭ�Է���������ù�ϵʽ��������ؼ��㡣
��1�����Թ��м������������̼������Ʒ����ˮ�ܽ⣬����ҺpH=10����Һ�Լ��ԣ�˵����Ϊǿ�������Σ������Һ�еμ�����KMnO4��Һ����ɫ��ȥ֤���α���������������ԭ��Ӧ��Na2CS3���л�ԭ�ԣ��ʴ�Ϊ��������ԭ�ԣ�
��2�������������������������d�����Ʒ�Һ©����N2��ѧ���ʱȽ��ȶ���Ϊ�˷�ֹ������������H2S���������Է�Ӧ��ʼʱ��Ҫ��ͨ��һ��ʱ��N2���ų�װ���еĿ������ʴ�Ϊ����Һ©�����ų�װ���еĿ�����
��B�з�����Ӧ������ͭ�����ⷴӦ���ɺ�ɫ��ͭ��������Ӧ�����ӷ���ʽΪ��Cu2++H2S=CuS��+2H+���ʴ�Ϊ��Cu2++H2S=CuS��+2H+��
����Ӧ���������K���ٻ���ͨ����N2һ��ʱ�䣬��Ŀ���ǣ���װ���е�H2Sȫ������B�б�������գ���װ���е�CS2ȫ������C�б�������գ��ʴ�Ϊ����װ���е�H2Sȫ������B�б�������գ���װ���е�CS2ȫ������C�б�������գ�
������B�г�������֮ǰ��Ҫ���е�ʵ����������ǣ����ˡ�ϴ�ӡ������B�����ɳ���������Ϊ8.4g�����ʵ���=![]() �����ʵ����غ㣬CS32-+2H+=CS2+H2S����Cu2++H2S=CuS��+2H+���õ�������ϵ��CS32H2SCuS�� n��Na2CS3��= n��CuS��=0.0875mol����35.0mL�����̼������Һ�����ʵ���Ũ��
�����ʵ����غ㣬CS32-+2H+=CS2+H2S����Cu2++H2S=CuS��+2H+���õ�������ϵ��CS32H2SCuS�� n��Na2CS3��= n��CuS��=0.0875mol����35.0mL�����̼������Һ�����ʵ���Ũ��![]() ���ʴ�Ϊ��ϴ�ӡ���� 2.5mol/L��
���ʴ�Ϊ��ϴ�ӡ���� 2.5mol/L��
������Ӧ������ͨ��N2��Ϊͨ�ȿ�����ͨ���ⶨC����Һ����������ֵ�����������̼������Һ��Ũ��ʱ��C�г����ն���̼�������տ����ж�����̼����Һ��������ƫ����õ���ҺŨ�Ȼ�ƫ�ߣ��ʴ�Ϊ��ƫ�ߡ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ⶨijNaOH��Һ�����ʵ���Ũ�ȣ�����0.1000 mol��L��1��HCl����Һ�����к͵ζ����ü�����ָʾ��������ش��������⣺
(1)�ζ�ʱ��ʢװ����NaOH��Һ����������Ϊ_______________��
(2)ʢװ���������������Ϊ________________��
(3)�ζ����յ����ɫ�仯Ϊ_______________________________________________________��
(4)����ѧ����ʵ������У���¼�ζ�ǰ�ζ�����Һ�����Ϊ0.50 mL���ζ���Һ����ͼ�����ʱ���ı���Һ�����Ϊ____________��
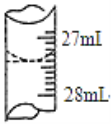
(5)������Щ������ʹ�ⶨ���ƫ��_________������ĸ����
A����ƿ������ˮϴ�������ô���Һ��ϴ
B����ʽ�ζ���������ˮϴ�������ñ�Һ��ϴ
C���ζ�ǰ��ʽ�ζ��ܼ������δ�ų����ζ���������ʧ
D���ζ�ǰ������ȷ���ζ����ӵζ��ܶ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ף���ͼ��ʾ��������ԭ�Ӷ��ﵽ�� 8�����ȶ��ṹ��X��Y��Z��W��ԭ��������������Ķ���������Ԫ�أ�ԭ�Ӱ뾶:r��w��> r��X��> r��Y�� > r��Z��������˵����ȷ���ǣ� ��
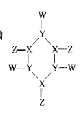
A.YZ����������������
B.Ԫ�صķǽ�����ǿ��:Y>Z
C.X������⻯���Ӧ��ˮ������ǿ��
D.Y������⻯������W���⻯�ﷴӦ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��AgBr��AgCl�����ܣ���AgCl��AgBr�ı�����Һ�������ϣ��ټ���������ŨAgNO3��Һ�������ķ�ӦΪ
A. ֻ��AgBr�������� B. AgCl��AgBr������������
C. AgCl��AgBr�������У�����AgCl����Ϊ�� D. AgCl��AgBr�������У�����AgBr����Ϊ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����顢��ϩ���л����ڹ�ҵ���й㷺��Ӧ�á��ش��������⣺
(1)�����л�����ϩ���ʣ�ʵ��������ͼװ�ó��ӣ��õ������ı��顣���Լ�aΪ���Ը��������Һ�����Լ�b��c�����Ʒֱ�Ϊ______��_______��
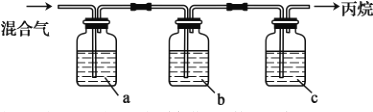
(2)��ͼΪ�������ʵ������ܺͼ����ת����������ϵ����������ֽ�õ�ʯī(C)���������Ȼ�ѧ����ʽΪ_________��

(3)�������ݻ���Ϊ1 L�ĺ����ܱ��������Բ�ͬ����̼��[n(H2)/n(CO2)]����2 mol H2��һ������CO2����һ�������·�����Ӧ2CO2(g) +6H2(g)![]() C2 H4(g) +4H2O(g) ��H��CO2��ƽ��ת������(CO2)���¶ȵĹ�ϵ��ͼ��ʾ��
C2 H4(g) +4H2O(g) ��H��CO2��ƽ��ת������(CO2)���¶ȵĹ�ϵ��ͼ��ʾ��
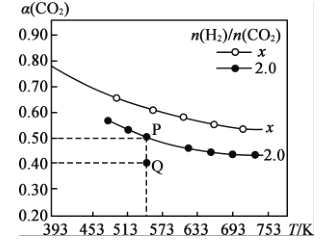
�ٸ÷�Ӧ��H___________(����>����<"����=")0���жϵ�������__________��
������̼��Ϊ2.0ʱ��Q��v(��)_______P��v(��)(����>����<"����=��)��
����̼�ȣ�x_____2. 0(����>����<������=��)��
��Q���Ӧ�¶��£��÷�Ӧƽ�ⳣ��K=_______L3�� mol-3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧѧϰС���������ʵ�顣
��̽����Ӧ���ʵ�Ӱ�����ء���������µķ�������¼ʵ����(������Һ�������� ��)����ѡ�Լ���������0.20mol/LH2C2O4 ��Һ��0.010mol/L KMnO4 ��Һ�����ԣ�������ˮ�� �Թܡ���Ͳ�����������ˮԡ��
��1������ʵ���٢���̽�� �Ի�ѧ��Ӧ���ʵ�Ӱ�죻������ʵ���ڢ���̽��Ũ�ȶԻ�ѧ��Ӧ���ʵ�Ӱ�죬�� a Ϊ ������ʵ����Ҫ����������������� ����������Ӧ��д ��
���ⶨ H2C2O4��xH2O �� x ֵ�� ��֪��M��H2C2O4��=90g/mol
��ȡ 1.260 g �����ᾧ�壬�������Ƴ� 100.00 mL ˮ��ҺΪ����Һ��
��ȡ 25.00 mL ����Һ������ƿ�У��ټ����ʵ�ϡ H2SO4
����Ũ��Ϊ 0.05000 mol��L-1 �� KMnO ����Һ���еζ���
��2����д����ζ��йط�Ӧ�����ӷ���ʽ
��3��ijѧ���ĵζ���ʽ���гֲ�����ȥ�����£���������� ��ѡ�� a��b����


��4������ͼ��֪���� KMnO4 ��Һ���Ϊ mL��
��5���ζ��������۾�Ӧע��_________________��
��6��ͨ���������ݣ���� x= ���Ա� KMnO4 ��Һ�ζ���Ʒ��Һ��Ũ�ȣ�δ�� �� KMnO4 ��Һ��ϴ�ζ��ܣ�����ʵ���� ��ƫ��ƫС��û��Ӱ�죩��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ����˹������(��ͼ��)�ܹ���ú������еļ���ﵽһ��Ũ��ʱ��ͨ����������ʾ����������˹�����ǹ���ԭ������ȼ�ϵ�صĹ���ԭ������װ����ͼ����ʾ�����еĹ���������Y2O3��Na2O��O2�����������������ƶ���
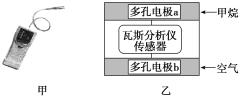
�����й�������ȷ����(����)
A.��˹�����ǹ���ʱ��������·�е����ɵ缫b����缫a
B.�缫b��������O2���ɵ缫a����缫b
C.�缫a�ķ�ӦʽΪCH4��5O2����8e��=CO32����2H2O
D.��������������1 mol O2��ͨ��ʱ������ת��4 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���춡ϩ�ڴ����������ܷ����Ӿ۷�Ӧ��
(1)д���춡ϩ�ۺϳɵĸ߷��ӻ�����Ľṹ��ʽ��________��
(2)��һ�������£��������춡ϩ֮��Ҳ�ܷ����Ӿ۷�Ӧ���������ֶ�����A��B��A��B�ڴ��������¼�����ܵõ�2��2��4����������C����д��A��B��C�Ľṹ��ʽ��____________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ȼ�ѧ����ʽ��д��ȷ���ǣ�
A.2SO2+O2![]() 2SO3 ��H=-196.6 kJ��mol-1
2SO3 ��H=-196.6 kJ��mol-1
B.H2(g)+ ![]() O2(g)=H2O(l) ��H=-285.5 kJ��mol-1
O2(g)=H2O(l) ��H=-285.5 kJ��mol-1
C.2H2(g)+O2(g)=2H2O(l) ��H=-571.6 kJ
D.C(s)+O2(g)=CO2(g) ��H=+393.5 kJ��mol-1
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com