
【题目】按以下装置图进行实验,填写有关现象及化学方程式。

(1)A中现象是____________________,
(2)B中浓硫酸的作用是_______________
(3)C中发生反应的化学方程式为______________,
(4)D中现象是_______________;反应的离子方程式是__________________________,
E中收集的气体是____________。
【答案】固体质量减轻、试管内壁有无色液滴除去二氧化碳中水蒸气或干燥气体或吸收水蒸汽2Na2O2+2CO2=2Na2CO3+O2澄清石灰水变浑浊CO2 + Ca2+ +2OH-=CaCO3↓ + H2O氧气/O2
【解析】
碳酸氢钠受热分解生成碳酸钠和水和二氧化碳,浓硫酸吸收水蒸气,过氧化钠和二氧化碳反应生成碳酸钠和氧气,澄清石灰水吸收剩余的二氧化碳,最后用排水收集氧气。
(1)A中碳酸氢钠受热分解生成碳酸钠和水和二氧化碳,所以现象为固体质量减轻、试管内壁有无色液滴;(2)浓硫酸的作用是除去二氧化碳中水蒸气或干燥气体或吸收水蒸汽;(3).过氧化钠和二氧化碳反应生成碳酸钠和氧气,方程式为 2Na2O2+2CO2=2Na2CO3+O2 ; (4) 澄清石灰水吸收二氧化碳,溶液变浑浊;氢氧化钙和二氧化碳反应生成碳酸钙和水,离子方程式为:CO2 + Ca2+ +2OH-=CaCO3↓ + H2O; (6)E中收集的气体为氧气。


 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是
A. 氯气与碘化钾溶液反应:Cl2 + I- = Cl- + I2
B. 醋酸除去水垢:2H+ + CaCO3 = Ca2+ + CO2↑ + H2O
C. 铜和浓硝酸反应:Cu + 4H+ + 2NO![]() = Cu2+ + 2NO2↑ + 2H2O
= Cu2+ + 2NO2↑ + 2H2O
D. 二氧化锰与浓盐酸反应:MnO2 + 4H+ + 4Cl- ![]() Mn2+ + 2Cl2↑ + 2H2O
Mn2+ + 2Cl2↑ + 2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列物质:①氢氧化钡固体②KHSO4③HNO3④稀硫酸⑤二氧化碳气体⑥铜⑦碳酸钠粉末⑧蔗糖晶体⑨熔融氯化钠⑩CuSO4·5H2O晶体。
请用序号填空:
(1)上述状态下可导电的是___。
(2)属于电解质的是___。
(3)属于非电解质的是___。
(4)②在水溶液中的电离方程式为___,①与②以物质的量之比为1:2在溶液中反应的离子方程式为___。
(5)③与⑥可以发生如下反应:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,还原产物是___(填名称)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应Fe(s)+CO2(g)![]() FeO(s)+CO(g),在温度为973 K时,平衡常数K=1.47,在1 173 K时,K=2.15。
FeO(s)+CO(g),在温度为973 K时,平衡常数K=1.47,在1 173 K时,K=2.15。
(1)写出该反应的平衡常数表达式_____。
(2)若该反应在体积固定的密闭容器中进行,在一定条件下达到平衡状态,如果改变下列条件再达平衡后(填“增大”“减小”或“不变”):
①升高温度,CO2的平衡浓度_____,
②再通入CO2,CO2的转化率_____,
③增大容器的体积,混合气体的平均相对分子质量_____。
(3)该反应的逆反应速率随时间变化情况如图:

①从图中看到,反应在t2时达平衡,在t1时改变了某种条件,改变的条件可能是_____(填字母)。
a.升温b.增大CO2的浓度c.使用催化剂d.增压
②如果在t3时再增加CO2的量,t4时反应又处于新平衡状态,请在图上画出t3~t5时间段的v(逆)变化曲线_____。
(4)能判断该反应达到平衡的依据是_____。
A.容器内压强不变了 B.c(CO)不变了 C.v正(CO2)=v逆(CO) D.c(CO2)=c(CO)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】本题为选做题,包括A、B两题。选学《化学与生活》模块的考生答A题,选学《有机化学基础》模块的考生答B题,每位考生只可选做1题。若两题都作答,则以A题计分。
A. 《化学与生活》

(1) 营养均衡是保证健康的重要方面。某种食品的配料标签如图所示,根据该食品的配料填空。
①该食品配料中,富含糖类的物质是____。
②该食品配料中,苯甲酸钠的作用是____。
③该食品配料中,碳酸氢钠的作用是____。
(2) 材料是社会经济发展的物质基础。
①钢铁在生活中的应用十分广泛,在潮湿的空气中容易发生____腐蚀。
②普通玻璃的主要成分是Na2SiO3、CaSiO3和 ____(填化学式)。____(填化学式)对玻璃有腐蚀作用,可用于在玻璃仪器上标注刻度及文字。
③聚氯乙烯塑料的结构简式为________,玻璃钢属于________(填“无机非金属材料”“功能高分子材料”或“复合材料”)。
(3)化学与技术的发展是解决环境问题的有效路径。
①减少燃煤产生气体SO2的排放,能够有效控制______(填“硝酸型酸雨”“硫酸型酸雨”或“光化学烟雾”)的形成;向燃煤中加入适量的____(填名称)可减少燃煤烟气中的SO2排放。
②燃煤产生的CO2用氨水吸收可得到氮肥碳铵(NH4HCO3),写出该反应的化学方程式______________。工业上通常采用沉淀法除去废水中的重金属离子,需要控制废水的_____使重金属离子以氢氧化物的形式沉淀出来。
③工业上采用将CO在500 ℃、铝矾催化作用下还原SO2,反应得到两种产物,其中一种产物在常温下是固体。该项技术可大大降低燃煤烟气中SO2的含量,反应的化学方程式为____________________。
B.《有机化学基础》
(1) 有机物的结构决定了其所具有的性质。
①下列有机物不溶于水的是____(填字母)。
a. 乙醛 b. 乙醇 c. 乙酸乙酯
②下列化合物中,不能与新制氢氧化铜悬浊液反应的是____(填字母)。
a. 福尔马林 b. 乙烯 c. 乙酸
③下列试剂中,可用于鉴别苯和甲苯的是____(填字母)。
a. 水 b. 溴水 c. 酸性KMnO4溶液
(2)水杨酸是一种柳树皮提取物,是天然的消炎药,其结构为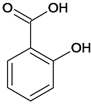 。
。
①水杨酸苯环上的一氯代物有____种。
②水杨酸需密闭保存,其原因是__________。
③水杨酸与足量NaHCO3溶液反应,所得有机产物的结构简式为______。
(3)化合物C是一种医药中间体,由甲苯制备化合物C的路线如下:
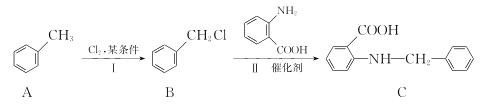
①A→B的反应类型是____。
②B分子中化学环境不同的氢原子有____种。
③D是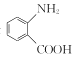 的一种同分异构体,D分子中只有一种官能团,苯环上的一氯代物有2种。则D的结构简式为________。
的一种同分异构体,D分子中只有一种官能团,苯环上的一氯代物有2种。则D的结构简式为________。
④B→C的反应中能生成化合物E,E和C的相对分子质量相同,写出生成化合物E的化学方程式_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某Na2CO3、NaAlO2的混合溶液中逐滴加入1molL1的盐酸,测得溶液中的CO32、HCO3、AlO2、Al3+的物质的量与加入盐酸溶液的体积变化关系如图所示。则下列说法正确的是( )(已知:H2CO3的电离平衡常数K1 = 4.3×107,K2 = 5.6×1011;Al(OH)3的酸式电离平衡常数K=6.3×1013)

A. a曲线表示的离子方程式为:AlO2+4H+ = Al3+ + 2H2O
B. M点时生成的CO2为0.05 mol
C. 原混合溶液中的CO32与AlO2的物质的量之比为1:2
D. V1:V2=1:4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(部分产物已略去)。则W、X不可能是( )

选项 | W | X |
A | 稀硫酸 | NaAlO2溶液 |
B | 稀硝酸 | Fe |
C | CO2 | Ca(OH)2溶液 |
D | Cl2 | Fe |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列物质:①氢氧化钠固体②铜丝③氯化氢气体④稀硫酸⑤二氧化碳气体⑥氨水⑦碳酸氢钠固体⑧蔗糖晶体⑨熔融氢化钠⑩胆矾(C![]() )晶体
)晶体
(1)上述物质相应状态下可导电的是_______________________________。
(2)属于电解质的是_______________________________。
(3)属于非电解质的是_______________________________。
(4)上述状态下的电解质不能导电的是_______________________________。
(5)⑦溶于水后的电离方程式是_______________________________。
(6)①和⑦混合溶于水的离子方程式是_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对于“摩尔”的理解正确的是( )
A. 1摩尔H2O质量为18g
B. 摩尔是国际科学界建议采用的一种物理量,简称摩,符号为 mol
C. 22.4LO 2 中所含氧气分子为1 摩尔
D. 1mol 氧含 6.02×10 23 个O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com