
【题目】在一个固定体积的密闭容器中,加入4mol A和2mol B发生反应:2A(g)+B(g)![]() 3C(g)+D(g)达到平衡时,C的浓度为Wmol/L,若维持容器体积和温度不变,按下列四种方法改变起始物质,达到平衡后,C的浓度仍为Wmol/L的是( )
3C(g)+D(g)达到平衡时,C的浓度为Wmol/L,若维持容器体积和温度不变,按下列四种方法改变起始物质,达到平衡后,C的浓度仍为Wmol/L的是( )
A.8mol A+4mol B B.2mol A+1mol B
C.6mol C+2mol D+2mol B D.6mol C+2mol D
【答案】D
【解析】
试题分析:恒温恒容下,不同途径的该可逆反应达到平衡后,C的浓度仍为W mol/L,说明与原平衡为等效平衡,则根据
2A(g)+B(g)![]() 3C(g)+D(g)
3C(g)+D(g)
4mol 2mol 6mol 2mol
可知,按化学计量数转化到左边,一定满足:n(A)=4mol,n(B)=2mol。
A.8mol A+4mol B与4molA+2molB与不相等,在温度、体积不变的情况下不是相同平衡状态,A错误;B.开始加入2mol A+1mol B与4molA+2molB与不相等,在温度、体积不变的情况下不是相同平衡状态,B错误;C.6mol C+2mol D+2mol B与相当于4molA、4molB,与4molA、2molB不相等,在温度、体积不变的情况下不是相同平衡状态,C错误;D.6molC+2molD相当于4molA+2molB,与4molA+2molB相等,在温度、体积不变的情况下是相同平衡状态,达到平衡后,C的浓度仍为Wmol/L,D正确;答案选D。


科目:高中化学 来源: 题型:
【题目】化学与人类生产、生活、社会可持续发展密切相关,下列说法正确的是( )
A. 凡含有添加剂的食物对人体健康均有害,不宜食用
B. “霾尘积聚难见路人”,雾霾所形成的气溶胶有丁达尔效应
C. 人体缺乏铁元素,可以补充硫酸亚铁,且多多益善
D. “青蒿一握,以水二升渍,绞取汁”,屠呦呦对青蒿素的提取属于化学变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温恒容密闭容器中,能说明反应:2N02(g)![]() 2NO(g)+02(g)达到平衡状态的是 ( )
2NO(g)+02(g)达到平衡状态的是 ( )
①单位时间内生成nmol O2的同时生成2nmol NO2;②单位时间内生成nmol O2的同时生成2nmol N0;③混合气体的颜色不再改变;④混合气体的密度不再改变的状态;⑤混合气体的平均相对分子质量不再改变的状态。
A.①③⑤ B.②④⑤ C.①③④ D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.需要加热的反应一定是吸热反应
B.所有的化学反应都有能量变化
C.所有的放热反应都可以在常温常压下自发进行
D.核能作为一种反应热,是理想的新能源
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究乙烯与溴的加成反应,甲同学设计并进行如下实验:先取一定量的工业用乙烯气体(在储气瓶中),使气体通入溴水中,发现溶液褪色,即证明乙烯与溴水发生了加成反应;乙同学发现在甲同学的实验中,褪色后的溶液里有少许淡黄色浑浊物质,推测在工业上制得的乙烯中还可能含有少量还原性气体杂质,由此他提出必须先除去杂质,然后乙烯再与溴水反应。
请你回答下列问题。
(1)甲同学的实验中与乙烯有关的化学方程式为:______________________。
(2)甲同学设计的实验________(填“能”或“不能”)验证乙烯与溴发生加成反应,其理由是________。(填写序号)
①使溴水褪色的反应未必是加成反应
②使溴水褪色的反应就是加成反应
③使溴水褪色的物质未必是乙烯
④使溴水褪色的物质就是乙烯
(3)乙同学推测此乙烯中必定含有一种杂质气体是________,它与溴水反应的化学方程式是_______________。在验证过程中必须全部除去。除去该杂质的试剂可用________。
(4)为验证这一反应是加成反应而不是取代反应,丙同学提出可用pH试纸来测试反应后溶液的酸性,理由是_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂被誉为“金属味精”,以LiCoO2为正极材料的锂离子电池已被广泛用作便携式电源。工业上常以β-锂辉矿(主要成分为LiAlSi2O6,还含有FeO、MgO、CaO等杂质)为原料来制取金属锂。其中一种工艺流程如图所示:
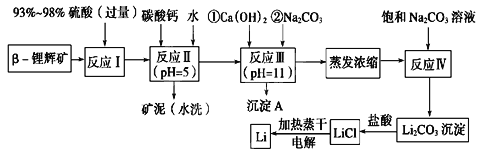
已知:①部分金属氢氧化物开始沉淀和完全沉淀时的pH如下表:
氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
开始沉淀pH | 2.7 | 3.7 | 9.6 |
完全沉淀pH | 3.7 | 4.7 | 11 |
②Li2CO3在不同温度下的溶解度如下表:
温度/℃ | 0 | 10 | 20 | 50 | 75 | 100 |
Li2CO3的溶解度/g | 1.539 | 1.406 | 1.329 | 1.181 | 0.866 | 0.728 |
请回答下列问题:
(1)用氧化物形式表示LiAlSi2O6的组成:________________________。
(2)反应Ⅱ加入碳酸钙的作用是___________________。
(3)流程中两次使用碳酸钠溶液,请说明前后两次使用中浓度不同的原因:______________。
(4)洗涤所得Li2CO3沉淀要使用________(填“热水”或“冷水”),你选择的理由是________________。
(5)将盐酸与Li2CO3完全反应后的溶液,加热蒸干得到固体,再将其熔融电解生产锂。电解时产生的氯气中会混有少量氧气,原因是:__________________________。
(6)下列关于金属锂及碱金属的说法正确的是___________(填序号)。
A.锂是碱金属,其熔点高于钠 B.根据对角线原则,氢氧化锂是强碱
C.金属锂的氧化物形式十分复杂 D.碱金属中密度最小的是锂,其次是钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有稀硫酸、纯碱、二氧化碳、铜片、食盐、生石灰、铁片和木炭粉8种物质。
(1)在这8种物质中,属于电解质的有____________________
(用相应的化学式表示,下同)。
(2)这8种物质中的某5种存在下面的相互关系,选择适当的物质填入①~⑤,使有连线的两种物质能发生反应,并回答下列问题。

①它们的化学式分别为:①______________;②______________;③____________;④________________;⑤______________。
②如果连线对应的反应分别用A、B、C、D、E表示。五个反应中属于氧化还原反应的有________________个;反应A的离子方程式为_____________,反应B________________(填“属于”或“不属于”)离子反应,反应D的化学方程式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在密闭容器中发生如下反应:N2O4(g)![]() 2NO2(g)△H>0,反应达到平衡时,下列说法不正确的是( )
2NO2(g)△H>0,反应达到平衡时,下列说法不正确的是( )
A.若缩小容器的体积,则容器中气体的颜色先变深后又变浅,且比原平衡颜色深
B.若压强不变,向容器中再加入一定量的N2O4,再次达到平衡时各种物质的百分含量不变
C.若体积不变,向容器中再加入一定量的N2O4,平衡向逆反应方向移动,再次平衡时N2O4的转化率将降低
D.若体积不变,升高温度,再次平衡时体系颜色加深
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列情况没有发生蛋白质变性的是( )
A.用福尔马林浸动物标本 B.用蘸有质量分数为75%的酒精棉花球擦皮肤
C.用紫外线光灯照射病房 D.淀粉和淀粉酶混合后微热
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com