
��20g Ba��OH��2��8H2O������10 g NH4Cl����һ�����С�ձ��У����ձ����ڵ���3��4��ˮ�IJ���Ƭ�ϣ��ò�����Ѹ�ٽ��衣������˵����ȷ����
| A��ʵ���в������������Ǽ��ٹ����ܽ� |
| B������Ƭ�Ͻ������С�ձ�ճ��һ��˵���÷�Ӧ�Ƿ��ȷ�Ӧ |
| C����ȡ��Ӧ�������Ķ��ٻ�Ӱ�췴Ӧ�����ȣ����Ƿ��� |
| D���÷�Ӧ�У���Ӧ���������С��������������� |
 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
����̼���á����Ե��ܺġ�����Ⱦ�����ŷ�Ϊ�����Ŀɳ�����չ����ģʽ������˵���롰��̼���á������ϵ���
| A�������з������л��ܼ����ˮ��Ϊ��ȡ�� |
| B����ǿ��ú��ʯ�͡���Ȼ�����ۺ����õ��о������ȼ�ϵ������� |
| C������CO2�ϳɾ�̼������ɽ������ϣ�ʵ�֡�̼����ѭ������ |
| D��������Ҵ���ȼ���ȷֱ���891��0 kJ��mol��1��1366��8 kJ��mol��1�����ü��������̼�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�����뻯ѧ��Ӧ�����仯��ص�������ȷ����
| A��������������һ�����ڷ�Ӧ�������� |
| B�����ȷ�Ӧ�ķ�Ӧ�������Ǵ������ȷ�Ӧ�ķ�Ӧ���� |
| C����˹���ɣ��ɼ���ijЩ����ֱ�Ӳ����ķ�Ӧ���ʱ� |
| D��ͬ��ͬѹ�£�H2(g)+Cl2(g)��2HCl(g)�ڹ��պ͵�ȼ�����ġ�H��ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�����������ɷ������·�Ӧ��P4+5O2�TP4O10����֪�������л�ѧ����Ҫ���յ������ֱ�Ϊ��P-P��a kJ?mol-1��P-O��b kJ?mol-1��P��O��c kJ?mol-1��O��O��d kJ?mol-1������ͼʾ�ķ��ӽṹ���й����ݹ���÷�Ӧ�ġ�H��������ȷ����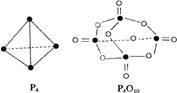
A��6a+5d-4c-12b��kJ?mol-1 B����4c+12b-6a-5d��kJ?mol-1
C����4c+12b-4a-5d��kJ?mol-1 D����4a+5d-4c-12b��kJ?mol-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��֪��N2(g)+3H2(g) 2NH3(g)��H=" ��92" kJ/mol������������±���һ�������£������Ϊ1L���ܱ������м���1molN2��3molH2��ַ�Ӧ���ų�����Q1kJ������˵����ȷ���ǣ� ��
2NH3(g)��H=" ��92" kJ/mol������������±���һ�������£������Ϊ1L���ܱ������м���1molN2��3molH2��ַ�Ӧ���ų�����Q1kJ������˵����ȷ���ǣ� ��
| | H2(g) | N2(g) | NH3(g) |
| 1mol�����еĻ�ѧ���γ�ʱҪ�ͷų�������/kJ | 436 | 946 | a |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
����̼���ã����ܼ��š���21�������羭�÷�չ����˼·����������֮��㣵��ǣ� ��
| A������ˮ�ܡ����ܡ�̫���ܡ������ܡ����ܵ�����Դ������ʹ��ú��ʯ�͵Ȼ�ʯȼ�� |
| B��������չũ���������������Ľո�ת��Ϊ����Ч����Դ |
| C����������ú��ʯ�ͺ���Ȼ���������㾭�÷�չ����Ҫ |
| D��������չ����Դ���������϶����������綯�����ȣ��Լ���̼������������ŷ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��֪��2H2(g) + O2(g)��2H2O(l) ��H����571��6 kJ��mol��1
2H2(g) + O2(g)��2H2O(g�� ��H����483��6kJ��mol��1
2CH3OH(l)��3O2(g)===2CO2(g)��4H2O(l) ��H����1452 kJ��mol��1
����˵����ȷ����
| A��H2(g)��ȼ���Ȧ�H����285��8 kJ��mol��1 |
| B��1molH2O(l)���1mo1H2O(g)������88kJ���� |
| C��3H2(g)��CO2(g)=CH3OH(l)��H2O(l)��H����135��9 kJ��mol��1 |
| D������Ѱ���������ʹH2O�ֽ⣬ͬʱ�ų����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
������Ⱦ�����ѳ�Ӱ�컷������Ҫ���أ�����������2CO(g)��SO2(g) 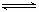 2 CO2 (g) ��S (g)����H=" +8.0" kJ/mol�ķ�Ӧ��������Ⱦ��ʹ�����ʹ����ӿ췴Ӧ�������йظ÷�Ӧ���̵������仯ʾ��ͼ��ȷ����
2 CO2 (g) ��S (g)����H=" +8.0" kJ/mol�ķ�Ӧ��������Ⱦ��ʹ�����ʹ����ӿ췴Ӧ�������йظ÷�Ӧ���̵������仯ʾ��ͼ��ȷ����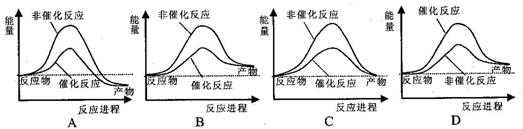
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�����й��������жϻ��ʾ������ȷ���ǣ� ��
| A�����������������������ֱ���ȫȼ�գ����߷ų��������� |
B����C(ʯī) �� C(���ʯ) Q Q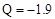 kJ����֪ʯī�Ƚ��ʯ���ȶ� kJ����֪ʯī�Ƚ��ʯ���ȶ� |
C����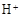 (aq) (aq) (aq) �� H2O(l) (aq) �� H2O(l) Q Q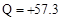 kJ����֪����1mol CH3COOH��ϡ��Һ�뺬1mol NaOH��ϡ��Һ��ϣ��ų���������57.3 kJ kJ����֪����1mol CH3COOH��ϡ��Һ�뺬1mol NaOH��ϡ��Һ��ϣ��ų���������57.3 kJ |
D��2gH2��ȫȼ������Һ̬ˮ�ų�285.8kJ������������ȼ�յ��Ȼ�ѧ����ʽΪ��2H2(g) O2(g) �� 2H2O(l) O2(g) �� 2H2O(l) Q�� Q��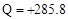 kJ kJ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com