
| A. | 2SO2(g)+O2(g)?2SO3(g);△H=-2a KJ/mol | B. | 2SO2(g)+O2(g)2?SO3(g);△H=-a KJ/mol | ||
| C. | SO2(g)+$\frac{1}{2}$O2(g)?SO3(g);△H=a KJ/mol | D. | SO2(g)+$\frac{1}{2}$O2(g)?SO3(g);△H=-2a KJ/mol |
分析 SO2在接触室中被催化氧化为SO3,已知该反应为一放热反应.现将2mol SO2、1mol O2充入一密闭容器中充分反应后,放出热量akJ,此时测得SO2的转化率为50%,物质的量为1mol.该反应是可逆反应,发生反应的二氧化硫为1mol,放热为aKJ,所以依据反应放出的热量,结合热化学方程式的书写方法来解答,注意标注物质的聚集状态.
解答 解:将2mol SO2、1mol O2充入一密闭容器中充分反应后,放出热量akJ,此时测得SO2的物质的量为1mol,说明反应是可逆反应,不能进行彻底,实际发生反应的二氧化硫为1mol,1mol二氧化硫全部反应放热aKJ,热化学方程式为:2SO2(g)+O2(g)?2SO3(g)△H=-2akJ•mol-1或SO2(g)+$\frac{1}{2}$O2(g)?SO3(g)△H=-a kJ•mol-1;
A.选项中的热化学方程式符合题意,故A正确;
B.选择中热化学方程式,焓变值应为:-2a kJ•mol-1,故B错误;
C.反应是放热反应,焓变值为负值,故C错误;
D.选择中热化学方程式,焓变值应为:-a kJ•mol-1,故D错误;
故选:A.
点评 本题考查了热化学方程式书写正误判断,明确二氧化硫与氧气反应为可逆反应,不能进行到底,熟悉热化学方程式的书写方法及注意事项是解题关键,题目难度中等.


 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案科目:高中化学 来源: 题型:选择题
| 选项 | 实验现象 | 推论 |
| A | 乙烯气体可以使溴水褪色 | 乙烯发生取代反应 |
| B | 浓硫酸电导率比较低 | 硫酸浓度大时是弱电解质 |
| C | 氨气用于喷泉实验 | 氨气极易溶于水 |
| D | 硝酸溶液使pH试纸先变红后变白 | 硝酸酸性太强不能用pH试纸检测 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 物质 | CH4 | CO2 | CO | H2 |
| 体积分数 | 0.1 | 0.1 | 0.4 | 0.4 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D | |
| 用品 |  |  |  |  |
| 主要成分 | H2O2 | Na2CO3 | Al(OH)3 | NaCl |
| 用途 | 消毒剂 | 发酵粉 | 抗酸药 | 调味品 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
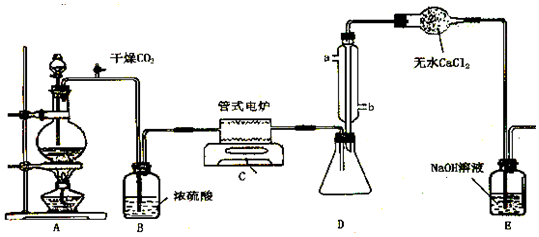
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 乙苯的同分异构体共有三种 | |
| B. | 可用Br2/CCl4鉴别乙苯和苯乙烯 | |
| C. | 乙苯和苯乙烯分子中均含有碳碳双健 | |
| D. | 乙苯和苯乙烯分子内共平面的碳原子数均为7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 淀粉和油脂的水解都是高分子生成小分子的过程 | |
| B. | 2-甲基丙烷和异丁烷互为同系物 | |
| C. |  属于取代反应 属于取代反应 | |
| D. | C3H4Cl2的链状有机物的同分异构体有5种(不考虑立体异构) |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 外加直流电源保护钢闸门时,钢闸门与电源的负极相连 | |
| B. | 铅蓄电池在放电过程中,负极质量增加,正极质量减少 | |
| C. | 锅炉中沉积的CaSO4可用饱和Na2CO3溶液浸泡,再将不溶物用稀盐酸溶解除去 | |
| D. | t℃时,恒容密闭容器中反应:NO2(g)+SO2(g)?NO(g)+SO3(g),通入少量O2,K值及SO2转化率不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | Y |
| Z | W |
| A. | 若HmXOn为强酸,则X的氢化物溶于水一定显酸性(m、n均为正整数) | |
| B. | 若四种元素均为非金属,则W的最高价氧化物对应水化物一定为强酸 | |
| C. | 若四种元素中只有一种为金属,则Y的最高价氧化物对应水化物一定为强酸 | |
| D. | 若四种元素均为金属,则Z的最高价氧化物对应水化物一定为强碱 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com