
【题目】根据下列转化关系,回答有关问题: 
(1)B、C试剂分别是、 .
(2)①、⑤和⑥反应的化学方程式分别是: ①
⑤
⑥
(3)由图示转化关系可知淀粉(填“部分水解”或“完全水解”).
【答案】
(1)NaOH;银氨溶液
(2)(C6H10O5)n+nH2O ![]() ?nC6H12O6 ;2CH3CHO+O2
?nC6H12O6 ;2CH3CHO+O2![]() ?2CH3COOH;CH3COOH+CH3CH2OH
?2CH3COOH;CH3COOH+CH3CH2OH ![]() ?CH3COOCH2CH3+H2O
?CH3COOCH2CH3+H2O
(3)部分水解
【解析】解:(1)淀粉在稀硫酸作用下水解生成葡萄糖,加Na0H溶液中和稀硫酸,使混合液呈碱性,然后加入银氨溶液,有单质银生成可检验产物葡萄糖,证明淀粉已水解,由水解后的溶液加碘水变蓝,则说明水解不完全.
所以答案是:NaOH;银氨溶液;(2)反应①淀粉在酸性条件下水解生成葡萄糖:(C6H10O5)n+nH2O ![]() nC6H12O6 ,反应②葡萄糖在水浴加热条件下发生银镜反应,反应的方程式为CH2OH(CHOH)4CHO+2[Ag(NH3)2]OH
nC6H12O6 ,反应②葡萄糖在水浴加热条件下发生银镜反应,反应的方程式为CH2OH(CHOH)4CHO+2[Ag(NH3)2]OH ![]() CH2OH(CHOH)4COONH4+2Ag↓+3NH3+H2O,反应③葡萄糖转化为乙醇的化学反应方程式为:C6H12O6
CH2OH(CHOH)4COONH4+2Ag↓+3NH3+H2O,反应③葡萄糖转化为乙醇的化学反应方程式为:C6H12O6 ![]() 2C2H5OH+2CO2↑.反应④乙醇被氧化成乙醛,乙醇中含﹣OH,能发生催化氧化,反应的化学反应方程式为:2CH3CH2OH+O2
2C2H5OH+2CO2↑.反应④乙醇被氧化成乙醛,乙醇中含﹣OH,能发生催化氧化,反应的化学反应方程式为:2CH3CH2OH+O2 ![]() 2CH3CHO+2H2O,反应⑤乙醛被氧化成乙酸,反应的方程式为:2CH3CHO+O2
2CH3CHO+2H2O,反应⑤乙醛被氧化成乙酸,反应的方程式为:2CH3CHO+O2 ![]() 2CH3COOH,反应⑥乙醇和乙酸的酯化反应,反应的方程式为:H3COOH+CH3CH2OH
2CH3COOH,反应⑥乙醇和乙酸的酯化反应,反应的方程式为:H3COOH+CH3CH2OH ![]() CH3COOCH2CH3+H2O;所以答案是:(C6H10O5)n+nH2O
CH3COOCH2CH3+H2O;所以答案是:(C6H10O5)n+nH2O ![]() nC6H12O6 ;2CH3CHO+O2
nC6H12O6 ;2CH3CHO+O2 ![]() 2CH3COOH;CH3COOH+CH3CH2OH
2CH3COOH;CH3COOH+CH3CH2OH ![]() CH3COOCH2CH3+H2O;(3)加入银氨溶液,有单质银生成可检验产物葡萄糖,证明淀粉已水解,由水解后的溶液加碘水变蓝,则说明水解不完全,所以答案是:部分水解.
CH3COOCH2CH3+H2O;(3)加入银氨溶液,有单质银生成可检验产物葡萄糖,证明淀粉已水解,由水解后的溶液加碘水变蓝,则说明水解不完全,所以答案是:部分水解.


科目:高中化学 来源: 题型:
【题目】图为浓硫酸与铜片反应的装置.请回答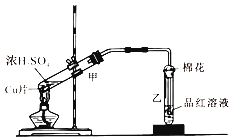
(1)浓硫酸与铜片反应的化学方程式为
(2)反应一段时间后,试管乙中品红溶液的现象是
(3)下列有关该实验的说法中,不正确的是 .
A.该反应中浓硫酸只体现酸性
B.试管乙中含有碱液的棉花,其作用是吸收过量的SO2 , 防止环境污染
C.反应一段时间后,将试管甲中的溶液缓慢倒入盛有水的烧杯,溶液显蓝色
D.含0.04mol溶质的浓硫酸与足量的铜片反应,能收集到448mL的SO2(标准状况)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胶体区别于其它分散系的特征是( )
A.胶体粒子直径在1nm~100nm之间B.胶体粒子带电荷
C.胶体粒子不能穿过半透膜D.胶体粒子能够发生布朗运动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着世界工业经济的发展、人口的剧增,全球能源紧张及世界气候面临越来越严重的问题,如何降低大气中CO2的含量及有效地开发利用CO2引起了全世界的普遍重视.
(1)如图为C及其氧化物的变化关系图,若①变化是置换反应,则其化学方程式可为; 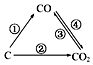
(2)把煤作为燃料可通过下列两种途径:
途径Ⅰ:C(s)+O2(g)═CO2(g)△H1<0;①
途径Ⅱ:先制成水煤气:C(s)+H2O(g)═CO(g)+H2(g)△H2>0;②
再燃烧水煤气:2CO(g)+O2(g)═2CO2(g)△H3<0,③
2H2(g)+O2(g)═2H2O(g)△H4<0.④
则途径Ⅰ放出的热量(填“大于”、“等于”或“小于”)途径Ⅱ放出的热量.
(3)甲醇是一种可再生能源,具有开发和应用的广阔前景,已知反应2CH3OH(g)CH3OCH3(g)+H2O(g)某温度下的平衡常数为400.此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
物质 | CH3OH | CH3OCH3 | H2O |
浓度/ | 0.44 | 0.6 | 0.6 |
比较此时正、逆反应速率的大小:v正v逆(填“>”“<”或“=”).
(4)生产液晶显示器的过程中使用的化学清洗剂NF3是一种温室气体,其存储能量的能力是CO2的12 000~20 000倍,在大气中的寿命可长达740年之久,以下是几种化学键的键能:
化学键 | N≡N | F﹣F | N﹣F |
键能/kJmol﹣1 | 941.7 | 154.8 | 283.0 |
则反应N2(g)+3F2(g)═2NF3(g)的△H=
(5)25℃、101kPa时,已知:
2H2O(g)═O2(g)+2H2(g)△H1
Cl2(g)+H2(g)═2HCl(g)△H2
2Cl2(g)+2H2O(g)═4HCl(g)+O2(g)△H3
则△H3与△H1和△H2间的关系正确的是
A.△H3=△H1+2△H2
B.△H3=△H1+△H2
C.△H3=△H1﹣2△H2
D.△H3=△H1﹣△H2
(6)臭氧可用于净化空气,饮用水消毒,处理工业废物和作为漂白剂.臭氧几乎可与除铂、金、铱、氟以外的所有单质反应.如6Ag(s)+O3(g)=3Ag2O(s)△H=﹣235.8kJmol﹣1 ,
已知:2Ag2O(s)=4Ag(s)+O2(g)△H=+62.2kJmol﹣1 ,
则O3转化为O2的热化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中只含有以下离子中的全部或部分: Ag+、Fe3+、Al3+、H+、SO42-、CO32-、OH-、Cl-,取该溶液做以下实验:
①观察溶液外观, 溶液有颜色;
②取少量该溶液加入Ba(NO3)2溶液, 无现象;
③取该溶液 100 mL,向其中逐滴滴加 1 mol/L的NaOH溶液至过量,生成沉淀物质的量与所加入的 NaOH 溶液的体积关系如图所示。根据实验回答以下问题:
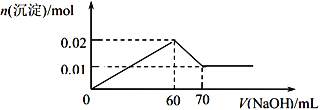
(1)检验溶液中阴离子的离子方程式为________________________________。
(2)根据以上实验推断,溶液中各离子的物质的量浓度分别为________________________________。
(3)若取以上溶液 100 mL,加入足量氨水后过滤,再将所得沉淀洗涤、灼烧,所得固体残留物的物质的量为_____________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在同温同压下,某有机物和过量Na反应得到V1 L氢气,另一份等量的该有机物和足量的NaHCO3反应得到V2 L二氧化碳,若V1=V2≠0,则该有机物可能是( )
A.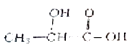
B.HOOC﹣COOH
C.HOCH2CH2OH
D.CH3COOH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com