
ij��ѧ������ȤС��Ϊ̽��ͭ��Ũ����ķ�Ӧ������ͼ��ʾ��װ�ý���ʵ�飺


��ش��������⣺
��1��B�������ռ�ʵ���в��������װ�ã���δ�����ܻ�ȫ���뽫װ��ͼ����������
��2��ʵ��������ȡ6.4gͭƬ��12mL18mol��L-1Ũ�������Բ����ƿ�й��ȣ�ֱ����Ӧֹͣ���������ƿ�л���ͭƬʣ�࣬��С���е�ͬѧ��Ϊ����һ����������ʣ�ࡣ
��д��ͭ��Ũ���ᷴӦ�Ļ�ѧ����ʽ��_________________________________________��
ʵ��������m gͭ�μ��˷�Ӧ������______mol���ᱻ��ԭ������ת����ĿΪ___��
�������Լ��У���֤����Ӧֹͣ����ƿ��������ʣ�����__________����д��ĸ��ţ���
A����������Һ B���Ȼ�����Һ C������ D��̼������Һ
��Ϊʲô��һ����������ʣ�൫δ��ʹͭƬ��ȫ�ܽ⣿����Ϊ��ԭ����
__________________________________________________________________��
��3��Ϊ�˲ⶨ������������ʵ���������ȤС�����������ʵ�鷽����
����һ����װ��A���������建��ͨ���ѳ�������װ�м�ʯ�ҵĸ���ܣ���Ӧֹͣ���ٴγ�������������������յĶ�������
����������װ��A���������建��ͨ���������������ữ�ĸ��������Һ���ټ����������Ȼ�����Һ�����ˡ�ϴ�ӡ�����Ƶó������������Ƕ�������ת��Ϊ���ᱵ������������
ʵ���ϣ�����һ����������ȡ��
����һ�����������к��� ��ʹ���������ƫ��Ҳ��������
��ʹ���������ƫС��
������������ ���Ȼ�����Һ��Ӧ��ʹ�ⶨ������������ʵ������ƫ��
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ǰ����(Li2NH)��һ�ִ��������ߡ���ȫ�ԺõĹ��崢����ϣ��䴢��ԭ���ɱ�ʾΪ��Li2NH��H2===LiNH2��LiH�������й�˵����ȷ����(����)
A��Li2NH��N�Ļ��ϼ��ǣ�1
B���÷�Ӧ��H2�������������ǻ�ԭ��
C��Li����H�������Ӱ뾶���
D���˷������ƿ�����ԭ����ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����������2014�걱��APEC��ע������֮һ��������Ⱦ�ķ�����Σ������ζ��뻯ѧ�йء����д�ʩ��Ŀ��֮���ϵ��ȷ����
A������װ�����ڰڷ����˵Ļ��ܡ����������ڿ�������
B������������ʹ�ú���ϴ�Ӽ�������ֹ���֡������ն���
C���Ͻ��ŷ�δ���������ж���ҵ��ˮ������ֹˮ����ʧ
D����������װβ������װ�á������ٵ��������Pһ����̼���ŷ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���й��ڽ���ұ����˵����ȷ����
A������ұ���ı����ǽ�����̬������ԭΪ����̬��ұ�������ɽ����Ļ����Ծ���
B��Cu��ʪ��ұ���ǽ�������Ͷ�뵽CuSO4��Һ�У��Ӷ��û���ͭ
C��Feͨ�������Ȼ�ԭ��ұ��������ʯ��ʯ��Ŀ���dz�ȥ������̼
D������Al�Ļ�����ǿ���ʹ�ҵ�ϲ��õ������AlCl3�ķ�������Al
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���ж��й�ʵ����ʵ�Ľ�����ȷ����
A����ij��Һ�еμ���ˮ���ټ���KSCN��Һ����Һ�ʺ�ɫ��˵��ԭ��Һ�к���Fe2+
B��Ũ�����Ũ���᳤�ڱ�¶�ڿ�����Ũ�Ⱦ����ͣ�ԭ������ͬ
C����ij��Һ�м����Ȼ�����Һ�����ɰ�ɫ�������ټ���ϡ���ᣬ�������ܽ⣬��ԭ��Һһ������SO42
D�������£�Ũ��������������������ˣ�˵���������Ũ�����Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ͼΪũ��ɽȪ��Ȫˮƿ�ϵIJ���˵�����֣��г��˸�������Ȼˮ����ָ�꣬����ĸơ�þ���ء�����ָ�� ��
 A��Ԫ�� B��ԭ�� C������ D������
A��Ԫ�� B��ԭ�� C������ D������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ȷ��ʾ���з�Ӧ�����ӷ���ʽ�ǣ� ��
A��Ũ��������м��Ӧ��2Fe+6H+=2Fe3++3H2��
B����������ˮ����Al(OH)3���壺Al3����3H2O=Al(OH)3����3H��
C��Ca(HCO3)2��Һ������NaOH��Һ��Ӧ��
HCO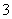 ��Ca2����OH��=CaCO3��+H2O
��Ca2����OH��=CaCO3��+H2O
D��Na2O2����ˮ����O2��Na2O2��H2O=2Na����2OH����O2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ˮ�е�NO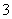 �����ཡ�������Σ����Ϊ�˽�������ˮ��NO
�����ཡ�������Σ����Ϊ�˽�������ˮ��NO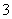 ��Ũ�ȣ�ij����ˮ�о���Ա������ڼ��������������۽�NO
��Ũ�ȣ�ij����ˮ�о���Ա������ڼ��������������۽�NO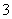 ��ԭΪN2���仯ѧ����ʽΪ��Al + NaNO3 + NaOH �� NaAlO2 + N2��+ H2O (δ��ƽ)����ش���������:
��ԭΪN2���仯ѧ����ʽΪ��Al + NaNO3 + NaOH �� NaAlO2 + N2��+ H2O (δ��ƽ)����ش���������:
��1��������Ӧ�У�________Ԫ�صĻ��ϼ����ߣ����Ԫ�ص�ԭ��________(��õ�����ʧȥ��)���ӣ���________Ԫ�صĻ��ϼ۽��ͣ����Ԫ�ص�ԭ�ӱ�________(���������ԭ��)��
��2����ƽ������Ӧ:
Al + NaNO3 + NaOH = NaAlO2 + N2��+ H2O
��3���á�˫���ŷ�����ʾ��Ӧ�е���ת�Ƶķ������Ŀ:
___________________________________________________________��
��4��������Ӧ������״���²���11.2 L�������ʣ���ת�Ƶ��ӵ���ĿΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����ᣨH2A����pKa1 = 2.86��pKa2 = 5.70����20.00 mL Na2A��NaHA�����Һ�м���1.00 mL 0.0100 mol��L��1 HCl��pHΪ5.70������ͬ��Ũ��10.00 mL HCI��pHΪ4.28�����ʼ���Һ��Na2A��NaHAŨ�Ⱥ�pH��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com