
 如图所示是向MgCl2和AlCl3的混合溶液中加入一定量NaOH溶液,紧接着再加入一定量稀盐酸,生成沉淀的物质的量y与加入溶液的体积x的关系图.根据图示判断,下列结论中不正确的是( )
如图所示是向MgCl2和AlCl3的混合溶液中加入一定量NaOH溶液,紧接着再加入一定量稀盐酸,生成沉淀的物质的量y与加入溶液的体积x的关系图.根据图示判断,下列结论中不正确的是( )| A. | N点时溶液中的溶质只有NaCl | |
| B. | c(NaOH)=c(HCl) | |
| C. | 原混合溶液中c(MgCl2):c(AlCl3)=1:2 | |
| D. | K点之前加入的是NaOH溶液,K点之后加入的是盐酸 |
分析 A、在MgCl2和AlCl3的混合溶液中加入NaOH溶液,首先发生反应:Mg2++2OH-=Mg(OH)2↓、Al3++3OH-=Al(OH)3↓,至N点时Mg2+、Al3+恰好完全沉淀,溶液中的溶质只有NaCl;
B、x=8时(P点),又产生沉淀:AlO-+H++H2O═Al(OH)3↓,说明加入的盐酸与NaOH反应后有剩余,至x=9时(F点),AlO恰好完全转化为Al(OH)3沉淀,用去盐酸1mL,又知在NM段,溶解Al(OH)3需要1mLNaOH溶液,故c(NaOH)=c(HCl);
C、沉淀Al3+需要消耗3mLNaOH溶液,则沉淀Mg2+所消耗的NaOH溶液为2mL,因此c(MgCl2):c(AlCl3)=1:1;
D、接着Al(OH)3开始溶解:Al(OH)3+OH-═AlO-+2H2O,至x=6时(M点)Al(OH)3恰好完全溶解,x在6~8之间时沉淀量不变,说明M点时仍在加入NaOH溶液.
解答 解:A、在MgCl2和AlCl3的混合溶液中加入NaOH溶液,首先发生反应:Mg2++2OH-=Mg(OH)2↓、Al3++3OH-=Al(OH)3↓,至N点时Mg2+、Al3+恰好完全沉淀,溶液中的溶质只有NaCl,故A正确;
B、x=8时(P点),又产生沉淀:AlO-+H++H2O═Al(OH)3↓,说明加入的盐酸与NaOH反应后有剩余,至x=9时(F点),AlO恰好完全转化为Al(OH)3沉淀,用去盐酸1mL,又知在NM段,溶解Al(OH)3需要1mLNaOH溶液,故c(NaOH)=c(HCl),故B正确;
C、因为沉淀Al3+需要消耗3mLNaOH溶液,则沉淀Mg2+所消耗的NaOH溶液为2mL,因此c(MgCl2):c(AlCl3)=1:1,故C错误.
D、接着Al(OH)3开始溶解:Al(OH)3+OH-═AlO-+2H2O,至x=6时(M点)Al(OH)3恰好完全溶解,x在6~8之间时沉淀量不变,说明M点时仍在加入NaOH溶液,故D正确;
故选:C.
点评 本题考查了MgCl2和AlCl3溶液与酸碱的关系,理清反应的整个过程,问题即可解决,可以利用方程式计算,也可以用原子守恒计算.


 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钠可以作食品干燥剂 | B. | 干冰可以用于人工降雨 | ||
| C. | 稀硫酸可以除铁锈 | D. | 氯化钠可以配制生理盐水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 还原剂 | B. | 氧化剂 | C. | 催化剂 | D. | 溶剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCO3-、ClO-、K+、H+ | B. | Na+、Fe2+、NO3-、H+ | ||
| C. | K+、Mg2+、Cl-、SO42- | D. | OH-、NH4+、Cl-、SO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
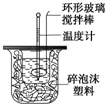 利用下图装置测定中和热的实验步骤如下:
利用下图装置测定中和热的实验步骤如下:| 温度 实验次数 | 起始温度t1℃ | 终止温度t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
| HCl | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 29.5 | |
| 2 | 27.0 | 27.4 | 27.2 | 32.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.2 | |
| 4 | 26.4 | 26.2 | 26.3 | 29.8 | |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ②④ | C. | ③ | D. | ①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 1 mol苯乙烯可以和4mol Br2发生加成反应 | |
| B. | 分子中所有原子可以在同一平面内 | |
| C. | 与HCl加成只生成一种产物 | |
| D. | 能使酸性KMnO4溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁与硫酸铜溶液反应:Fe+Cu2+═Fe2++Cu | |
| B. | 硫酸铜溶液与氢氧化钡溶液混合:Cu2++SO42-+Ba2++2OH-═Cu(OH)2↓+BaSO4↓ | |
| C. | 在碳酸氢钠溶液中滴加稀盐酸:H++HCO3-═CO2↑+H2O | |
| D. | 铁与稀盐酸反应制取氢气:2Fe+6H+═2Fe3++3H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol/L | B. | 0.2mol/L | C. | 0.3mol/L | D. | 0.4mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com