
【题目】下列说法正确的是![]()
![]()
A.海水淡化的常用方法有蒸馏法、电渗析法和过滤法
B.pH相等的三种溶液:![]() 溶液
溶液![]() 溶液
溶液![]() 溶液,其浓度大小顺序为
溶液,其浓度大小顺序为![]()
C.在![]() 和
和![]() 的混合溶液中加入
的混合溶液中加入![]() 产生黑色沉淀,证明
产生黑色沉淀,证明![]()
D.侯式制碱法的化学方程式为![]()
【答案】D
【解析】
A.海水淡化的常用方法有蒸馏法、电渗析法和离子交换法,过滤不能淡化海水,只能除去水中难溶性的物质,A错误;
B.NH4HSO4电离产生H+使溶液显酸性,NH4Cl中NH4+水解消耗水电离产生的OH-使溶液显酸性;NH4Al(SO4)2中NH4+、Al3+都水解消耗水电离产生的OH-使溶液显酸性,电离作用大于水解作用,所以浓度相等的![]() 溶液、
溶液、![]() 溶液、
溶液、![]() 溶液的pH关系为
溶液的pH关系为![]() ,则pH相等的三种溶液的物质的量浓度关系为
,则pH相等的三种溶液的物质的量浓度关系为![]() ,B错误;
,B错误;
C.由于硫化铜和硫化银均为黑色沉淀,二者构型不同,所以不能证明二者的溶度积的大小关系,C错误;
D.侯式制碱法是利用饱和氯化钠溶液与氨气、二氧化碳反应得到溶解度较小的碳酸氢钠,对应的化学方程式为![]() ,D正确;
,D正确;
故合理选项是D。


科目:高中化学 来源: 题型:
【题目】以煤为主要原料可以制备乙二醇,相关工艺流程如下:

(1)写出方法l在催化剂的条件下直接制取乙二醇的化学方程式_______
(2)合成气在不同催化剂作用下,可以合成不同的物质。下列物质仅用合成气为原料就能得到且原子利用率为100%的是_____填字母)。
A.草酸( HOOC-COOH) B.甲醇(CH3OH) C.尿素[CO(NH2)2]
(3)工业上还可以利用天然气(主要成份为CH4)与C02反应制备合成气。已知:
CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890.3kJ/mol
2H2(g)+ O2(g)= 2H2O(l) △H=-571.6kJ/mol
2CO(g)+O2(g)=2CO2(g) △H=-566.0kJ/mol
则CH4与CO2生成合成气的热化学方程式为____________________。
(4)方法2:在恒容密闭容器中投入草酸二甲酯和H2发生如下反应:
CH3OOC—COOCH3(g)+ 4H2(g)![]() HOCH2CH2OH(g)+2CH3OH(g)△H=-34kJ/mol
HOCH2CH2OH(g)+2CH3OH(g)△H=-34kJ/mol
为提高乙二醇的产量和速率,宜采用的措施是___________(填字母)。
A.升高温度 B.增大压强 C.增大氢气浓度
(5)草酸二甲酯水解生成草酸:CH3OOC—COOCH3+ 2H2O![]() HOOC—COOH+2CH3OH
HOOC—COOH+2CH3OH
①草酸是二元弱酸,可以制备![]() (草酸氢钾),
(草酸氢钾),![]() 溶液呈酸性,用化学平衡原理解释:__________________。
溶液呈酸性,用化学平衡原理解释:__________________。
②在一定的![]() 溶液中滴加NaOH溶液至中性。下列关系一定不正确的是_______(填字母)。
溶液中滴加NaOH溶液至中性。下列关系一定不正确的是_______(填字母)。
A.![]()
B.![]()
C.![]()
(6)乙二醇、空气在KOH溶液中构成燃料电池,加入乙二醇的电极为电源的_____填“正”或“负”)极,负极反应式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃时,将1.0Lc mol·L-1 CH3COOH溶液与0.1mol NaOH固体混合,使之充分反应。然后向该混合溶液中通入HCl气体或加入NaOH固体(忽略体积和温度变化),溶液pH随通入(或加入)物质的物质的量的变化如图所示。下列叙述错误的是( )
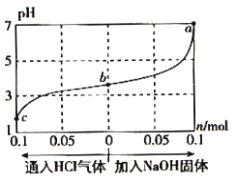
A.水的电离程度:a>b>c
B.b点对应的混合溶液中:c(Na+)<c(CH3COO-)
C.c点对应的混合溶液中:c(CH3COOH)>c(Na+)>c(OH-)
D.该温度下,a、b、c三点CH3COOH的电离平衡常数均为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验事实得出的相应结论正确的是( )
选项 | 实验事实 | 结论 |
A | NH3 的水溶液可以导电 | NH3 是电解质 |
B | SO2 通入硝酸钡溶液出现白色沉淀 | BaSO3 不溶于强酸 |
C | 浓硝酸久置发黄 | 硝酸不稳定 |
D | 浓硫酸能脱去胆矾晶体中的水 | 浓硫酸具有脱水性 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将![]() 缓慢通入100mL水中至饱和,然后向所得饱和氯水中逐滴加人
缓慢通入100mL水中至饱和,然后向所得饱和氯水中逐滴加人![]() 溶液,整个过程中pH的变化如图所示,下列有关叙述正确的是( )
溶液,整个过程中pH的变化如图所示,下列有关叙述正确的是( )

A.曲线③④段有离子反应:![]()
B.可依据②处数据计算所溶解的![]()
C.③处表示氯气与氢氧化钠溶液恰好反应完全
D.①处![]() 约为
约为![]() 处
处![]() 的两倍
的两倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的叙述正确的是( )
A. 已知氟利昂12的结构式为![]() ,该分子是平面形分子
,该分子是平面形分子
B. 1mol苹果酸[HOOCCH(OH)CH2COOH]可与3molNaHCO3发生反应
C. 用甲苯分别制取TNT、邻溴甲苯所涉及的反应均为取代反应
D. ![]() 的一氯代物共有5种(不考虑立体异构)
的一氯代物共有5种(不考虑立体异构)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.如图为原电池装置示意图。
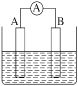
(1)若A为Pb,B为PbO2,电解质为H2SO4溶液,工作时的总反应为Pb+PbO2+2H2SO4=2PbSO4+2H2O,写出B电极反应式:__。该电池在工作时,A电极的质量将___(填“增加”“减小”或“不变”),若该电池反应消耗了0.1molH2SO4,则转移电子的数目为__。
(2)若A、B均为铂片,电解质为KOH溶液,分别从A、B两极通入H2和O2,该电池即为氢氧燃料电池,写出A电极反应式:___。该电池在工作一段时间后,溶液的碱性将___(填“增强”“减弱”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 时,向
时,向![]() 溶液中滴加等浓度的NaOH溶液,溶液的pH与NaOH溶液的体积关系如图所示.下列叙述不正确的是
溶液中滴加等浓度的NaOH溶液,溶液的pH与NaOH溶液的体积关系如图所示.下列叙述不正确的是![]()

A.C点溶液中含有![]() 和
和![]()
B.![]() 溶液中水的电离程度比
溶液中水的电离程度比![]() 溶液中小
溶液中小
C.B点,![]()
D.D点,![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阅读下列材料,完成下列小题。
戴维发现Cl2的反应为MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O。多余的Cl2可用NaOH溶液吸收。液氯用于自来水消毒已成为目前给水系统中最为经济有效的消毒技术,但其消毒后生成的副产物对人体存在健康隐患。ClO2是一种易溶于水的气体,是国际上公认的高效、安全、无毒的绿色消毒剂。
MnCl2+Cl2↑+2H2O。多余的Cl2可用NaOH溶液吸收。液氯用于自来水消毒已成为目前给水系统中最为经济有效的消毒技术,但其消毒后生成的副产物对人体存在健康隐患。ClO2是一种易溶于水的气体,是国际上公认的高效、安全、无毒的绿色消毒剂。
【1】戴维发现Cl2的反应中,还原剂是
A.MnO2B.HClC.MnCl2D.Cl2
【2】从氧化还原反应的角度分析,下列物质中不可以替代MnO2的是
A.O2B.NaClO3C.NaClOD.NaCl
【3】Cl2被NaOH溶液吸收时会生成NaClO。NaClO属于
A.酸B.碱C.盐D.氧化物
【4】下列物质中可以替代NaOH溶液吸收Cl2的是
A.石灰乳B.食盐水C.浓硫酸D.稀盐酸
【5】实验室收集ClO2可以采用的方法是
A.![]() B.
B.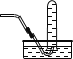 C.
C.![]() D.
D.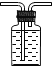
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com