
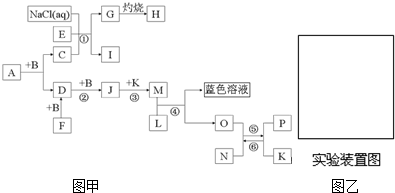
分析 反应①②③均是化工生产中的重要反应,I是一种常用的氮肥,由氯化钠溶液反应生成,所以反应①是侯德榜制碱法的反应,可推知I为NH4Cl,G为NaHCO3,H为Na2CO3,E、C分别为中为CO2、NH3中的一种,A是一种含两种元素组成的液态有机溶剂,A中含有碳元素,A与单质B反应得到C,则B为O2,C为CO2,故E为NH3.单质F与B(O2)反应生成D为氧化物,D与氧气继续反应生成J也是氧化物,而M(D)=2M(B)=2M(F),可推知F为S,D为SO2,J为SO3,则A与氧气反应生成二氧化碳与二氧化硫,则A为CS2,A和B反应前后气体体积(常温常压)保持不变.单质P与K反应得到N与单质O,N为磁性氧化物,则N为Fe3O4,O为H2,P为Fe,K为H2O,可推知M为H2SO4,L为单质,与硫酸在一定条件下反应生成蓝色溶液,所以L为Cu,据此解答.
解答 解:反应①②③均是化工生产中的重要反应,I是一种常用的氮肥,由氯化钠溶液反应生成,所以反应①是侯德榜制碱法的反应,可推知I为NH4Cl,G为NaHCO3,H为Na2CO3,E、C分别为中为CO2、NH3中的一种,A是一种含两种元素组成的液态有机溶剂,A中含有碳元素,A与单质B反应得到C,则B为O2,C为CO2,故E为NH3.单质F与B(O2)反应生成D为氧化物,D与氧气继续反应生成J也是氧化物,而M(D)=2M(B)=2M(F),可推知F为S,D为SO2,J为SO3,则A与氧气反应生成二氧化碳与二氧化硫,则A为CS2,A和B反应前后气体体积(常温常压)保持不变.单质P与K反应得到N与单质O,N为磁性氧化物,则N为Fe3O4,O为H2,P为Fe,K为H2O,可推知M为H2SO4,L为单质,与硫酸在一定条件下反应生成蓝色溶液,所以L为Cu.
(1)由以上分析可知A为CS2,故答案为:CS2;
(2)反应①的反应方程式为:NaCl+CO2+H2O+NH3=NaHCO3↓+NH4Cl,工业上叫联合制碱法或侯氏制碱法,
故答案为:NaCl+CO2+H2O+NH3=NaHCO3↓+NH4Cl;联合制碱法或侯氏制碱法;
(3)反应⑥的化学方程式:3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2,
故答案为:3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2;
(4)在加热条件下,硫与铜反应生成硫化亚铜,化学反应方程式为:2Cu+S$\frac{\underline{\;\;△\;\;}}{\;}$Cu2S,
故答案为:2Cu+S$\frac{\underline{\;\;△\;\;}}{\;}$Cu2S;
(5)完成反应④,应是铜作阳极,碳作阴极,电解质溶液为硫酸,装置图为 ,
,
故答案为: .
.
点评 本题考查无机物的推断,涉及S、Fe、Cu元素单质化合物性质以及常见化学工业,题目难度较大,注意利用物质的颜色、连续反应、常见化学工业等进行推断,难度较大.


科目:高中化学 来源: 题型:选择题
| A. | 原子序数为34 | B. | 还原性:H2Se<H2S | ||
| C. | 酸性:H2SeO4<HBrO4 | D. | Se氧化物化学式有:SeO2、SeO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 烃的组成均符合通式CnH2n+2 | |
| B. | 烃类均不溶于水 | |
| C. | 甲烷在烃中含碳量最低 | |
| D. | 甲烷只能发生取代反应而不能发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+ Na+ OH- SO42- | B. | Mg2+ SO42- NH4+ Cl- | ||
| C. | K+ Na+ HCO3- Cl- | D. | K+ Na+ NO3- CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 17g氨气中所含原子数为NA | |
| B. | 标准状况下,1 L水中所含分子数为$\frac{1}{22.4}$NA | |
| C. | 0.3 mol/L的MgCl2溶液中含Mg2+数目0.3 NA | |
| D. | 常温常压下,16 g O2含有的氧原子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (1)(3)(4) | B. | (1)(3)(5) | C. | (2)(4)(5) | D. | (1)(4)(5) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,2.24 L苯中含有的分子数为0.1 NA | |
| B. | 标准状况下,2.24 L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.1 NA | |
| C. | 0.1 mol•L-1的硫酸铜溶液中含铜离子数为0.1 NA | |
| D. | 1mol FeCl3跟水完全反应转化为氢氧化铁胶体后,其中胶体粒子的数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若a的相对分子质量是42,则d是乙醛 | |
| B. | 若d的相对分子质量是44,则a是乙炔 | |
| C. | 若a为苯乙烯(C6H5-CH=CH2),则f的分子式是C16H3202 | |
| D. | 若a为单烯烃,则d与f的实验式一定相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 焰色反应实验中,铂丝在蘸取待测溶液前,应先用稀硫酸洗净并灼烧 | |
| B. | 检验某溶液是否含有SO42-时,应取少量该溶液,依次加入BaCl2溶液和稀盐酸 | |
| C. | 取用一小块钾后,剩余的钾可放回原试剂瓶里 | |
| D. | 将NaOH溶液滴加到AlCl3溶液中,振荡,制备Al(OH)3胶体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com