
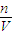 计算氢氧化钠的浓度.
计算氢氧化钠的浓度.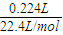 =0.01mol,则:
=0.01mol,则: =0.46g,
=0.46g,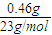 =0.02mol,n(Na2O)=
=0.02mol,n(Na2O)=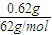 =0.01mol,
=0.01mol,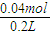 =0.2mol/L,
=0.2mol/L,

科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A.9.2 g B.10.6 g? C.6.2 g D.4.6 g?
查看答案和解析>>
科目:高中化学 来源:2011-2012学年河北省南宫中学高一12月月考化学试卷 题型:单选题
一块表面已被氧化为Na2O的钠块10.8g,将其投入100g水中,产生H2 0.2g,则被氧化的钠是 ( )
| A.9.2g | B.10.6g | C.6.2g | D.4.6g |
查看答案和解析>>
科目:高中化学 来源:2014届广东省佛山市高一上学期第二阶段考试化学试卷 题型:计算题
(6分)一块表面已被氧化为Na2O的钠块8.5g,将其投入1L水中,测得产生H2 标况下体积为1.12L,通过计算求出未被氧化的钠与已被氧化的钠的质量比。(要求得出最简整数比)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com