
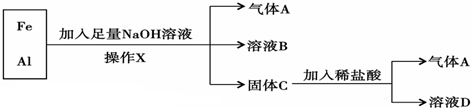
分析 由分离流程可知,Fe、Al的混合物中加入足量NaOH后,只有Al与NaOH溶液发生反应生成偏铝酸钠和氢气,而Fe和氢氧化钠不反应,则A是氢气,B是偏铝酸钠和过量的氢氧化钠的混合物,固体C是Fe,金属铁可以和盐酸反应生成氯化亚铁和氢气,则D是氯化亚铁,以此来解答.
解答 解:由分离流程可知,Fe、Al的混合物中加入足量NaOH后,只有Al与NaOH溶液发生反应生成偏铝酸钠和氢气,而Fe和氢氧化钠不反应,则A是氢气,B是偏铝酸钠和过量的氢氧化钠的混合物,固体C是Fe,金属铁可以和盐酸反应生成氯化亚铁和氢气,则D是氯化亚铁,
(1)操作X分离溶液与不溶性固体,则名称是过滤,故答案为:过滤;
(2)气体A是H2(或氢气),故答案为:H2(或氢气);
(3)A与Cl2混合光照可能发生爆炸,生成HCl,H元素的化合价升高,则A在该反应中作为还原剂,故答案为:HCl;还原剂;
(4)溶液B中阴离子除OH-外还有AlO2-;溶液D中存在的金属离子为Fe2+;如等物质的量的铝和铁分别与足量的盐酸反应,Al、Fe均完全反应,由电子守恒可知,气体的物质的量比等于金属失去电子数之比,则生成的气体的物质的量之比为(3-0):(2-0)=3:2,故答案为:AlO2-;Fe2+;3:2.
点评 本题考查混合物的分离提纯,为高频考点,把握物质的性质、流程中发生的反应、混合物分离方法为解答的关键,侧重分析与应用能力的考查,注意元素化合物性质的综合应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 金属铝溶于氢氧化钠溶液 Al+2OH-→AlO2-+H2↑ | |
| B. | 铁跟稀硫酸反应:Fe+2H+→Fe2++H2↑ | |
| C. | 碳酸钙跟盐酸反应:CO32-+2H+→CO2↑+H2O | |
| D. | 氯化铝溶液中加入过量的氨水:Al3++3OH-→Al(OH)3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
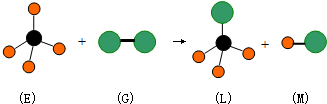
| A. | L能溶于水 | B. | M属于离子化合物 | ||
| C. | G有漂白性 | D. | 该反应是取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 位于 IA的元素与位于ⅦA的元素组成的化合物都是离子化合物 | |
| B. | 元素周期表中ⅡA族的元素都是金属元素 | |
| C. | 元素周期表有7个横行,18个纵列 | |
| D. | 除氦外的稀有气体原子的最外层电子数都是8个 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钠溶液 | B. | 浓氨水 | C. | 盐酸 | D. | 硝酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
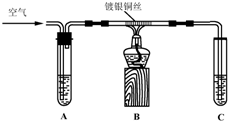 Ⅰ.中学课本中介绍了如下实验:把一端弯成螺旋状的铜丝放在酒精灯外焰加热,待铜丝表面变黑后立即把它插入盛有约2mL乙醇的试管里,反复操作几次.上述实验判断有乙醛生成的现象为铜丝由黑变红,并产生刺激性气味
Ⅰ.中学课本中介绍了如下实验:把一端弯成螺旋状的铜丝放在酒精灯外焰加热,待铜丝表面变黑后立即把它插入盛有约2mL乙醇的试管里,反复操作几次.上述实验判断有乙醛生成的现象为铜丝由黑变红,并产生刺激性气味查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com