
设NA为阿伏加德罗常数的值。下列说法中,正确的是
A.1mol Na被氧化完全转化生成Na2O2,失去电子数为2NA
B.常温常压下,46g由NO2和N2O4组成的混合气体中含有原子的总数为3NA
C.将lmL 1 mol·L-1 FeCl3溶液逐滴加入沸水,制得红褐色Fe(OH)3胶体,所含胶粒的数目是1×10-3NA
D.标准状况下,6.72L NO2与足量水充分反应转移的电子数目为0.3NA
B
【解析】
试题分析:A.1mol Na被氧化完全转化生成Na2O2,钠的化合价是+1价,则失去电子数为NA,A错误;B.NO2和N2O4的最简式相同,均是NO2,则常温常压下,46g由NO2和N2O4组成的混合气体中相当于含有的NO2的物质的量是46g÷46g/mol=1mol,所以含有原子的总数为3NA,B正确;C.铁离子水解是可逆反应,则将lmL 1 mol·L-1 FeCl3溶液逐滴加入沸水,制得红褐色Fe(OH)3胶体,所含胶粒的数目小于1×10-3NA,C错误;D.标准状况下,6.72L NO2的物质的量是6.72L÷22.4L/mol=0.3mol。根据方程式3NO2+H2O=2HNO3+NO可知与足量水充分反应转移的电子数目为0.2NA,D错误,答案选B。
考点:考查阿伏加德罗常数的计算


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2014-2015学年安徽省濉溪县高三第二次月考化学试卷(解析版) 题型:选择题
为实现下列实验目的,下表提供的主要玻璃仪器和所用试剂合理的是
选项 | 实验目的 | 主要玻璃仪器 | 试剂 |
A | 鉴别Na2CO3和NaHCO3溶液 | 试管、胶头滴管 | 澄清石灰水 |
B | 分离I2和CCl4的混合物 | 分液漏斗、烧杯 | 乙醇 |
C | 实验室制取干燥的NH3 | 试管、酒精灯、带导管的橡皮塞 | NH4Cl、Ca(OH)2、碱石灰 |
D | 测定NaOH溶液的浓度 | 滴定管、锥形瓶、烧杯 | NaOH溶液、酚酞试剂、0.1000 mol·L-1盐酸 |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省济南市高三上学期期末考试化学试卷(解析版) 题型:选择题
实验室需配制一种溶液,除水电离出的离子外还含有五种离子,且在该溶液中这五种离子的物质的量浓度均为l mol·L-1,下面四个选项中,能达到此要求的是
A.Al3+、K+、SO42-、Cl-、HCO3- B.Fe2+、H+、Br-、NO3—、Cl-
C.Na+、K+、SO42-、NO3—、Cl- D.Al3+、Na+、Cl-、SO42-、NO3—
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省济南市高三上学期期末考试化学试卷(解析版) 题型:选择题
短周期中的主族元素M、R(M、R代表元素符号)形成的简单离子M2-与R+的核外电子数之和为20,下列说法中,正确的是
A.M原子所含质子数一定大于R原子所含质子数
B.M、R两种元素结合形成的化合物中不可能含有共价键
C.M2-与R+的电子层结构不可能相同
D.M一定存在同素异形体
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北大冶一中等六校高三元月调考理综化学试卷(解析版) 题型:实验题
(15分)硫代硫酸钠是一种重要的化工产品。工业上常利用含硫废水生产Na2S2O35H2O,实验室可用如下装置(略去部分加持仪器)模拟生成过程。
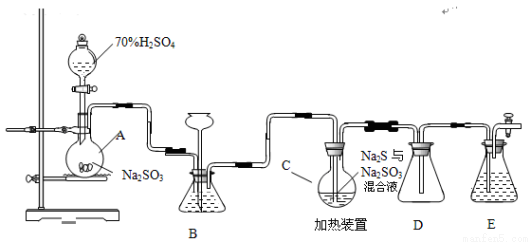
烧瓶C中发生反应如下:
Na2S(aq)+H2O(l)+SO2(g)=Na2SO3(aq)+H2S(aq) (I)
2H2S(aq)+SO2(g)=3S(s)+2H2O(l) (II)
S(s)+Na2SO3(aq) Na2S2O3(aq) (III)
Na2S2O3(aq) (III)
(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液注,若 ,则整个装置气密性良好。装置D的作用是 。装置E中为 溶液。
(2)为提高产品纯度,应使烧瓶C中Na2S和Na2SO3恰好完全反应,则烧瓶C中Na2S和Na2SO3物质的量之比为 。
(3)装置B的作用之一是观察SO2的生成速率,其中的液体最好选择 。
a.蒸馏水 b.饱和Na2SO3溶液
c.饱和NaHSO3溶液 d.饱和NaHCO3溶液
(4)实验中,为使SO2缓慢进入烧瓶C,采用的操作是 。
(5)已知反应(III)相对较慢,则烧瓶C中反应达到终点的现象是 。
(6)反应终止后,烧瓶C中的溶液经蒸发浓缩冷却,过滤,洗涤,干燥,即得到粗产品(主要含有Na2S2O35H2O和其他杂质)。某兴趣小组为测定该产品纯度,准确称取4.96 g产品,用适量蒸馏水溶解,以淀粉作指示剂,用0.1000 molL1碘的标准溶液滴定。反应原理为:2S2O32-+I2=S4O62-+2I,滴定至终点时,滴定起始和终点的液面位置如下图,则产品的纯度为_________。
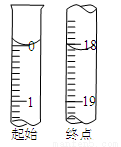
经仪器分析,该产品纯度为16%,分析该兴趣小组测定产品纯度偏差的原因(忽略人为误差)_______。
[M(Na2S2O35H2O)=248g/mol]
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北大冶一中等六校高三元月调考理综化学试卷(解析版) 题型:选择题
下列离子方程式书写正确的是
A.H218O中投入Na2O2固体:2H218O+2Na2O2===4OH-+4Na++18O2↑
B.Fe3O4与稀HNO3反应:Fe3O4+8H+===Fe2++2Fe3++4H2O
C.向NaHCO3溶液中加入少量Ca(OH)2:HCO3-+Ca2++OH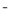 ===CaCO3↓+H2O
===CaCO3↓+H2O
D.将少量NaOH溶液加入到NH4HCO3溶液中:OH-+HCO3-===CO32-+H2O
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省高三12月月考化学试卷(解析版) 题型:选择题
镁粉是制备焰火的原料,工业上通过冷却镁蒸气制得镁粉。下列气体中可以用冷却镁蒸气的是
A.空气 B.二氧化碳 C.氧气 D.氩气
查看答案和解析>>
科目:高中化学 来源:2014-2015学年安徽省合肥市高三第一次教学质量检测化学试卷(解析版) 题型:选择题
在Na2O2与CO2 的反应中,下列说法正确的是
A.该反应中Na2O2 是氧化剂,CO2 是还原剂
B.1mol Na2O2参加反应,有2mole—转移
C.Na2O2晶体中阴阳离子个数比为1:2
D.CO2分子中含有极性键和非极性键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com