
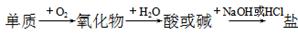
| A£®¹č | B£®Įņ | C£®Ķ | D£®Ģś |


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
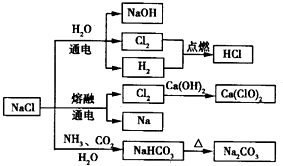
| A£®25”ę£¬NaHCO3ŌŚĖ®ÖŠµÄČܽā¶Č±ČNa2CO3µÄ“ó |
| B£®ŹÆ»ŅČéÓėCl2µÄ·“Ó¦ÖŠ£¬Cl2¼ČŹĒŃõ»Æ¼Į£¬ÓÖŹĒ»¹Ō¼Į |
| C£®³£ĪĀĻĀøÉŌļµÄCl2ÄÜÓĆøÖĘæÖü“ę£¬ĖłŅŌCl2²»ÓėĢś·“Ó¦ |
| D£®ČēĶ¼ĖłŹ¾×Ŗ»Æ·“Ó¦¶¼ŹĒŃõ»Æ»¹Ō·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®S2ŗĶS4 | B£®COŗĶCO2 | C£®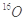 ŗĶ ŗĶ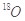 | D£®H2ŗĶD2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗŹµŃéĢā
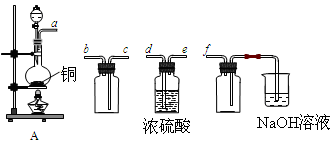
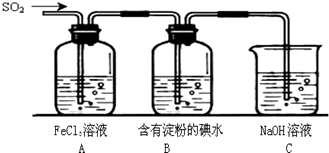
| A£®ÉÕĘæ | B£®¾Ę¾«µĘ | C£®Ā©¶· | D£®ÉÕ± E£®²£Į§°ō |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗŹµŃéĢā
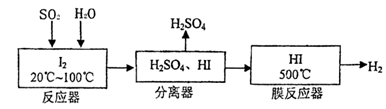
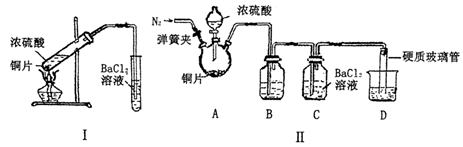
| øĽųµÄ²Ł×÷»ņ×°ÖĆ(×¢Ć÷±ŲŅŖµÄŹŌ¼Į) | øĽųµÄ×÷ÓĆ |
| Ź¹ÓĆ·ÖŅŗĀ©¶·µĪ¼ÓÅØĮņĖį | æŲÖĘ·“Ó¦ĖŁĀŹ |
| | |
| | |
| | |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®µćČ¼Įņ»Ē£®²śÉś“Ģ¼¤ŠŌĘųĪ¶ĘųĢ壬øĆĘųĢåæÉŅŌĘÆ°×Ö½½¬ |
| B£®ĻņÕįĢĒÖŠ¼ÓČėÅØĮņĖį£¬ÕįĢĒ±äŗŚÉ«£¬ĖµĆ÷ÅØĮņĖį¾ßÓŠĒæµÄĪüĖ®ŠŌ |
| C£®½«H2SĘųĢåĶØČėCuSO4ČÜŅŗÉś³ÉCuS³Įµķ£¬ĖµĆ÷H2SĪŖĒæµē½āÖŹ |
| D£®½«Alʬ¼ÓČėÅØĮņĖįÖŠ£¬·“Ó¦¾ēĮŅ£¬ĖµĆ÷ÅØĮņĖį¾ßÓŠĒæµÄŃõ»ÆŠŌ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĪŹ“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®ĪŽ·ØČ·¶Øѳʷ֊ÄĘ”¢ĮņŌŖĖŲµÄÖŹĮæ±Č |
| B£®Na2SO3Ņѱ»Ńõ»Æ |
| C£®¼ÓČėBa(NO3)2ČÜŅŗŗó£¬Éś³ÉµÄ³ĮµķÖŠŅ»¶Øŗ¬ÓŠBaSO4 |
| D£®¼ÓČėĻ”ĻõĖįŗóµÄ³ĮµķŅ»¶ØŹĒBaSO4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®¢Ś¢Ū¢Ü¢Ž | B£®¢Ś¢Ü¢Ż¢Ž | C£®¢Ł¢Ś¢Ü¢Ż | D£®¢Ū¢Ü¢Ż¢Ž |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com