
| A�� | �Ȳ���ʹ¯��˲��������ֲ��ܽ�ʡȼ�� | |
| B�� | �䲻��ʹ¯��˲������������Խ�ʡȼ�� | |
| C�� | ����ʹ¯��˲������ֿ��Խ�ʡȼ�� | |
| D�� | ���ܽ�ʡȼ�ϣ�����ʹ¯��˲����� |
���� ���ݸ�˹����������ú������ȼ��;���ų����������Ӷ������ܷ��ʡȼ�Ϻ�¯���Ƿ�˲�������
��� �⣺úֱ̿��ȼ�յ��Ȼ�ѧ����ʽ��C��s��+O2��g��=CO2��g����H=-392kJ/mol��
��¯����ͨ��ˮ����ʱ�������·�Ӧ��C��s��+H2O��g��=CO��g��+H2��g����H=+131kJ/mol �٣�
CO��g��+$\frac{1}{2}$O2��g���TCO2��g����H=-282KJ/mol�ڣ�H2��g��+$\frac{1}{2}$O2��g���TH2O��g����H=-241KJ/mol����
����̼�Ⱥ�ˮ������Ӧ����CO��������������ȼ��ʱ��ú֮̿��ȼ�ջ��������
���ݸ�˹���ɿ�֪������+��+�ۿɵã�C��s��+O2��g��=CO2��g����H=+131KJ/mol-282KJ/mol-241KJ/mol=-392kJ/mol����úֱ̿��ȼ�յ���ЧӦ����ͬ�ģ��ʲ�����ʡȼ�ϣ���ѡD��
���� ���⿼����ȼ�ϵ�ȼ�պ�˹���ɵ����ã��ѶȲ���ע��֪ʶ��������ã�


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ü���������۵ķ�����ȥCu��NO3�� 2��Һ�л��е�AgNO3 | |
| B�� | ��NaOH��Һ��ȥCO2�л��е�HCl���� | |
| C�� | ��ij��ɫδ֪��Һ�м���BaCl2��Һ���Լ���δ֪��Һ���Ƿ���SO42- | |
| D�� | ����ɫʯ����Һ��BaCl2��Һ�������ᡢ���ᡢ�����ơ��������ƺ������������ɫ��Һ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
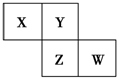 X��Y��Z��W��Ϊ������Ԫ�أ����������ڱ��е����λ����ͼ��ʾ����Yԭ�ӵ��������������ڲ��������3��������˵������ȷ���ǣ�������
X��Y��Z��W��Ϊ������Ԫ�أ����������ڱ��е����λ����ͼ��ʾ����Yԭ�ӵ��������������ڲ��������3��������˵������ȷ���ǣ�������| A�� | ����Ԫ�صļ��⻯�ﶼΪ���Է��� | |
| B�� | ����������Ӧ��ˮ���������W��Z�� | |
| C�� | Z�ĵ�����������Ӧ��Y���� | |
| D�� | X��Y�γɵĻ����ﶼ������ˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����Ħ�����ԼΪ22.4L•mol-1 | |
| B�� | �ڱ�״���£�1mol�κ�������ռ�������ԼΪ22.4L | |
| C�� | HNO3��Ħ��������63g | |
| D�� | ����������Ħ��������ȣ�����98g/mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
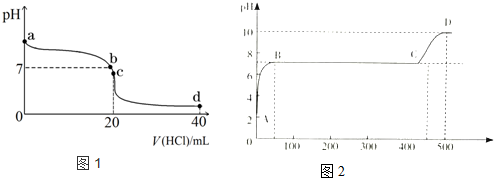
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | K+��Br-��Cl-��SO42- | B�� | SCN-��Fe3+��Cl-��K+ | ||
| C�� | K+��Cu2+��SO42-��Na+ | D�� | Na+��ClO-��NO3-��SO42- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
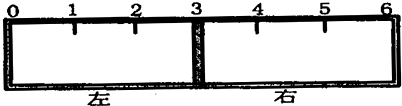
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com