
黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之一,还可以制备硫及铁的化合物.
(1)冶炼铜的反应为:
8CuFeS2+21O2 8Cu+4FeO+2Fe2O3+16SO2
8Cu+4FeO+2Fe2O3+16SO2
若CuFeS2中Fe的化合价为+2,反应中被还原的元素是 (填元素符号).
(2)上述冶炼过程产生大量SO2.下列处理方案中合理的是 (填代号).
a.高空排放 b.用于制备硫酸
c.用纯碱溶液吸收制Na2SO4 d.用浓硫酸吸收
(3)过二硫酸钾(K2S2O8)具有强氧化性,可将I﹣氧化为I2:S2O82﹣+2I﹣=2SO42﹣+I2.
通过改变反应途径,Fe3 +、Fe2+均可催化上述反应.试用离子方程式表示Fe3+对上述反应催化的过程: 、 (不必配平)
+、Fe2+均可催化上述反应.试用离子方程式表示Fe3+对上述反应催化的过程: 、 (不必配平)
(4)利用黄铜矿冶炼铜产生的炉渣(含Fe2O3、FeO、SiO2、Al2O3)可制备Fe2O3.方法为:
①用稀盐酸浸取炉渣,过滤.
②滤液先氧化,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得Fe2O3.
a.除去Al3+的离子方程式是 .
b.选用提供的试剂,设计实验验证炉渣中含有FeO.
提供的试剂:稀盐酸 稀硫酸 KSCN溶液 KMnO4溶液 NaOH溶液 碘水
所选试剂为 .证明炉渣中含有FeO的实验现象为 .
考点: 铁的化学性质;含硫物质的性质及综合应用;制备实验方案的设计.
专题: 氧族元素;几种重要的金属及其化合物.
分析: (1)反应中化合价降低的元素被还原;
(2)冶炼过程产生大量SO2,处理方案中合理的分析是二氧化硫是污染性气体,不能排放到空气中,可以吸收利用;
(3)三价铁具有氧化性,能将碘离子氧化;
(4)a、氧化铝是两性氧化物,能和强酸以及强碱反应;
b、亚铁离子能被高锰酸钾溶液氧化,使的高锰酸钾溶液褪色.
解答: 解:(1)化合价降低的元素Cu、O,在反应中被还原,故答案为:Cu、O;
(2)冶炼过程产生大量SO2.分析下列处理方案:
a.二氧化硫是污染性气体,高空排放会污染空气,处理不合理,故a错误;
b.可以利用吸收二氧化硫生成硫酸,用于制备硫酸,故b合理;
c.用纯碱溶液吸收二氧化硫可以制Na2SO4,故c合理;
d.用浓硫酸不能吸收二氧化硫,故d不合理;
故答案为:b、c.
(3)三价铁具有氧化性,能将碘离子氧化,S2O82﹣能将亚铁离子氧化,原理为:2Fe3++2I﹣=2Fe2++I2,S2O82﹣+2Fe2+=2SO42﹣+2Fe3+,
故答案为:2Fe3++2I﹣=2Fe2++I2;S2O82﹣+2Fe2+=2SO42﹣+2Fe3+;
(4)a.氧化铝是两性氧化物,能和强酸以及强碱反应,6H++AI2O3=3H2O+2Al3+,除去铝离子的反应是利用过量氢氧化钠溶液和铝离子反应生成四羟基合铝,
故答案为:Al3++4OH﹣=2H2O+AlO2﹣;
b.高锰酸钾溶液能氧化亚铁离子,使得高锰酸钾溶液褪色,故答案为:稀硫酸、KMnO4溶液;稀硫酸浸取炉渣所得溶液使KMnO4溶液褪色.
点评: 本题是对金属的化学性质的考查,要求学生熟记教材知识,学以致用,综合性较强,难度中等.


 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:高中化学 来源: 题型:
2012年2月6日,在辽宁沈阳至本溪段的丹霞公路发生了应雾大路滑而引起汽车追尾的重大的交通事故.雾属于下列哪种分散系()
A. 乳浊液 B. 溶液 C. 胶体 D. 悬浊液
查看答案和解析>>
科目:高中化学 来源: 题型:
将铝粉与某铁的氧化物FeO•2Fe2O3粉末配制成铝热剂,分成两等份.一份直接放入足量的烧碱溶液中,充分反应后放出气体在标准状况下的体积为15.68L;另一份在高温下恰好反应完全,反应后的混合物与足量的盐酸反应后,放出的气体在标准状况下的体积为()
A. 11.20L B. 15.68L C. 22.40L D. 31.36L
查看答案和解析>>
科目:高中化学 来源: 题型:
还原2.4×10﹣3 mol XO(OH)3+到X元素的低价态时,消耗0.2mol•L﹣1的Na2SO3溶液30mL,则X元素反应后的价态是()
A. +1 B. ﹣1 C. 0 D. ﹣2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列措施或事实不能用勒夏特列原理解释的是()
A. 新制的氯水在光照下颜色变浅
B. Fe(SCN)3溶液中加入6mol/L NaOH溶液后颜色变浅
C. 在合成氨的反应中,降温或加压有利于氨的合成
D. H2、I2、HI平衡混合气加压后颜色变深
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关实验的说法不正确的是()
A. 在测定中和反应的反应热实验中,要读取最高温度
B. 中和滴定实验中,洗净后的锥形瓶不需要干燥
C. 向CH3COONa溶液中滴入石蕊试液,溶液变蓝
D. 向白色ZnS沉淀上滴加CuSO4溶液,沉淀变为黑色,说明Ksp(ZnS)<Ksp(CuS)
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)如图是由4个碳原子结合成的6种有机物(氢原子没有画出):
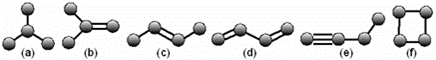
①写出有机物(a)的系统命名法的名称 ;
②上述有机物中与(c)互为同分异构体的是 (填序号);
③任写一种与(e)互为同系物的有机物的结构简式 ;
④上述有机物中不能与溴水反应使其褪色的有 (填序号).
(2)某有机物含C、H、O、N四种元素,质量分数分别为32%、6.66%、42.67%、18.67%.该有机物的蒸汽对氢气的相对密度为37.5.通过计算确定:
①该有机物的分子式 ;
②写出该有机物可能的一种同分异构体的结构简式 、.
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高一上第二次段考化学试卷(解析版) 题型:填空题
铁和铜是生活中两种常见的金属材料,某同学查阅资料得知铁主要是由铁矿石经热还原的方法冶炼的,常见的铁矿石有磁铁矿、赤铁矿、黄铁矿(主要成分为FeS2)等。
(1)赤铁矿的主要成分为__________(填化学式),工业上用一氧化碳还原赤铁矿冶炼铁的化学反应方程式为________________;
(2)从矿物资料查得,一定条件下自然界存在如下反应:
14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4;(已知FeS2中Fe显+2价)
该反应中氧化剂是_____(填化学式),当有5molFeS2发生反应时,电子转移数为________;
(3)印刷电路板是由高分子材料和铜箔复合而成,刻制印刷电路时,用FeCl3溶液作“腐蚀液”,请写出刻制过程的离子方程式__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com