
【题目】NA是阿伏加德罗常数的值,下列说法正确的是
A. 1.9gH3O+中含质子总数为NA
B. 体积均为22.4L(标准状况)的乙烯和乙酸含氢原子数均为4NA
C. 1L0.1mol·L-1NH4A1(SO4)2溶液中阳离子总数小于0.2NA
D. 当反应MgO+C+Cl2![]() MgCl2+CO中断裂2 mol Cl-Cl键时,转移电子总数为4NA
MgCl2+CO中断裂2 mol Cl-Cl键时,转移电子总数为4NA
【答案】D
【解析】
A. 1.9gH3O+的物质的量为0.1mol,含有1.1mol质子,含有的质子数为1.1NA,故A错误;
B. 标况下乙酸不是气体,不能使用标况下的气体摩尔体积计算,故B错误;
C. NH4A1(SO4)2溶液中NH4+和Al3+发生水解,其中Al3+水解反应为:Al3++3H2O![]() Al(OH)3+3H+,由此可知阳离子数目增加,所以1L0.1mol·L-1NH4A1(SO4)2溶液中阳离子总数大于0.2NA,故C错误;
Al(OH)3+3H+,由此可知阳离子数目增加,所以1L0.1mol·L-1NH4A1(SO4)2溶液中阳离子总数大于0.2NA,故C错误;
D. 由反应式MgO+C+Cl2![]() MgCl2+CO可知,Cl2得电子,断裂2 mol Cl-Cl键即有2mol Cl2参加反应,转移电子总数为2
MgCl2+CO可知,Cl2得电子,断裂2 mol Cl-Cl键即有2mol Cl2参加反应,转移电子总数为2![]() 2 NA =4NA,故D正确。
2 NA =4NA,故D正确。
答案选D。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】已知反应:2NO2(红棕色)![]() N2O4(无色)△H<0。将一定量的NO2充入注射器中后封口,下图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法正确的是
N2O4(无色)△H<0。将一定量的NO2充入注射器中后封口,下图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法正确的是

A. b点的操作是拉伸注射器
B. d点:v(正)< v(逆)
C. c点与a点相比,c(NO2)增大,c(N2O4)减小
D. 若不忽略体系温度变化,且没有能量损失,则T(b)>T(c)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 1mol—OH含10NA个电子
B. 1molC2H518OH与足量CH3COOH充分反应可得NA个H2O
C. 标准状况下,11.2L丙烯所含的极性共价键数为3NA
D. 常温下,将1mol铁加入到足量的浓硝酸中,生成NO2气体的体积大于67.2L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸晶体的组成可表示为H2C2O4·xH2O,为了测定x值,进行下述实验:
①称取n g草酸晶体配成100.00 mL水溶液;
②取25.00 mL所配制的草酸溶液置于锥形瓶中,加稀硫酸,用浓度为a mol·L-1的KMnO4溶液滴定,试回答下列问题:
(1)写出滴定实验中所发生反应的化学方程式:_______________
(2)实验中KMnO4溶液应装在____式滴定管中,滴定终点的判断依据是________________
(3)滴定过程中用去V mL a mol·L-1的KMnO4溶液,则所配制的草酸的物质的量浓度为_______mol·L-1
(4)若滴定终点读数时目光俯视,则计算出的x值可能___________(填偏大、偏小、无影响)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知298K时,Ksp(NiS)=1.0×10-21,Ksp(NiCO3)=1.0×10-7 ;p(Ni)=-lg c(Ni2+),p(B)=-lg c(S2-)或-lg c(CO32-)。在含物质的量浓度相同的Na2S和Na2CO3的混合溶液中滴加Ni(NO3)2溶液产生两种沉淀,溶液中阳离子、阴离子浓度关系如图所示。下列说法错误的是( )
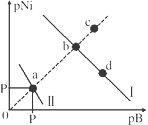
A. 对于曲线I,在b点加热,b点向c点移动
B. 常温下NiCO3的溶解度大于NiS的溶解度
C. 向d点对应的溶液中加入对应阴离子的钠盐,d点向b点移动
D. P为3.5且对应的阴离子是CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,用HCl气体或NaOH固体调节0.01mol·L-1二元酸(以H2A表示)溶液的pH(忽略溶液体积的变化),溶液中H2A、HA-、A2-、H+、OH-浓度的对数值(lgc)变化如下图所示:
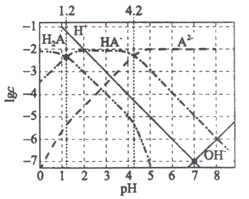
下列说法错误的是
A. 25℃时,H2A的Ka1数量级为10-2
B. pH=1.2时,调节溶液pH用的是HCl气体
C. pH=7时,溶液中:c(Na+)=c(HA-)+c(A2-)
D. pH=8时,溶液中:c(A2-)>c(HA-)>c(H2A)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根皮素R( )可应用于面膜、护肤膏霜和精华素中。其中一种合成R的路线如下:
)可应用于面膜、护肤膏霜和精华素中。其中一种合成R的路线如下:

已知
①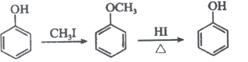
②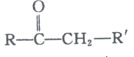 +R’’CHO
+R’’CHO +H2O
+H2O
(1)A的化学名称是___________,B→C的反应类型是___________。
(2)D的结构简式是___________,其核磁共振氢谱共有___________组峰。
(3)E→F的化学方程式为___________,G的官能团的名称是___________。
(4)G→H的化学方程式为______________________。
(5)M是F的同分异构体,同时符合下列条件的M的结构有___________种(不考虑立体异构)
①1能与FeCl3溶液发生显色反应 ②能发生银镜反应
(6)设计以丙烯和1,3-丙二醛为起始原料制备![]() 的合成路线___________(无机试剂任选)。
的合成路线___________(无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化硅(Si3N4)耐高温、硬度大,可用石英与焦炭在1400~1450℃的氮气中合成:3SiO2(s)+6C(s)+2N2(g)=Si3N4(s)+6CO(g)-Q(Q>0),在一定条件下,向10L密闭容器中加入反应物,10min后达到平衡。完成下列问题:
(1)上述反应所涉及的属于第三周期的元素,其原子的最外层电子轨道表示式为______。其中一种元素的原子核外s电子数与p电子数相等,其原子的核外电子能量不同的有_____种。
(2)上述反应混合物中的极性分子是______,写出非极性分子的电子式________。分析用氮化硅制造轴承和发动机中耐热部件的原因是___________。
(3)该反应的平衡常数表达式为__________。可以提高二氧化硅转化率的措施是________(任写一条),该措施对平衡常数的影响为__________(填“增大”、“减小”或“保持不变”)。
(4)测得平衡时固体质量减少了5.6g,则用氮气表示的平均反应速率为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯化六氨合钴[Co(NH3)6]Cl3 是橙黄色、微溶于水的配合物,是合成其它一些含钴配合物的原料。下图是某科研小组以含钴废料(含少量Fe、Al 等杂质)制取[Co(NH3)6]Cl3 的工艺流程:

回答下列问题:
(1)写出加“适量NaClO3”发生反应的离子方程式______________。
(2)“加Na2CO3 调pH至a”会生成两种沉淀,分别为_______________________(填化学式)。
(3)操作Ⅰ的步骤包括_____________________________、冷却结晶、减压过滤。
(4)流程中NH4Cl除作反应物外,还可防止加氨水时c(OH-) 过大,其原理是_________________。
(5)“氧化”步骤,甲同学认为应先加入氨水再加入H2O2,乙同学认为试剂添加顺序对产物无影响。你认为___________(填“甲”或“乙”)同学观点正确,理由是_________________________________。写出该步骤的化学方程式:________________________________
(6)通过碘量法可测定产品中钴的含量。将 [Co(NH3)6]Cl3 转化成Co3+后,加入过量KI 溶液,再用Na2S2O3标准液滴定(淀粉溶液做指示剂),反应原理:2Co3++2I-=2Co2++I2,I2+2S2O32-=2I-+S4O62-,实验过程中,下列操作会导致所测钴含量数值偏高的是_______。
a.用久置于空气中的 KI 固体配制溶液
b.盛装Na2S2O3标准液的碱式滴定管未润洗
c.滴定结束后,发现滴定管内有气泡
d.溶液蓝色退去,立即读数
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com