
 氧化还原反应在生产、生活中具有广泛的用途,贯穿古今.
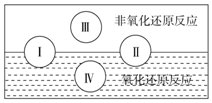
氧化还原反应在生产、生活中具有广泛的用途,贯穿古今.分析 (1)发生的反应中含元素的化合价变化,为氧化还原反应;
(2)由图可知,Ⅳ为氧化还原反应,且属于置换反应;
(3)Cu由+2价降低为0,N元素的化合价由-3价升高为0,由电子守恒、原子守恒分析;
(4)将铜丝浸入稀硫酸中并不断地从容器下部吹入细小的空气泡,发生2Cu+2H2SO4+O2=2CuSO4+2H2O,反应无污染,符合原子经济的要求;
(5)K2Cr2O7+14HCl═2KCl+2CrCl3+3Cl2↑+7H2O反应中,在参加反应的14mol盐酸中,被氧化的HCl为6mol,转移电子的物质的量为6mol,14.6gHCl的物质的量为:$\frac{14.6g}{36.5g/mol}$=0.4mol,由此分析解答.
解答 解:(1)A.煤的形成发生复杂的物理化学变化,C元素的化合价一定变化,为氧化还原反应,故A不选;
B.鞭炮燃放是化学变化,故B不选;
C.简单机械织布,为物理变化,故C选;
D.烧制陶瓷发生复杂的物理化学变化,存在氧化过程,涉及氧化还原反应,如涉及碳的燃烧等,故D不选;
故答案为:C;
(2)由图可知,Ⅳ为氧化还原反应,且属于置换反应,如2Na+2H2O=2NaOH+H2↑,离子反应方程式为:2Na+2H2O=2Na++2OH-+H2↑,水中H元素的化合价降低,则水为氧化剂,
故答案为:2Na+2H2O=2Na++2OH-+H2↑;氧化;
(3)①Cu由+2价降低为0,N元素的化合价由-3价升高为0,由电子守恒、原子守恒可知,NH4Cl失去3个电子,而铜得到2个电子,得失电子守恒,NH4Cl前面系数为2,铜前面的系数为3,再结合原子守恒可知,反应为4CuO+2NH4Cl=3Cu+CuCl2+N2+4H2O,
故答案为:4;2;3;1;1;4;
②N元素失去电子被氧化,Cu元素得到电子,则CuO为氧化剂,故答案为:氮;CuO;
(4)将铜丝浸入稀硫酸中并不断地从容器下部吹入细小的空气泡,发生2Cu+2H2SO4+O2=2CuSO4+2H2O,反应无污染,符合原子经济的要求;
①发生反应的化学方程式2Cu+2H2SO4+O2=2CuSO4+2H2O,故答案为:2Cu+2H2SO4+O2=2CuSO4+2H2O;
②这样做的好处是反应物完全转化成生成物,提高H2SO4的利用率;反应无污染,而浓硫酸与铜在加热条件下反应生成SO2和硫酸铜,产生污染大气的SO2;反应在常温下就能进行,而浓硫酸与铜在加热条件下反应,节省能源,
故答案为:无污染,高H2SO4的利用率;节省能源;
(5)K2Cr2O7+14HCl═2KCl+2CrCl3+3Cl2↑+7H2O反应中,在参加反应的14mol盐酸中,被氧化的HCl为6mol,转移电子的物质的量为6mol,14.6gHCl的物质的量为:$\frac{14.6g}{36.5g/mol}$=0.4mol,故答案为:0.4mol.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,注意从化合价角度分析,侧重氧化还原反应中基本概念及转移电子的考查,题目难度不大.


 出彩同步大试卷系列答案
出彩同步大试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 同温同压下,相同质量的NO和C2H4 (气体)体积相同 | |
| B. | 同温同压下,相同体积的H2和CO2的原子数之比为2:3 | |
| C. | 同温同压下,气体的密度之比等于摩尔质量之比 | |
| D. | 同温同体积的气体,若物质的量相同则压强相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 0.1mol/L的NaHA其PH=1,溶液中存在:c(Na+)+c(H+)=c(OH-)+2c(A2-)+c(HA-) | |
| B. | 40%的醋酸溶液(p=1.049gcm-3)与60%的醋酸溶液(p=1.064gcm-3)等体积混合后,所得溶液中溶质的质量分数大于50% | |
| C. | 0.1mol/L的醋酸溶液V1L和等浓度的氢氧化钠溶液V2L混合后呈碱性,则一定有V1≤V2 | |
| D. | 1L0.5mol/LFeCl3的溶液与0.2L1mol/LKCl溶液中Cl-数目之比为15:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ②③ | C. | ①③ | D. | ①② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1:1 | B. | 4:2:1 | C. | 2:3:4 | D. | 6:3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 大气中的SO2、NO2是酸性氧化物,与酸雨的形成密切相关 | |
| B. | 氢氧化铝常用于治疗胃酸过多,过量服用会造成重金属中毒 | |
| C. | 制豆腐时向豆浆中加入硫酸钙使蛋白质等聚沉,可制成豆腐 | |
| D. | 氢氧燃料电池是一种高能电池,释放的电能与等量氢气完全燃烧释放的热能相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
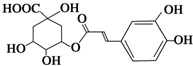 从金银花中提取的绿原酸结构简式如图所示.其有抗菌、消炎、解毒.利胆.降压和增加胃肠蠕动的作用.用于急性细菌性感染及放、化疗所致的白细胞减少症.下列说法不正确的是( )
从金银花中提取的绿原酸结构简式如图所示.其有抗菌、消炎、解毒.利胆.降压和增加胃肠蠕动的作用.用于急性细菌性感染及放、化疗所致的白细胞减少症.下列说法不正确的是( )| A. | 绿原酸的分子式为C16H18O9 | |
| B. | 绿原酸及其水解产物之一在空气中均能稳定存在,遇FeCl3溶液时显紫色 | |
| C. | 1mol绿原酸与NaOH溶液反应时,最多消4molNaOH | |
| D. | 1mol绿原酸与足量金属Na反应时能产生3molH2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com