
| A. | ①② | B. | ①④ | C. | ②③ | D. | ③④ |
分析 ①检验氯离子,需要试剂为硝酸、硝酸银;
②小苏打与醋酸反应生成气体,而食盐不能;
③蛋壳中的碳酸钙与醋酸反应生成气体;
④无水硫酸铜遇水变蓝,可检验水.
解答 解:①检验氯离子,需要试剂为硝酸、硝酸银,则家庭厨房中的物质不能检验,故不选;
②小苏打与醋酸反应生成气体,而食盐不能,可利用厨房中的醋酸检验,故选;
③蛋壳中的碳酸钙与醋酸反应生成气体,可利用厨房中的醋酸检验,故选;
④无水硫酸铜遇水变蓝,可检验水,则家庭厨房中的物质不能检验,故不选;
故选C.
点评 本题考查物质的鉴别和检验,为高频考点,把握物质的性质、发生的反应和现象为解答的关键,侧重分析与应用能力的考查,注意厨房实验的化学试剂,题目难度不大.


 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源: 题型:选择题
| 混合物 | 非电解质 | 碱 | 酸式盐 | |
| A | 漂白粉 | 氯气 | 氨水 | 碳酸氢钠 |
| B | 福尔马林 | 苯 | 碱式碳酸铜 | 明矾 |
| C | 胆矾 | 二氧化硫 | 纯碱 | 氯化铵 |
| D | 食醋 | 乙醇 | 苛性钠 | 硫酸氢钠 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
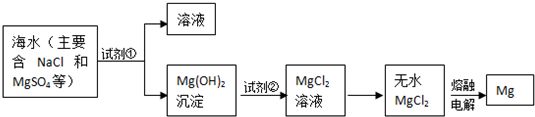
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 饱和Na2S溶液 | B. | 饱和NaHCO3溶液 | C. | 饱和NaHS溶液 | D. | 饱和NaCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 己烷有4种同分异构体,它们的熔点、沸点各不相同 | |
| B. | 甲醛能发生氧化反应、还原反应和聚合反应 | |
| C. | 油脂皂化反应得到高级脂肪酸盐与甘油 | |
| D. | 聚合物(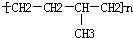 )可由单体CH3CH=CH2和CH2=CH2加聚制得 )可由单体CH3CH=CH2和CH2=CH2加聚制得 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲苯分子中的所有原子可能共平面 | |
| B. | 苯乙烯分子中的所有原子一定共平面 | |
| C. | 二氯甲烷分子为正四面体结构 | |
| D. | 乙烷分子中的所有原子不可能共平面 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | BaCl2→Na2CO3→HCl | |
| B. | 过量的BaCl2→过量的Na2CO3→足量的HCl | |
| C. | 过量的Ba(NO3)2→过量的Na2CO3→HCl | |
| D. | Ba(OH)2→Na2CO3→HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蛋白质、纤维素、蔗糖、PVC、淀粉都是高分子化合物 | |
| B. | 使用太阳能热水器、沼气的利用、玉米制乙醇都涉及到生物质能的利用 | |
| C. | 氢键在形成蛋白质二级结构和DNA双螺旋结构中起关键作用 | |
| D. | 石油、煤、天然气、可燃冰、生物柴油都属于化石燃料 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com