
����Ŀ����֪������±�����ڴ����������¿��������������±���⣬A��ˮ���Ĵ������C�������г������л���ұ��ܱ����Ը��������Һ����Ϊ�����ᣮ��������֮���ת����ϵ��ͼ��ʾ�����������������������ȥ���� 
��ش��������⣺
��1��д�����ʵĽṹ��ʽ��A��C��E ��
��2���ڢ١���6����Ӧ�У�������ȥ��Ӧ���������ţ���
��3��д�����з�Ӧ�Ļ�ѧ����ʽ��
����
����
�� ��
H��I��Ӧ����ʽΪ ��
���𰸡�
��1��CH2�TCH2��CH3CH2OH��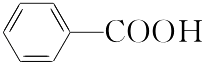
��2���ڢ�
��3��![]() ��CH3CH2OH
��CH3CH2OH ![]() CH2�TCH2��+H2O��
CH2�TCH2��+H2O��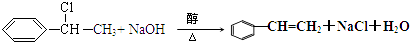 ��
��![]()
![]()

���������⣺A��ˮ���Ĵ������AΪCH2=CH2��C�������г������л���ܷ�����Ӧ����A����Ϸ�Ӧ����֪��CΪCH3CH2OH��A��HCl�����ӳɷ�Ӧ����B��B�ܷ�����ȥ��Ӧ����A����BΪCH3CH2Cl��B������Ӧ����D��D����һϵ�з�Ӧ����I��H�����Ӿ۷�Ӧ����H����D��H��̼ԭ�Ӹ�������8��B����ȡ����Ӧ����D����DΪ ![]() ��D����������Ӧ����EΪ
��D����������Ӧ����EΪ ![]() ��C��E����������Ӧ����F������F��Է�������֪��F�ṹ��ʽΪ
��C��E����������Ӧ����F������F��Է�������֪��F�ṹ��ʽΪ ![]() �� D����ȡ����Ӧ����G��G����ȡ����Ӧ����
�� D����ȡ����Ӧ����G��G����ȡ����Ӧ���� ![]() ����GΪ
����GΪ ![]() ��G������ȥ��Ӧ����HΪ
��G������ȥ��Ӧ����HΪ ![]() ��H�����Ӿ۷�Ӧ���ɸ߾���IΪ
��H�����Ӿ۷�Ӧ���ɸ߾���IΪ 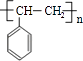 ����1��ͨ�����Ϸ���֪��A��C��E�ṹ��ʽ�ֱ�ΪCH2�TCH2��CH3CH2OH��
����1��ͨ�����Ϸ���֪��A��C��E�ṹ��ʽ�ֱ�ΪCH2�TCH2��CH3CH2OH�� 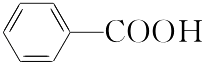 �����Դ��ǣ�CH2�TCH2��CH3CH2OH��
�����Դ��ǣ�CH2�TCH2��CH3CH2OH�� 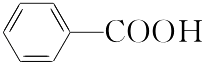 ����2���ڢ١���6����Ӧ�У�������ȥ��Ӧ���Ǣڢޣ����Դ��ǣ��ڢޣ���3����Ϊ������ͱ���ȡ����Ӧ����Ӧ����ʽΪ��
����2���ڢ١���6����Ӧ�У�������ȥ��Ӧ���Ǣڢޣ����Դ��ǣ��ڢޣ���3����Ϊ������ͱ���ȡ����Ӧ����Ӧ����ʽΪ�� ![]() ����Ϊ�Ҵ�����ȥ��Ӧ����Ӧ����ʽΪCH3CH2OH
����Ϊ�Ҵ�����ȥ��Ӧ����Ӧ����ʽΪCH3CH2OH ![]() CH2�TCH2��+H2O����Ӧ����ʽΪ
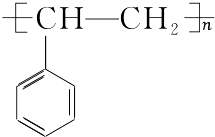
CH2�TCH2��+H2O����Ӧ����ʽΪ 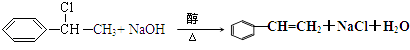 �� H��I��Ӧ����ʽΪ��
�� H��I��Ӧ����ʽΪ�� 
![]()
 �����Դ��ǣ�
�����Դ��ǣ� ![]() �� CH3CH2OH
�� CH3CH2OH ![]() CH2�TCH2��+H2O��
CH2�TCH2��+H2O�� 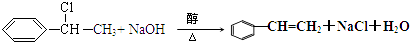 ��
�� 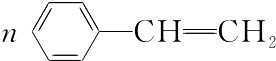
![]()
 ��
��


 ��ʦָ����ĩ��̾�ϵ�д�
��ʦָ����ĩ��̾�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������е����Ų�ʽ�жϣ����ڼ���̬��ԭ����
A. 1s22s22p6B. 1s22s22p63s1C. 1s22s23s1D. [Ar]3d14s2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����϶���������HEV����ʹ���������أ��乤��ԭ����ͼ��ʾ�� ����MΪ����Ͻ�MHΪ��������ԭ�ӵĴ���Ͻ�KOH��Һ�����Һ�����������أ�����˵������ȷ���ǣ� ��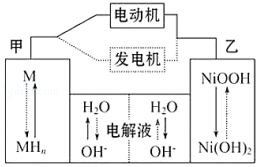
A.���ʱ����������pH����
B.�綯������ʱ��Һ��OH������ƶ�
C.�ŵ�ʱ������ӦʽΪ��NiOOH+H2O+e���TNi��OH��2+OH��
D.�缫�ܷ�ӦʽΪ��MH+NiOOH ![]() M+Ni��OH��2
M+Ni��OH��2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������X�ķ���ʽΪC5H11Cl����NaOH�Ĵ���Һ����X���ɵ÷���ʽΪC5H10�����ֲ���Y��Z��Y��Z��������ɵõ�2�����飮����������X��NaOH��ˮ��Һ�������������л�����Ľṹ��ʽ�����ǣ� ��
A.CH3CH2CH2CH2CH2OH
B.��CH3��2COHCH2CH3
C.��CH3��2CHCH2CH2OH
D.��CH3��3CCH2OH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ӦCH3OH��l��+NH3��g��CH3NH2��g��+H2O��g���ڸ��¶�ʱ�����Է����У���÷�Ӧ���̵ġ�H����S�ж���ȷ���ǣ� ��
A.��H��0����S��0
B.��H��0����S��0
C.��H��0����S��0
D.��H��0����S��0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����100mlij���ʵ���Ũ�ȵ�NaOH��Һ�л���ͨ��һ������CO2 �� ��ַ�Ӧ����������Һ����ε���1mol/L��������Һ������������������״̬������������������ϵ��ͼ��ʾ
��1��д��OA+�η�����Ӧ�����ӷ���ʽ����
��2����Ӧ��B��ʱ������Һ�е���������
��3��ԭNaOH��Һ�����ʵ���Ũ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijǿ������ҺX����Ba2+��Al3+��NH4+��Fe2+��Fe3+��CO32����SO32����SO42����Cl����NO3���е�һ�ֻ��֣�ȡ����Һ��������ʵ�飬ʵ���������£� 
����������Ϣ���ش��������⣺
��1����Ӧ�۵Ļ�ѧ����ʽΪ ��
��2������C��H������F�Ļ�ѧʽ�ֱ�Ϊ ��
��3��д���йط�Ӧ�����ӷ���ʽ����������A �� �� ��
��4�����������У���ҺX�п϶������е������� �� ���ܺ��е������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ɻ��õ������������泥�NH4ClO4���Ļ����Ϊ����ȼ�ϣ���ȼʱ����������������������立�Ӧ���䷽��ʽ�ɱ�ʾΪ��2NH4ClO4 ![]() N2��+4H2O+Cl2��+2O2�����ų�����ΪQ�����жԴ˷�Ӧ�����д�����ǣ� ��
N2��+4H2O+Cl2��+2O2�����ų�����ΪQ�����жԴ˷�Ӧ�����д�����ǣ� ��
A.��Ӧ���ڷֽⷴӦ
B.������Ӧ˲������������������ƶ�����ɻ�����
C.��Ӧ�������仯��˵����Ҫ�ǻ�ѧ��ת��Ϊ���ܺͶ���
D.�ڷ�Ӧ�и������ֻ������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NH3�����ζ�����Ҫ�Ļ���ԭ�ϣ� 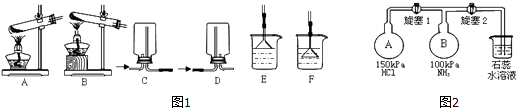
��1����NH4Cl��Ca��OH��2�Ʊ�NH3�Ļ�ѧ����ʽΪ���÷�Ӧ�����������ռ���β������װ����ͼ1����Ϊ��
��2������ͼ2װ�ý���NH3����ʵ�飮�ȴ�����1��Bƿ�е������� �� �ȶ��ر�����1���ٴ�����2��Bƿ�е���������
��3��д��NH4Cl��Һˮ������ӷ���ʽ��
���ʵ�飬̽��ijһ�����ض���Һ��NH4Clˮ��̶ȵ�Ӱ�죮
��ѡ�Լ�������������NH4Cl������ˮ��250mL����ƿ���ձ�����ͷ�ιܡ���������ҩ�ס���ƽ��pH�ơ��¶ȼơ�����ˮԡ�ۣ��ɵ����¶ȣ�
��ʵ��Ŀ�ģ�̽������Һ��NH4Clˮ��̶ȵ�Ӱ�죻
�����ʵ�鷽�����ⶨʵ�������������ʵ�鷽�����г���ֱ�Ӷ�ȡ���ݵ���������������ⶨ�����ݣ���������ĸ��ʾ�����С�V����Һ������ʾ��������Һ���������
������ | V����Һ��/mL | NH4Cl����/g | �¶�/�� | �� | |
1 | 250 | X | �� | ||
2 | 250 | �� |
�۰�ʵ�����1�������ݽ���ʵ�飬����ȡ�Ĵ�������������ֵΪX����NH4Clˮ�ⷴӦ��ƽ��ת����Ϊ��ֻ�г���ʽ������ˮ���������Ӱ�죩��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com