
【题目】在恒温条件下将一定量X和Y的混合气体通入一容积为2L的密闭容器中,X和Y两物质的浓度随时间变化情况如图。

(1)该反应的化学方程式为(反应物或生成物用符号X、Y表示):_________________________。
(2)a、b、c、d四个点中,表示化学反应处于平衡状态的点是________________。
素材1:某温度和压强下,2L容器中,发生反应2SO2+O2![]() 2SO3,不同时间点测得密闭体系中三种物质的物质的量如下:
2SO3,不同时间点测得密闭体系中三种物质的物质的量如下:
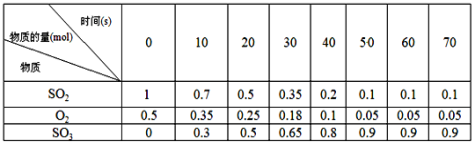
素材2:反应在不同条件下进行时SO2的转化率:(SO2的转化率是反应的SO2占起始SO2的百分数,SO2的转化率越大,化学反应的限度越大)
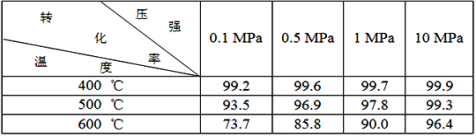
根据以上的两个素材回答问题:
(3)根据素材1中计算20~30s期间,用二氧化硫表示的化学反应平均速率为________。
(4)根据素材2中分析得到,提高该化学反应限度的途径有_______________。
(5)根据素材1、素材2中分析得到,要实现素材1中SO2的转化率需控制的反应具体条件是__________________。
【答案】Y![]() 2X bd 0.0075mol·L-1·s-1 增大压强或(在一定范围内或适当)降低温度 温度为600℃,压强为1MPa
2X bd 0.0075mol·L-1·s-1 增大压强或(在一定范围内或适当)降低温度 温度为600℃,压强为1MPa
【解析】
结合反应物和生成物的浓度变化量与化学计量数成正比解题;根据平衡状态的特征分析;利用速率公式、转化率公式计算。
(1)由图可知,X的物质的量增加,Y的物质的量减少,则X为生成物,Y为反应物,由10mim达到平衡可知,Y、X的浓度变化量之比为(0.6-0.4)mol/L:(0.6-0.2)mol/L=1:2,则反应方程式为:Y2X;
(2)由图可知,10-25min及35min之后X、Y的物质的量不发生变化,则相应时间段内的点处于化学平衡状态,即b、d处于化学平衡状态,故答案为:b、d;
(3)由素材1可知,20-30s内二氧化硫的物质的量的变化量为0.5mol-0.35mol=0.15mol,
则二氧化硫表示的化学反应的平均速率为 =0.0075 molL-1s-1;
=0.0075 molL-1s-1;
(4)由素材2可知,压强越大、温度越低时有利于提高该化学反应限度,但温度太低时反应速率较慢,则提高该化学反应限度的途径有增大压强或在一定范围内降低温度;
(5)由素材1可知,50s时反应达到平衡,则二氧化硫的转化率为![]() =90%,结合素材2可知,转化率为90%时温度为600℃,压强为1MPa。
=90%,结合素材2可知,转化率为90%时温度为600℃,压强为1MPa。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】硫酸铁铵[NH4Fe(SO4)2·xH2O]是一种重要铁盐。为充分利用资源,变废为宝,在实验室中探究采用废铁屑来制备硫酸铁铵,具体流程如下:
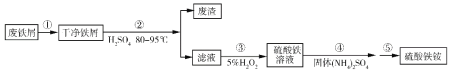
回答下列问题:
(1)步骤①的目的是去除废铁屑表面的油污,方法是_________________。
(2)步骤②需要加热的目的是_________________,温度保持80~95 ℃,采用的合适加热方式是_________________。铁屑中含有少量硫化物,反应产生的气体需要净化处理,合适的装置为_________________(填标号)。
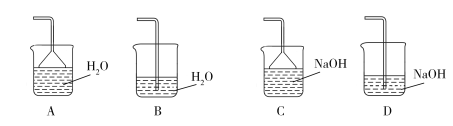
(3)步骤③中选用足量的H2O2,理由是_________________。分批加入H2O2,同时为了_________________,溶液要保持pH小于0.5。
(4)步骤⑤的具体实验操作有______________,经干燥得到硫酸铁铵晶体样品。
(5)采用热重分析法测定硫酸铁铵晶体样品所含结晶水数,将样品加热到150 ℃时,失掉1.5个结晶水,失重5.6%。硫酸铁铵晶体的化学式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有V、W、X、Y、Z五种元素,它们的核电荷数依次增大,且都小于20。其中只有X、Z是金属元素;V元素的一种核素原子核内无中子,Z元素原子的最外层只有一个电子;W和Y元素原子的最外层电子数相同,且W元素原子L层电子数是K层电子数的3倍;X元素原子的最外层电子数是Y元素原子最外层电子数的一半。回答下列问题:
(1)V的一种核素中质子数为中子数的1/2,则该核素的名称为____。
(2)Z的元素符号为____。
(3)X元素的离子结构示意图为___。
(4)Y的单质在加热条件下与铁反应的化学方程式为____。
(5)W元素的原子结构示意图为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.一定条件下,反应室(容积恒定为2L)中有反应:A(g)+2B(g)![]() C(g)。
C(g)。
(1)能说明上述反应达到平衡状态的是________(填字母,下同)。
A.反应中A与B的物质的量浓度之比为1∶2 B.混合气体总物质的量不再变化
C.混合气体的密度不随时间的变化而变化 D.2v正(A)=v逆(B)
(2)1molA(g)与2molB(g)在催化剂作用下在反应室反应生成C(g),A的平衡转化率与温度、压强的关系如图所示:
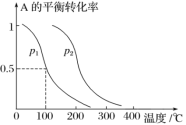
①p1________p2(填“<”、“>”或“=”,下同),正反应的ΔH________0。
②下列措施中一定能使![]() 增大的是________。
增大的是________。
A.升高温度B.恒温恒容再充入A
C.恒温恒容再充入BD.恒温恒容再充入1molC
(3)100℃时将1molA和2molB通入反应室,保持温度不变,10min末C(g)的浓度为0.05mol·L-1,则10min末B的转化率为_____,此时v正_____v逆(填“<”、“>”或“=”)。
II.一定温度下,在容积为VL的密闭容器中进行反应:aN(g)![]() bM(g),M、N的物质的量随时间的变化曲线如图所示:
bM(g),M、N的物质的量随时间的变化曲线如图所示:

(1)此反应的化学方程式中![]() =____________。
=____________。
(2)t1到t2时刻,以M的浓度变化表示的平均反应速率为____________。
(3)下列叙述能说明上述反应达到平衡状态的是____________(填字母)。
A.反应中M与N的物质的量之比为1∶1
B.混合气体的总质量不随时间的变化而变化
C.混合气体的总物质的量不随时间的变化而变化
D.单位时间内消耗amolN,同时生成bmolM
E.混合气体的压强不随时间的变化而变化
F.混合气体的平均相对分子质量不随时间的变化而变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所学知识,回答下列问题:
(1)“元时,南安有黄长者,为宅煮糖,宅垣忽坏,去土而糖白,后人遂效之。”泥土能将红糖变白糖,其表现的性质是__________。
(2)用鸡蛋壳膜和蒸馏水可除去淀粉胶体中的食盐,其原理是______________。
(3)欲使![]() 全部转化为
全部转化为![]() ,则需要氧化剂
,则需要氧化剂![]() (还原产物为
(还原产物为![]() )至少_______
)至少_______![]() 。
。
(4)下列变化为化学变化的是_________(填字母)。
A.![]() 的潮解 B.铁的生锈 C.新制氯水久置后颜色变浅
的潮解 B.铁的生锈 C.新制氯水久置后颜色变浅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯水中含有多种成分,因而具有多种性质,根据新制氯水分别与如图四种物质发生的反应填空(a、b、c、d、e中重合部分代表物质间反应,且氯水足量)。
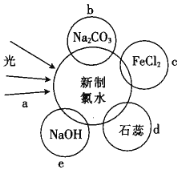
(1)氯水中含有的粒子有![]() 、
、![]() 、______、
、______、![]() 、
、![]() 、______、
、______、![]() 七种。
七种。
(2)久置的氯水变为_____________,原因是___________________________(用化学反应方程式表示)。
(3)b过程中的离子方程式是_______________________。
(4)e过程中所发生的主要反应的化学方程式为____________________________。
(5)能证明氯水具有漂白性的是______________________(填“a”“b”“c”或“d”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CH4-CO2催化重整不仅可以得到合成气(CO和H2),还对温室气体的减排具有重要意义。回答下列问题:
(1)CH4-CO2催化重整反应为:CH4(g)+CO2(g)![]() 2CO(g)+2H2(g)ΔH。
2CO(g)+2H2(g)ΔH。
已知:C(s)+2H2(g)=CH4(g)ΔH=-75kJ·mol1
C(s)+O2(g)=CO2(g)ΔH=-394kJ·mol1
C(s)+![]() O2(g)=CO(g)ΔH=-111kJ·mol1
O2(g)=CO(g)ΔH=-111kJ·mol1
该催化重整反应的ΔH=________kJ·mol1。有利于提高CH4平衡转化率的条件是____(填标号)。
A.高温低压B.低温高压C.高温高压D.低温低压
某温度下,在体积为2L的容器中加入2molCH4、1molCO2以及催化剂进行重整反应,达到平衡时CO2的转化率是50%,其平衡常数为___________________________。
素材1:研究人员研制出一种锂水电池,可作为鱼雷和潜艇的储备电源。该电池以金属锂和钢板为电极材料,以LiOH为电解质,使用时加入水即可放电。总反应为:2Li+2H2O===2LiOH+H2↑。根据以上素材回答下列问题:
(2)该电池的负极是________,负极反应式是_____________________________。
(3)正极现象是_______________________________________________。
(4)放电时OH-向_____________(填“正极”或“负极”)移动。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家开发出了多种太阳能电池,除晶体硅太阳能电池外,还有GaAs太阳能电池、铜铟镓硒薄膜太阳能电池等。
(1)基态Ga原子的电子排布式为___。
(2)高温下CuO容易转化为Cu2O,试从原子结构角度解释原因___。
(3)与SeO3互为等电子体的两种阴离子___(写化学式)。
(4)AsF3是极性分子,理由是___。
(5)金刚砂(SiC)晶胞如图所示:

①金刚砂中硅原子的杂化轨道类型为___,沿晶胞图中虚线方向的切面图为___(填标号)。

②若晶胞参数为apm,阿伏加德罗常数为NA,则金刚砂的密度为___g·cm-3(列出表达式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D四种易溶于水的化合物只由表中的八种离子组成,且四种化合物中阴、阳离子各不相同。
阴离子 | Cl-、SiO32-、OH-、NO3- |
阳离子 | H+、Ag+、Na+、K+ |
已知:A溶液呈强酸性,且A溶液与B、C溶液混合均产生白色沉淀,B的焰色反应呈黄色。
回答下列问题:
(1)写出A、B、C、D的化学式:A______,B_____,C____,D____。
(2)写出A溶液与B溶液反应的离子方程式: __________。
(3)请选出适合存放A、C、D溶液的试剂瓶的序号:
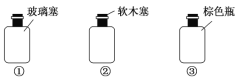
溶液 | A | C | D |
试剂瓶序号 | ___ | ___ | ___ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com