
【题目】Ⅰ.(1)Fe2(SO4)3(写出电离方程式)_____
(2)铝和氢氧化钠溶液混合(写出反应的离子方程式)_____
(3)2H++CO32﹣═H2O+CO2↑(改写成化学方程式)________
(4)除去NaHCO3溶液中混有少量 Na2CO3溶液的离子反应方程式_____.
Ⅱ.有一瓶溶液只含Cl﹣、CO32﹣、SO42﹣、Na+、Mg2+、Cu2+六种离子中的某几种通过实验:
①原溶液![]() 白色沉淀;
白色沉淀;
②原溶液中加BaCl2溶液不产生沉淀;
③原溶液中加AgNO3溶液产生白色沉淀,再加稀硝酸白色沉淀不溶解.
(1)试分析原溶液中一定含有的离子是_____,一定不含有的离子是_____,
(2)有的同学认为实验③可以省略,你认为是否正确_____(填是或否),理由是_____.
【答案】Fe2(SO4)3=2 Fe3++3SO42﹣ 2Al+2OH-+2H2O=2AlO2-+3H2↑ 2HCl+ Na2CO3═H2O+CO2↑+2 NaCl H2O+CO2+CO32﹣═2HCO3﹣ 一定含有Mg2+、Cl﹣ 一定不含有CO32﹣、SO42﹣、Cu2+ 是 溶液呈电中性,必须同时含有阴、阳离子,故一定有Cl﹣
【解析】
Ⅰ.(1)为强电解质完全电离,Fe2(SO4)3电离方程式:Fe2(SO4)3==2 Fe3++3SO42﹣;
(2)铝和氢氧化钠溶液混合生成偏铝酸钠和氢气,反应的离子方程式:2Al+2OH-+2H2O=2AlO2-+3H2↑;
(3)2H++CO32﹣═H2O+CO2↑,改写成化学方程式:2HCl+ Na2CO3═H2O+CO2↑+2 NaCl;
(4)除去NaHCO3溶液中混有少量 Na2CO3溶液的离子反应方程式: H2O+CO2+CO32﹣═2HCO3﹣.
Ⅱ.溶液中加入过量NaOH生成白色沉淀,该沉淀应为Mg(OH)2,说明溶液中含有Mg2+,没有Cu2+;原溶液中加BaCl2溶液不产生沉淀,说明溶液中不含CO32-和SO42-,BaCO3和BaSO4都难溶于水,原溶液中加AgNO3溶液产生白色沉淀,再加稀硝酸白色沉淀不溶解,生成的沉淀为AgCl,说明含有Cl-。
(1)由分析可知,原溶液中一定含有的离子是含有Mg2+、Cl-,一定不含有的离子是CO32-、SO42-、Cu2+,通过以上实验不能确定是否含有Na+;
(2)可以省略,溶液中的阴离子不存在CO32-、SO42-,阴离子只有Cl-,根据溶液呈电中性,肯定有Cl-存在。


科目:高中化学 来源: 题型:
【题目】中国人自古就有泡药酒的习惯。药酒多选用50-60度的白酒,将中药材浸泡在酒中,经过一段时间,中药材中的有效成分(主要是有机物)溶解在酒中,此时即可过滤去渣后饮用。泡药酒的原理属于

A.萃取B.结晶C.干燥D.置换
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学学习小组采用下列装置,对浓硝酸与木炭的反应进行探究。
已知:4HNO3![]() 4NO2↑+O2↑+2H2O
4NO2↑+O2↑+2H2O
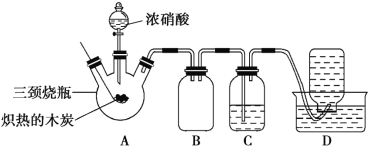
请回答下列问题:
(1)检查装置气密性后,将燃烧匙中的木炭在酒精灯上加热至红热状态,立即伸入三颈烧瓶中,并塞紧瓶塞,滴加浓硝酸,可观察到三颈烧瓶中气体的颜色为____,产生该气体的主要化学反应方程式是_____。
(2)装置C中盛有足量Ba(OH)2溶液,反应一段时间后可观察到C中出现白色沉淀,该白色沉淀为____(填化学式)。其中的Ba(OH)2溶液___(填“能”或“不能”)用Ca(OH)2溶液代替,理由是_____。
(3)装置B的作用是___。
(4)装置D中收集到了无色气体,部分同学认为是NO,还有部分同学认为是O2。
①下列对该气体的检验方法合适的是__(填序号)。
A.敞口观察集气瓶内气体的颜色变化
B.将润湿的蓝色石蕊试纸伸入集气瓶内,观察试纸是否变红
C.将带火星的木条伸入集气瓶中,观察木条是否复燃
②如果集气瓶中收集到的无色气体是氧气,则氧气的来源是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验装置应用于铜与浓硫酸反应制取二氧化硫和硫酸铜晶体,能达到实验目的的是
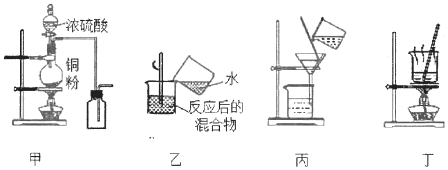
A. 用图甲装置制取并收集二氧化硫
B. 用图乙装置向反应后的混合物中加水稀释
C. 用图丙装置过滤出稀释后混合物中的不溶物
D. 用图丁装置将硫酸铜溶液蒸发结晶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于Na2CO3和 NaHCO3性质的说法正确的是( )
A.相同温度时,在水中的溶解度:NaHCO3>Na2CO3
B.与Ca(OH)2溶液反应:Na2CO3溶液中有白色沉淀生成,NaHCO3溶液中没有沉淀生成
C.热稳定性:NaHCO3>Na2CO3
D.相同物质的量浓度时,溶液的碱性:NaHCO3<Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是
A.向FeBr2溶液中通入少量Cl2:2Br-+ Cl2 = Br2+ 2Cl-
B.向NH4Al(SO4)2溶液中加入过量KOH溶液:Al3+ + 4OH- = AlO2- + 2H2O
C.用氢氧化钠溶液吸收工业废气中的NO2:2NO2 + 2OH- = NO3- + NO2- + H2O
D.用惰性电极电解AlCl3溶液:2Cl- + 2H2O ![]() Cl2↑ + H2↑ + 2OH-
Cl2↑ + H2↑ + 2OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将2.5g碳酸钠、碳酸氢钠和氢氧化钠的固体混合物完全溶解于水,制成稀溶液,然后向该溶液中逐滴加入1mol·L-1的盐酸,所加入盐酸的体积与产生CO2的体积(标准状况)关系如下图所示:
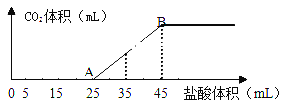
(1)写出OA段所发生反应的离子方程式_____________、___________。
(2)当加入45mL盐酸时,产生CO2的体积为______________mL(标准状况)。
(3)写出碳酸钠溶液呈碱性的原因(用离子方程式表示)_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在实验室中用二氧化锰跟浓盐酸反应制备干燥纯净的氯气。所用仪器如图:
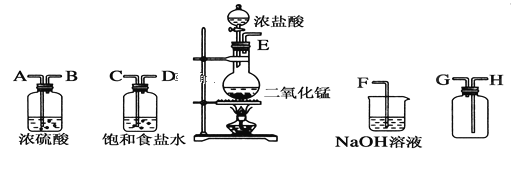
(1)连接上述仪器的正确顺序(填各接口处的字母):__接__;__接__;__接__;__接__。
(2)装置中,饱和食盐水的作用是______________;NaOH溶液的作用是____________。
(3)①气体发生装置中进行反应的化学方程式:_____________________________;该方程式中体现浓盐酸的__________________、____________________ 性质;氧化剂和还原剂的物质的量之比:________________________________________;
②NaOH溶液中发生反应的离子方程式:_______________________________________;
(4)实验室用下列方法制取氯气:①用含4 mol 氯化氢的浓盐酸与足量的二氧化锰反应;②用87 g 二氧化锰与足量浓盐酸反应,若不考虑氯化氢的挥发,则反应后所得氯气的物质的量(_____)
A.①比②多 B.②比①多 C.两种方法一样多 D.无法比较
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙三种不同的物质中均含有同一种元素,它们之间的转化关系如图示(部分反应物及生成物已略去)。下列说法错误的是:
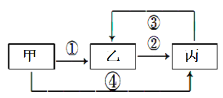
A.若甲为气态氢化物,乙为淡黄色固体,则丙具有漂白性
B.若甲为气体单质,乙为含有极性共价键的非极性分子,则反应②为吸热反应
C.若甲为金属氧化物,乙的水溶液呈酸性,则丙既能与强酸又能与强碱反应
D.若甲为金属单质,反应④为置换反应,则往乙溶液中滴加KSCN,溶液变为血红色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com