
| 化合物 | 密度/g•cm-3 | 沸点/℃ | 溶解性 |
| 正丁醇 | 0.810 | 118.0 | 可溶 |
| 冰醋酸 | 1.049 | 118.1 | 互溶 |
| 乙酸正丁酯 | 0.882 | 126.1 | 微溶 |
| 乙醇 | 0.79 | 78.5 | 互溶 |
| 乙酸乙酯 | 0.88 | 77.06 | 可溶 |
分析 I.(1)根据酯化反应原理酸脱羟基醇脱氢写出反应的化学方程式,在浓硫酸作用下正丁醇可能发生消去反应等副反应;
(2)“边反应边蒸馏”的方式收集产物的要求是反应物的沸点要高于生成物的沸点,而乙酸丁酯的沸点比乙酸、丁醇的沸点高,据此答题;
II.(1)乙酸正丁酯粗产品中含有乙酸、正丁醇、硫酸等杂质,要进行精制,要先用水洗除去部分可溶性杂质,再用碳酸钠溶液除硫酸,再水洗除碳酸钠,再用无水MgSO4干燥后再蒸馏得较纯的乙酸正丁酯;
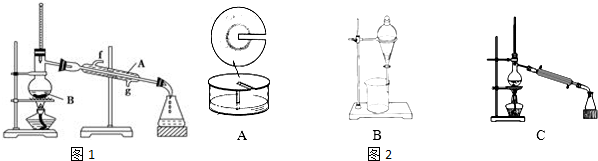
(2)①根据装置图可知图1中仪器A的名称,冷却时采用逆流冷却效果好,据此判断;
②根据乙酸正丁酯的沸点确定蒸馏时的温度;
III.(1)提高1-丁醇的利用率,可使平衡向生成酯的方向移动,根据平衡移动原理分析;
(2)互溶的液体可原理蒸馏的原理进行分离,据此设计;
解答 解:I.(1)酯化反应中酸脱羟基醇脱氢,反应的化学方程式为CH3COOH+CH3CH2CH2CH2OH $?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH2CH2CH3+H2O,在浓硫酸作用下正丁醇可能发生消去反应或取代生成醚等副反应,其产物为CH2═CHCH2CH3或CH3CH2CH2CH2OCH2CH2CH2CH3,
故答案为:CH3COOH+CH3CH2CH2CH2OH $?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH2CH2CH3+H2O;CH2═CHCH2CH3或CH3CH2CH2CH2OCH2CH2CH2CH3;
(2)“边反应边蒸馏”的方式收集产物的要求是反应物的沸点要高于生成物的沸点,而乙酸丁酯的沸点比乙酸、丁醇的沸点高,所以乙酸正丁酯的制备过程中不能否采用“边反应边蒸馏”的方式,
故答案为:不可以,因为乙酸正丁酯的沸点比乙酸和正丁醇都高;
II.(1)乙酸正丁酯粗产品中含有乙酸、正丁醇、硫酸等杂质,要进行精制,要先用水洗除去部分可溶性杂质,再用碳酸钠溶液除硫酸,再水洗除碳酸钠,再用无水MgSO4干燥后再蒸馏得较纯的乙酸正丁酯,故选C;
(2)①根据装置图可知图1中仪器A的名称为冷凝管,冷却时采用逆流冷却效果好,所以冷却水从g口进入,
故答案为:冷凝管;g;
②根据题意可知,乙酸正丁酯的沸点为126.1℃,所以蒸馏时的温度应控制在126.1℃左右,
故答案为:126.1℃;
III.(1)提高1-丁醇的利用率,可使平衡向生成酯的方向移动.
A.使用催化剂,缩短反应时间,平衡不移动,故A错误;
B.加过量乙酸,平衡向生成酯的方向移动,1-丁醇的利用率增大,故B正确;
C.不断移去产物,平衡向生成酯的方向移动,1-丁醇的利用率增大,故C正确;
D.缩短反应时间,反应未达平衡,1-丁醇的利用率降低,故D错误.
故选:BC.
(2)由表中数据可知,乙酸丁酯与乙酸乙酯沸点相差比较大,乙酸乙酯沸点为77.06℃,可利用蒸馏原理,将制得的乙酸丁酯进行蒸馏,故选C装置,看能否得到78℃左右的馏分,且该馏分不溶于饱和碳酸钠溶液,若有则说明含有乙酸乙酯,没有则不含乙酸乙酯.
故答案为:C;将制得的乙酸丁酯进行蒸馏,看能否得到78℃左右的馏分,且该馏分不溶于饱和碳酸钠溶液.
点评 本题以考查乙酸乙酯的制备为载体,旨在考查学生对知识的迁移运用,题目难度中等,注意基础知识的积累.


科目:高中化学 来源: 题型:解答题
| 嫦娥一号 | 液氢(H2) | ①2H2(g)+O2(g)=2H2O(l)△H=-571.6kJ•mol-1 ②2H2(l)+O2(l)=2H2O(g)△H=-482.6kJ•mol-1 |
| 祥云火炬 | 丙烷 (C3H8) | ③C3H8(l)+5O2(g)=3CO2(g)+4H2O(g)△H=-2013.8kJ•mol-1 ④C3H8(g)+5O2(g)=3CO2(g)+4H2O(l)△H=-2221.5kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,2.24LH2O含有的分子数等于0.1NA | |
| B. | 标准状况下,2.24L Cl2通入足量NaOH溶液中,反应转移电子的数目为0.1NA | |
| C. | 25℃时,pH=13的1.0LBa(OH)2溶液中含有的OH-数目为0.2NA | |
| D. | 18g重水(D2 O)所含的电子数为10NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在氮化铝的合成反应中,N2是还原剂,Al2O3是氧化剂 | |
| B. | 上述反应中每生成2 mol AlN,N2得到3 mol | |
| C. | 氮化铝中氮元素的化合价为-3 | |
| D. | 氮化铝晶体属于分子晶体,熔点和沸点较低 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 15mol•L-1 | B. | 10mol•L-1 | C. | 5mol•L-1 | D. | 1mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 两个反应均为氧化还原反应 | |
| B. | CO2与SO2不能用澄清石灰水鉴别 | |
| C. | CO2分子中各原子最外层均为8电子稳定结构 | |
| D. | 相同条件下:2CO(g)+SO2(g)=S(g)+2CO2(g)△H=+270kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com