
����Ŀ��
��1�������Ƶ�ˮ��Һ�׳� �� ��̼��������Һ�е���1��2�η�̪��Һ����Һ��ɫ��
��2��Fe(OH)3�����������ˮ����ȡ����Fe(OH)3�������Թ��У����Թ����μ�ϡ����������������������Ϊ��
��3��ʵ����ʢװNaOH��Һ���Լ�ƿ�����ò��������Է�ֹ������Ӧ�������ӷ���ʽ����
��4����Al��Na�ĵ���ͬʱ���뵽һ������ˮ�У���ַ�Ӧ���ּ����������������������ڣ�����������ѧ��Ӧ����ʽ��ʾ��仯��
����
����
��5����֪��5NH4NO3 ![]() 2HNO3+4N2��+9H2O����÷�Ӧ�����������뻹ԭ�����������Ϊ��
2HNO3+4N2��+9H2O����÷�Ӧ�����������뻹ԭ�����������Ϊ��
���𰸡�
��1��ˮ��������
��2���Ⱦ۳� ���ܽ�
��3��SiO2+2OH-=SiO32-+H2O
��4��2Na+H2O=2NaOH+H2����2Al+2NaOH+2H2O=2NaAlO2+3H2��
��5��5��3
����������1�������Ƶ�ˮ��Һ�׳�ˮ������̼��������Һ�Լ��ԣ���̼��������Һ�е���1��2�η�̪��Һ����Һ�Ժ�ɫ��
��2��ȡ����Fe(OH)3�������Թ��У����Թ����μ�ϡ�������������������ȷ����۳����������ɫ���������������������ܽ��������������Ȼ�����ˮ�����Բ���������Ϊ�۳������ܽ⡣
��3�������к��ж������裬����NaOH��Һ��Ӧ������Ժ�ǿ�Ĺ����ƣ���˲����ò��������Է�Ӧ�����ӷ���ʽΪSiO2+2OH-��SiO32-+H2O��
��4��������ˮ�����������ƺ�����������ʽΪ2Na+2H2O��2NaOH+H2�������ɵ��������ƿ����ܽ���������ƫ�����ƺ���������Ӧ�ķ���ʽΪ2Al+2NaOH+2H2O��2NaAlO2+3H2����
��5��笠��е�Ԫ�ػ��ϼ۴ӣ�3�����ߵ�0�ۣ�ʧȥ3�����ӡ�������е�Ԫ�ػ��ϼ۴ӣ�5�۽��͵�0�ۣ��õ�5�����ӣ����Ը��ݵ��ӵ�ʧ�غ��֪�÷�Ӧ�����������뻹ԭ�����������Ϊ5��3��


 Ӧ�����������Ĵ���ѧ������ϵ�д�
Ӧ�����������Ĵ���ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ڼ��Լ״�ȼ�ϵ�ص�������Ӧ���ҵ缫��Ӧʽ��д��ȷ����( )
A. CH3OH-6e-=CO2��+2H2OB. O2+4e-+2H2O=4OH-
C. CH3OH+6e-=CO32-+4OH-D. O2+4e-=2O2-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ϩ�Ʋ��ϩ��CH2=CH��CH3���Ľṹ��������ȷ���ǣ� ��
A.����ʹ���Ը��������Һ��ɫ
B.�����ڿ�����ȼ��
C.��ʹ��ˮ��ɫ
D.��HCl��һ���������ܼӳ�ֻ�õ�һ�ֲ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о������Ŷո�ʴ�������ǿ纣���ŵ���Ҫ���⣮�����й��ж�����ȷ���ǣ� �� 
A.��װ�â�ģ���о�ʱδ��a�������ݣ�˵����û�б���ʴ
B.�����Ŷ�����ӵ�Դ����������ȷ���Ŷղ�����ʴ
C.���в������������������������������Ŷ�
D.�٢ڢ��к�ˮ����ʵ�ֻ�ѧ��������ת���ĵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������һ�����Һ��ֻ���ܺ������������е������֣�Na+��NH4+��Cl����Ba2+��CO32����SO42����OH�� �� ��ȡ���ݸ�100 mL����Һ��������ʵ�飨ÿ��ʵ�����������ȫ��������ʵ��������д��Ӧ���ۣ�
��1����һ�ݼ�����NaOH��Һ���Ⱥ��ռ���0.68gNH3���壬ԭ��Һ��һ����������
��2���ڶ��ݼ�����BaCl2��Һ�ø������6.27 g������������ϴ�ӡ������������Ϊ2.33 g��
�ۺ�����ʵ�飬ԭ��Һ��һ�������� �� һ����������
��3�������ݼ���AgNO3��Һ�г���������
ԭ��Һ�л�һ������ �� ���ܴ�������û�У����վ��ɲ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��
��1�����ӹ�ҵ����FeCl3��Һ����ʴҺ����ӡˢ��·�塣��FeCl3����ʴҺ��Cu��Ӧ��ԭ��Ϊ��2FeCl3+Cu=2FeCl2+CuCl2��һ�������ۺ�ͭ�۵Ļ��������Ũ�ȵ�FeCl3��CuCl2�Ļ����Һ�У��ɷ��������Ӧ���������ȷ�����Ӧ�����ӷ���ʽΪ����
��2��ijУ�о���ѧϰС����������(Fe2O3)�ķ���м����ӡˢ��·��ĸ�ʴҺ(FeCl3��Һ)��������ʴ��·���ķ�Һ����ΪFeCl3��Һѭ��ʹ�á�ʵ���������£�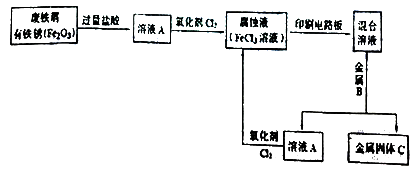
�����ʹ������д�����з�Ӧ�����ӷ���ʽ��
��ҺA����ʴҺ����
�����Һ+����B����������C����
��3�����鸯ʴҺ��Fe3+���ڵij����Լ��� �� ֤��Fe3+���ڵ���������
��4��ȡ���������Һ���Թ��У�����һ���������ۣ�����Ӧ�������Թ��������������壬�������һ������ �� ��Һ�п��ܺ��еĽ�������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪BΪ��ɫ��ĩ����D��E��G����ɫ��Ӧʵ�飬����ɫ�ܲ����۲죬��ɫ������ɫ��FΪ�����ɫҺ�壬H��ʹ���۱���������֮����ת����ϵ��ͼ1��ʾ�� 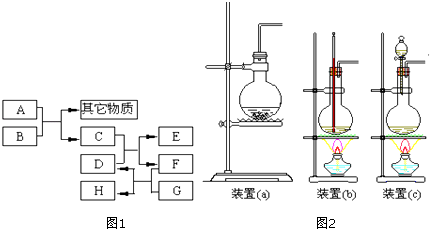
��1����������Ϲ�ϵ�����жϣ�ָ���������ʵĻ�ѧʽ��
A �� C �� D �� G ��
��2��д�����з�Ӧ�Ļ�ѧ����ʽ��C+D����A+B�� ��
��A��B�ķ�Ӧ�У�A��ʾ����������������д��ţ���ѡ���ۣ���
��ֻ�л�ԭ�ԣ��ڻ�ԭ�Ժ����ԣ���ֻ�������ԣ��������Ժ�����
��A��B���з�Ӧʱ��Ӧѡ��ͼ2��ʾװ���е���Ϊ���ʣ�
��3��C���������·�Ӧ�Ƶã�KClO3+6HCl=KCl+3Cl2��+3H2O���ڸ÷�Ӧ�У�����������Ԫ���뱻��ԭ����Ԫ�ص����ʵ���֮��Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʵ������ȡSO2����֤SO2ijЩ���ʵ�װ��ͼ�����۲쵽װ�â����е���ɫ�������ɣ����е���ˮ��ɫ����֪����Br2����ˮ�ʺ���ɫ������ش�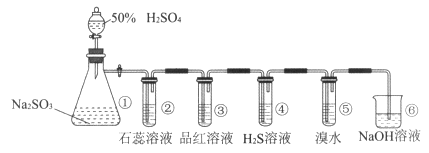
��1�����з�����Ӧ�����ӷ���ʽ����
��2�����е�ʵ����������
��3���۵�ʵ�������� �� ֤��SO2���ԡ�
��4������SO2������
��5�����з�Ӧ��������ǿ�ᣬ�÷�Ӧ�����ӷ���ʽ�� �� ��1 molSO2���뷴Ӧʱ��ת�Ƶ��ӵ����ʵ�������
��6������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����д�ʩ�У��������ѧ��Ӧ���ʵ���
A. Zn��ϡ����ķ�Ӧ�У���ZnƬ����Zn��
B. KC103�ķֽⷴӦ�У��ʵ���߷�Ӧ�¶�
C. H202�ķֽⷴӦ�У���������MnO2
D. �ϳɰ��ķ�Ӧ�У�������ϵ����ѹ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com