
 下列各组物质中,能一步实现如图所示①~⑤转化关系的是( )
下列各组物质中,能一步实现如图所示①~⑤转化关系的是( )| X | Y | Z | W | |
| A | Fe3O4 | Fe | FeCl2 | FeCl3 |
| B | Al | Al2O3 | NaAlO2 | Al(OH)3 |
| C | H2SO4 | SO2 | S | SO3 |
| D | CH3CH2Br | CH2=CH2 | C2H5OH | CH2BrCH2Br |
| A. | A | B. | B | C. | C | D. | D |
分析 A.Al与Fe3O4反应生成Fe,Fe与盐酸反应生成FeCl2,Fe与氯气反应生成FeCl3,FeCl2与氯气反应FeCl3,FeCl3与Fe反应生成FeCl2;
B.Al与氧气反应生成Al2O3,Al2O3与NaOH反应生成NaAlO2,Al2O3不能直接转化为Al(OH)3,NaAlO2与少量酸反应生成Al(OH)3,Al(OH)3与NaOH反应生成NaAlO2;
C.硫酸与Cu反应生成二氧化硫,二氧化硫与硫化氢反应生成S,二氧化硫与氧气反应生成三氧化硫,S不能一步转化为SO3;
D.CH3CH2Br发生消去反应生成乙烯,乙烯与水加成反应生成乙醇,乙烯与溴水发生加成反应生成CH2BrCH2Br,乙醇不能一步转化为CH2BrCH2Br.
解答 解:A.Fe3O4$\stackrel{Al}{→}$Fe$\stackrel{HCl}{→}$FeCl2$\stackrel{Cl_{2}}{→}$FeCl3$\stackrel{Fe}{→}$FeCl2,Fe$\stackrel{Cl_{2}}{→}$FeCl3,均能一步实现转化,故A选;
B.Al2O3不能一步转化为Al(OH)3,故B不选;
C.S不能一步转化为SO3,故C不选;
D.C2H5OH不能一步转化为CH2BrCH2Br,二者相互转化不能一步实现,故D不选;
故选A.
点评 本题考查金属元素的单质及化合物的性质、有机物的性质等,为高频考点,综合考查元素化合物知识,把握物质的性质及发生的反应为解答的关键,注意一步实现转化,题目难度不大.


 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


 ,D→E的反应类型是取代反应.
,D→E的反应类型是取代反应. .
. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 14C与12C60中碳原子化学性质相同 | B. | 14C与14N的质量数相同 | ||
| C. | 14C是12C60的同素异形体 | D. | 14C与12C、13C互为同位素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
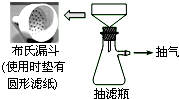 卷心菜中含有丰富的维生素C,维生素C在酸性溶液中能被碘氧化.某实验小组通过如下实验对卷心菜中维生素C的含量进行测定.
卷心菜中含有丰富的维生素C,维生素C在酸性溶液中能被碘氧化.某实验小组通过如下实验对卷心菜中维生素C的含量进行测定.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 $\stackrel{NaHCO_{3}溶液}{→}$X$\stackrel{NaOH溶液}{→}$Y$\stackrel{CO_{2}}{→}$Z$\stackrel{HCl}{→}$M$→_{浓H_{2}SO_{4}△}^{CH_{3}OH酯化}$N
$\stackrel{NaHCO_{3}溶液}{→}$X$\stackrel{NaOH溶液}{→}$Y$\stackrel{CO_{2}}{→}$Z$\stackrel{HCl}{→}$M$→_{浓H_{2}SO_{4}△}^{CH_{3}OH酯化}$N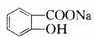 ,Y
,Y ,Z
,Z ,M
,M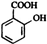 ,N
,N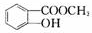 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题

| A. | 金属性:Z>Y | |
| B. | 气态氢化物的稳定性:M>N | |
| C. | X和Y形成的化合物中可能含共价键 | |
| D. | Z元素的离子半径是本周期元素离子半径最小的 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com