
科目:高中化学 来源: 题型:
下列说法错误的是( )
A.硅是制造太阳能电池的常用材料
B.二氧化硅是制造光导纤维的材料
C.常温下硅性质活泼,可以与氯气、强酸、强碱溶液等起反应
D.水玻璃可用作木材防火剂
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数的值。下列叙述正确的是 ( )
A.5. 6g铁粉在2.24L(标准状态)氯气中充分燃烧,失去的电子数为0.3NA
B.常温下,0.1mol/L CH3COOH溶液中所含的H+个数为0.1NA
C.CO和N:为等电子体,22. 4L的CO气体与Imol N2所含的电子数相等
D.13.0g锌与一定量浓硫酸恰好完全反应,生成气体分子数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
相同温度度,体积均为0.25L的两个恒容器中发生可逆反应:
X2(g)+2Y2(g)  2XY3(g)△H=-92.6kJ·mol-1,实验测得反应在起始、达到平衡时的有关数据如下表所示:
2XY3(g)△H=-92.6kJ·mol-1,实验测得反应在起始、达到平衡时的有关数据如下表所示:
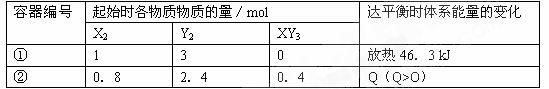
下列叙述不正确的是 ( )
A.容器①、②中反应的平衡常数相等
B.容器①、②中达到平衡时各物质的百分含量相同
C.达平衡时,两个容器中XY3的物质的量浓度均为2 mol·L-1
D.若容器①体积为0.20L.则达平衡时放出的热量大于46.3kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)某实验小组设计一套仿甲烷燃料电池,如右图所示。①该电池正极的电极反应为 。
②用该电池电解(惰性电极)500mL某CuSO4溶液,电解一段时间后,为使电解质溶液恢复到原状态,需要向溶液中加入9.8g Cu(OH)2固体。则原CuSO4溶液的物质的量浓度为 ,电解过程中收集到标准状况下的气体体积为 。
(2)希腊阿里斯多德大学的Ge orge Marnellos和Michael Stoukides,发明了一种合成氨的新方法,在常压下,把氢气和用氦气稀释的氮气分别通入一个加热到570℃的电解池,利用能通过氢离子的多孔陶瓷固体作电解质,氢气和氮气在电极上合成了氨,转化率达到78%,试写出电解池阴极的电极反应式 。
orge Marnellos和Michael Stoukides,发明了一种合成氨的新方法,在常压下,把氢气和用氦气稀释的氮气分别通入一个加热到570℃的电解池,利用能通过氢离子的多孔陶瓷固体作电解质,氢气和氮气在电极上合成了氨,转化率达到78%,试写出电解池阴极的电极反应式 。

查看答案和解析>>
科目:高中化学 来源: 题型:
关于蛋白质的叙述不正确的是( )
A、人工合成具有生命活力的蛋白质——结晶牛胰岛素是我国科学家1965年首次合成的
B、在蛋白质溶液中加入饱和硫酸铵溶液,蛋白质析出,若再加水,也不溶解
C、重金属盐类能使蛋白质凝结变性,所以误食重金属盐能使人中毒
D、浓HNO3溅在皮肤上能使皮肤呈现黄色,是由于浓HNO3和蛋白质发生了颜色反应
查看答案和解析>>
科目:高中化学 来源: 题型:
.I.下列四支试管中,过氧化氢分解的化学反应速率最大的是
| 试管 | 温度 | 过氧化氢浓度 | 催化剂 |
| a | 室温(25℃) | 12% | 有 |
| b | 水浴加热(50℃) | 4% | 无 |
| c | 水浴加热(50℃) | 12% | 有 |
| d | 室温(25℃) | 4% | 无 |
II.某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照如下方案完成实验。
| 实验编号 | 反应物 | 催化剂 |
| ① | 10mL2% H2O2溶液 | 无 |
| ② | 10mL5% H2O2溶液 | 无 |
| ③ | 10mL5% H2O2溶液 | 1mL0.1mol·L-1FeCl3溶液 |
| ④ | 10mL5% H2O2溶液+少量HCl溶液 | 1mL0.1mol·L-1FeCl3溶液 |
| ⑤ | 10mL5% H2O2溶液+少量NaOH溶液 | 1mL0.1mol·L-1FeCl3溶液 |
(1)实验①和②的目的是____________________________。
 (2)写出实验③的化学反应方程式 。
(2)写出实验③的化学反应方程式 。
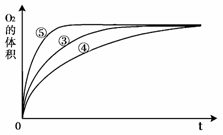
(3)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如右图。
分析右图能够得出的实验结论是
_________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com